Clear Sky Science · de
Genomweite Screens identifizieren Kernregulatoren der zelloberflächlichen Prionproteinausprägung
Warum das für die Gesundheit des Gehirns wichtig ist
Prionerkrankungen wie die Creutzfeldt‑Jakob‑Krankheit beim Menschen und die BSE‑Krankheit ("Rinderwahn") bei Rindern sind selten, aber stets tödliche Erkrankungen des Gehirns. Ein zentraler Übeltäter ist ein im Gehirn natürlich vorkommendes Protein, das Prionprotein, das fehlgefaltet sein und sich von Zelle zu Zelle ausbreiten kann. Je mehr dieses Proteins an der Oberfläche von Nervenzellen vorhanden ist, desto leichter kann die Krankheit Fuß fassen. Diese Studie hatte zum Ziel, genomeweit zu kartieren, welche Gene steuern, wie viel Prionprotein an der Außenseite von neuronähnlichen Zellen erscheint. Diese Karte kann Forschern helfen, neue Wege zu entwickeln, dieses Protein zu reduzieren und möglicherweise verschiedene neurodegenerative Erkrankungen zu verlangsamen.
Die Stellräder der Zelle finden
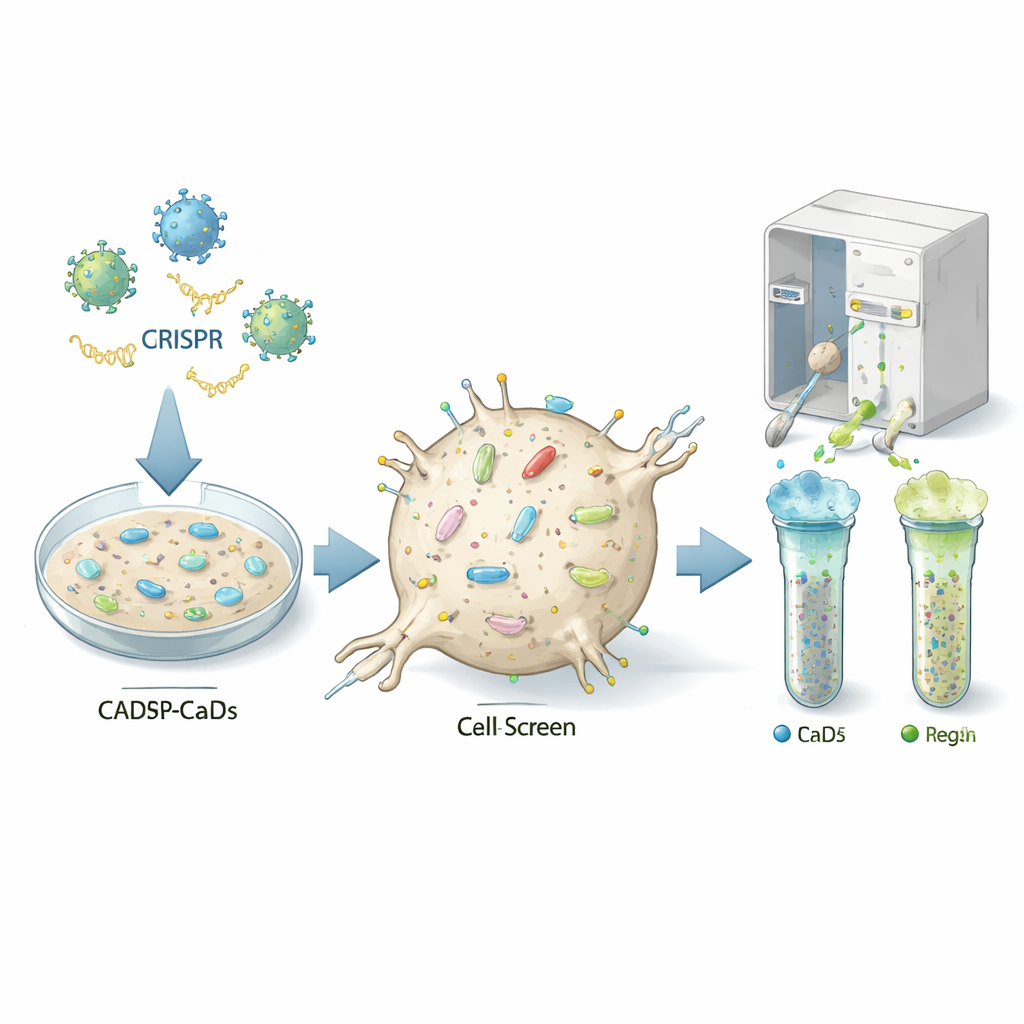
Die Autorinnen und Autoren nutzten einen leistungsfähigen Geneditieransatz namens CRISPR, um nahezu jedes Gen einzeln in einer mausstammigen, neuronähnlichen Zelllinie auszuschalten, die für Prioninfektionen empfänglich ist (sogenannte CAD5‑Zellen). Jede Zelle erhielt einen anderen genetischen "Treffer", sodass die resultierende Population Millionen von Varianten enthielt, von denen jeweils ein spezifisches Gen fehlte. Das Team färbte die Zellen anschließend mit fluoreszierenden Antikörpern an, die das normale Prionprotein an der Zelloberfläche erkennen, und trennte mit einer Zellsortiermaschine Zellen mit ungewöhnlich niedrigen oder hohen Proteinmengen. Durch das Sequenzieren der in den niedrigen bzw. hohen Gruppen angereicherten Guide‑RNAs konnten sie ableiten, welche ausgeschalteten Gene normalerweise als Ein‑ oder Ausschalter für das Prionprotein an der Zelloberfläche wirken.
Zwei Zellzustände, überlappende Antworten
Nervenzellen sehen im Laufe ihrer Entwicklung nicht alle gleich aus und verhalten sich auch unterschiedlich. Daher prüften die Forschenden, ob dieselben Gene das Prionprotein in verschiedenen Zellzuständen steuern. CAD5‑Zellen lassen sich in einem schnell wachsenden, weniger spezialisierten Zustand halten oder durch Entzug von Serum aus dem Kulturmedium in eine reifere, neuronähnlichere Form überführen. Das Team führte den gleichen genomweiten CRISPR‑Screen unter beiden Bedingungen durch. In den undifferenzierten (weniger reifen) Zellen validierten sie 46 Gene, die die Menge des Oberflächen‑Prionproteins erhöhen, und 21, die sie verringern. In den differenzierten (stärker neuronähnlichen) Zellen bestätigten sie 41 positive und 13 negative Regulatoren. Dreiundzwanzig Gene – überwiegend solche, die beim Anheften eines Lipid‑"Ankers" an das Protein helfen – wurden in beiden Zellzuständen geteilt, was eine Kernregulationsmaschinerie hervorhebt, die unabhängig vom Reifegrad wirkt.
Zentrale Produktionslinien, die am wichtigsten sind
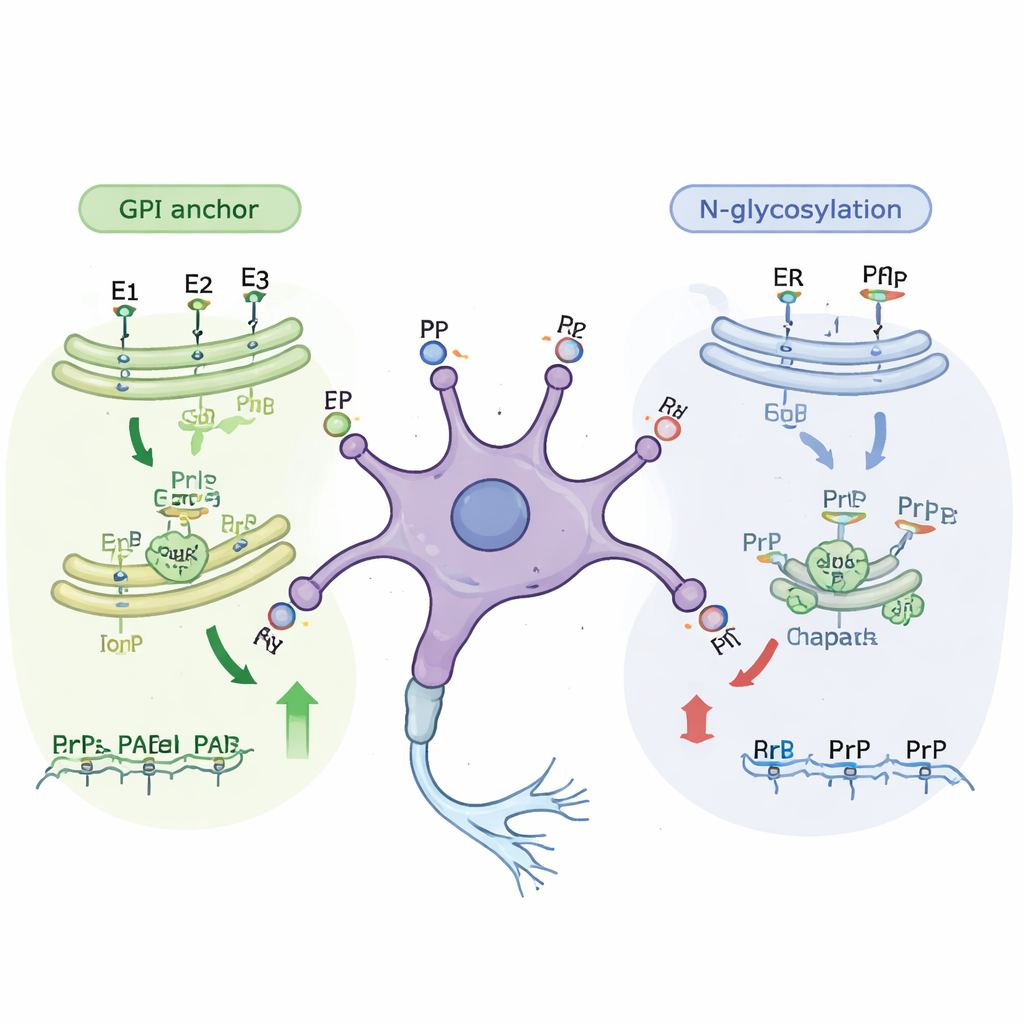
Weitere Analysen zeigten, dass viele der neu identifizierten Gene zu bekannten zellulären "Produktionslinien" gehören, die Proteine verändern, während sie zur Zelloberfläche transportiert werden. Ein wichtiger Weg baut den GPI‑Anker auf, eine fettreiche Struktur, die das Prionprotein an der Außenseite der Zellmembran verankert. Die Störung nahezu jedes Schritts in diesem Weg verringerte, in sowohl unreifen als auch reifen Zellen, wie viel Prionprotein die Oberfläche erreichte. Ein zweiter Weg betrifft die N‑gebundene Glykosylierung, bei der komplexe Zuckerketten an Proteine angehängt werden, während diese durch die inneren Membranen der Zelle passieren. Gene in diesem Zuckeranhängeweg traten vor allem in den weniger reifen Zellen als wichtig hervor. Als die Forschenden die Zellen mit kleinen Molekülen behandelten, die spezifische Glykosylierungsschritte blockieren, fielen die Oberflächen‑Prionproteinmengen um etwa ein Drittel, ohne die Zellen abzutöten, was die genetischen Befunde bestätigte.
Hilfsproteine und Stressreaktionen
Die Screens hoben außerdem molekulare Chaperone – Proteine, die anderen Proteinen beim richtigen Falten helfen – als wichtige Prionregulatoren hervor. Insbesondere Hspa5 (auch BiP genannt), ein zentrales Chaperon im Proteinfaltungs‑Kompartiment der Zelle, erwies sich in den stärker neuronähnlichen Zellen als positiver Regulator. Als die Forschenden Hspa5 mit einem Wirkstoff hemmten, sanken die Oberflächen‑Prionproteinmengen in beiden Zellzuständen, wiederum ohne offensichtliche Schädigung der Zellen. Weitere Treffer umfassten Gene, die am Proteintransport durch die Zelle beteiligt sind, die Steuerung der Genaktivität sowie mehrere Proteine, die mit Synapsenfunktion und anderen Hirnerkrankungen wie Alzheimer und ALS in Verbindung stehen. Zusammengenommen zeigen diese Ergebnisse, dass die Prionproteinmengen an der Zelloberfläche durch ein Netzwerk von Wegen geformt werden, das Proteinsynthese, Modifikation, Transport und Qualitätskontrolle umfasst.
Was das für künftige Behandlungen bedeutet
Diese Arbeit liefert den ersten umfassenden Katalog von Genen, die steuern, wie viel Prionprotein an der Oberfläche neuronähnlicher, prionanfälliger Zellen erscheint. Einige dieser Gene, insbesondere solche in den GPI‑Anker‑ und N‑Glykosylierungswegen sowie das Hspa5‑Chaperonsystem, erscheinen als vielversprechende Ansatzpunkte für die Wirkstoffforschung: Ihre Aktivität zu drosseln sollte die Menge an verfügbarem Prionprotein reduzieren, das fehlgefaltet werden kann, und frühere Studien zeigen, dass selbst partielle Reduktionen Krankheitsverläufe bei Tieren deutlich verzögern können. Gleichzeitig unterstreichen die deutlichen Unterschiede zwischen unreifen und reifen Zellen, dass der Zustand der Gehirnzellen bei der Auswahl von Zielstrukturen eine Rolle spielt. Zwar sind weitere Studien nötig, um zu prüfen, wie die Manipulation dieser Gene tatsächliche Prioninfektionen und andere neurodegenerative Erkrankungen in lebenden Gehirnen beeinflusst, doch bietet diese Studie eine Landkarte zellulärer Hebel, die Forschende erkunden können, um diese verheerenden Krankheiten zu verlangsamen oder zu verhindern.
Zitation: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
Schlüsselwörter: Prionprotein, CRISPR-Screen, Neurodegeneration, Protein-Glykosylierung, GPI-Anker