Clear Sky Science · de
Druckverstärktes Dual-Feststoff-Oberflächen-Ultrakurzkühlen verbessert die Erholung nach Auftauen in Hepatozyten und präzise geschnittenen Leberstücken
Warum das Einfrieren von Lebergewebe wichtig ist
Zellen und Gewebe außerhalb des Körpers am Leben zu erhalten, ist eine der stillen Stützen der modernen Medizin. Eingefrorene Leberzellen helfen Forschern, neue Medikamente zu testen, Krankheiten zu modellieren und könnten eines Tages versagende Organe reparieren. Das Einfrieren lebenden Materials ist jedoch heikel: Wenn sich Eiskristalle innerhalb oder zwischen Zellen bilden, reißen sie empfindliche Strukturen auseinander. Diese Studie untersucht eine neue Methode, Leberzellen und dünne Leberabschnitte so schnell und unter so kontrollierten Bedingungen zu kühlen, dass schädliche Eiskristalle kaum Zeit haben, zu entstehen.
Das Problem mit Eis und chemischen Schutzmitteln
Konventionelle Kryokonservierung stützt sich auf zwei unvollkommene Mittel: Kälte und Chemikalien. Beim Abkühlen neigt Wasser dazu, Eis zu bilden, das Membranen durchstechen und Gewebe zerstören kann. Um dem entgegenzuwirken, fügen Wissenschaftler kryoprotektive Agenzien wie Dimethylsulfoxid (DMSO) hinzu, die Wasser helfen, in einen glasartigen Zustand statt in kristallines Eis zu übergehen. Bei den üblicherweise verwendeten hohen Konzentrationen können diese Agenzien jedoch selbst zellschädigend wirken oder beim Ein- und Ausdringen in das Gewebe schädliche Anschwell- und Schrumpfprozesse verursachen. Das Ziel der Autoren war, die benötigte DMSO-Menge zu reduzieren und gleichzeitig schädliches Eis zu vermeiden, um die Lagerung von Leberzellen und -gewebe sicherer und praktikabler zu machen.
Eine neue Methode, Druck und Kühlung gleichzeitig anzuwenden
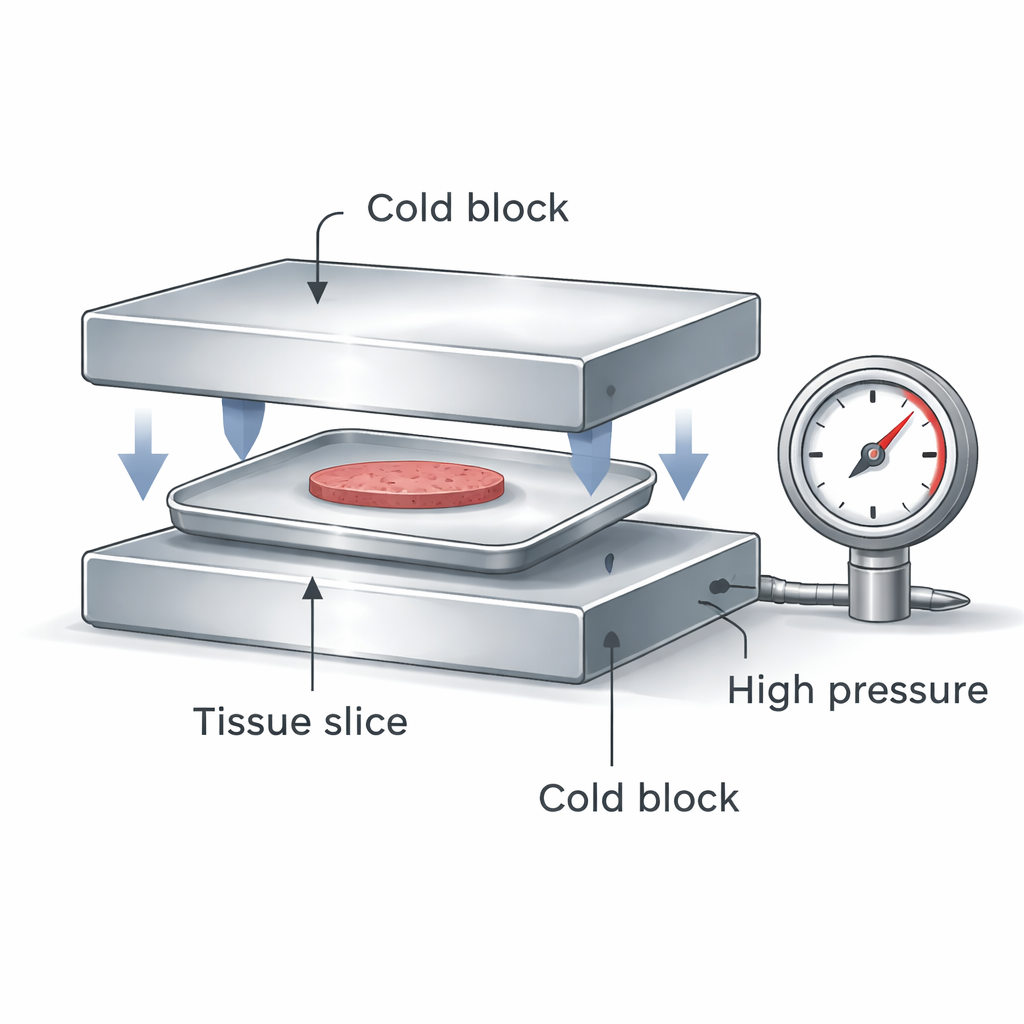
Das Team entwarf ein kompaktes Gerät, das einen versiegelten, flachen Aluminiumbehälter mit Leberzellen oder präzise geschnittenen Leberstücken zwischen zwei extrem kalte Metallblöcke klemmt. Wenn die Blöcke zusammenpressen, bewirken sie zwei wichtige Effekte gleichzeitig: Sie erzeugen hohen Druck im versiegelten Behälter und entziehen dem Probenmaterial sowohl von oben als auch von unten Wärme. Hoher Druck verschiebt das Verhalten von Wasser, sodass Eis bei niedrigeren Temperaturen entsteht und die Lösung leichter glasartig wird. Doppelseitiger Kontakt ermöglicht eine viel schnellere und gleichmäßigere Abkühlrate als das bloße Eintauchen einer Kunststoffampulle in flüssigen Stickstoff, und der versiegelte Behälter hält die Probe von Kontaminationen fern.
Das optimale Gleichgewicht für Sicherheit und Überleben finden
Um zu prüfen, ob dieser Ansatz schonend genug für lebendes Material ist, überprüften die Forscher zunächst, dass der Aluminiumbehälter selbst die aus der Leber stammenden HepG2-Zellen während der kurzen Handhabungszeiten nicht schädigt. Die Zellüberlebensrate blieb im Wesentlichen unverändert. Anschließend setzten sie diese Zellen vor dem Einfrieren verschiedenen DMSO-Konzentrationen aus und bestätigten ein bekanntes Abwägen: Mehr DMSO unterdrückt besser die Eisbildung, wird aber bei 30 % deutlich toxisch, während 20 % weitgehend tolerierbar bleibt. Für Mäuseleberstücke testeten sie, wie viel Druck das Gewebe ohne Einfrieren aushält. Kurze Druckstöße bis zu 150 Megapascal hatten kaum Einfluss auf die Vitalität, aber 200 Megapascal führten zu einem etwa 30%igen Rückgang und markierten damit eine obere Grenze für einen sicheren Betrieb.
Besser erhaltene Leberstücke nach dem Auftauen
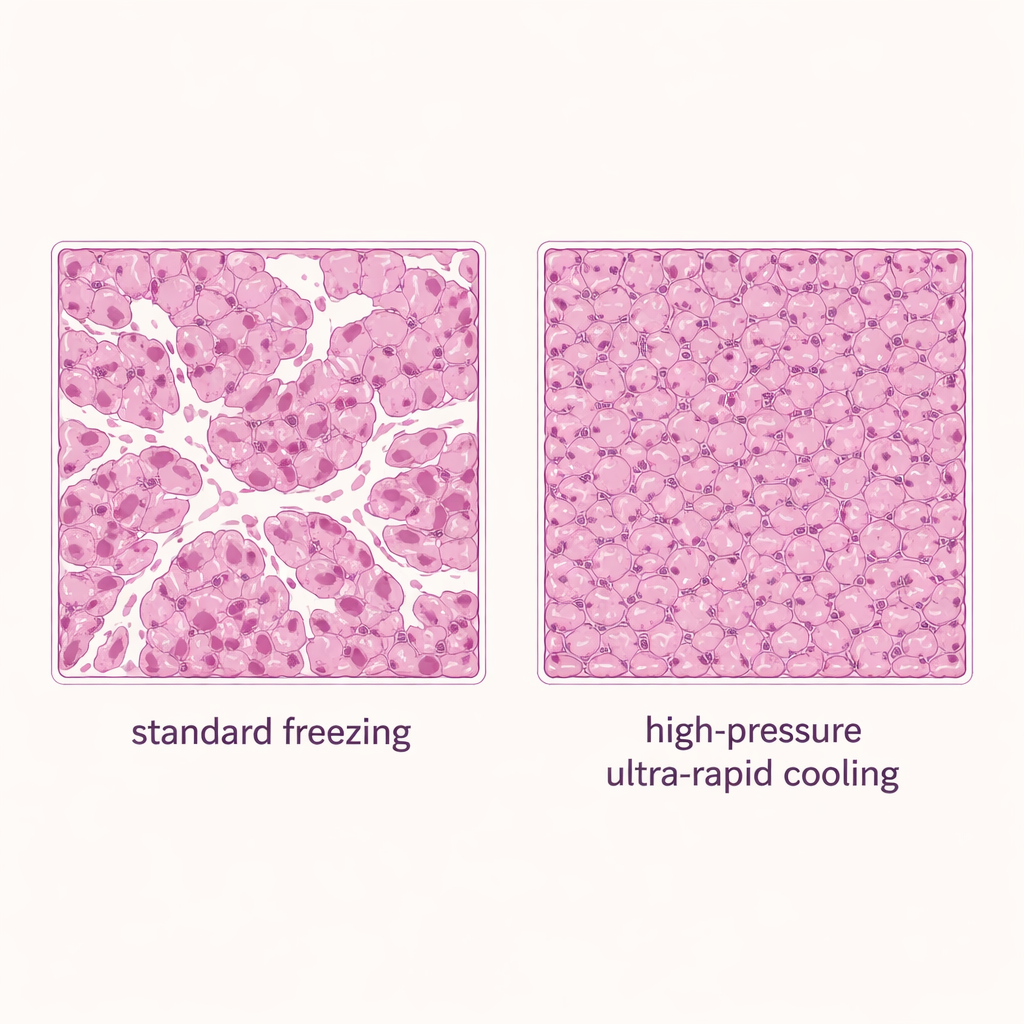
Nachdem sichere Bereiche festgelegt waren, verglichen die Autoren drei Einfrierungsmethoden für Leberstücke: das standardmäßige Eintauchen des versiegelten Behälters in flüssigen Stickstoff (ein konvektiver, also flüssigkeitsbasierter Ansatz), Festkörperflächenkühlung ohne zusätzlichen Druck und Festkörperflächenkühlung mit hohem Druck von 150 Megapascal. Alle Gruppen verwendeten 20% DMSO. Die druckunterstützte Methode lieferte die besten Ergebnisse: Etwa 80 % der ursprünglichen Gewebevitalität blieben erhalten und übertrafen sowohl das Standardverfahren als auch die Festkörperflächenkühlung allein. Die Mikroskopie gefärbter Gewebeschnitte stützte diese Befunde. Proben, die konventionell durch Eintauchen eingefroren wurden, zeigten viele offene weiße Räume — typische Spuren von Eisschäden — während das druckverstärkte Festkörperflächenkühlen dichtere, intaktere Gewebe mit deutlich weniger Lücken erzeugte.
Was das für die zukünftige Gewebebankierung bedeutet
Insgesamt zeigt die Studie, dass das Zusammendrücken eines versiegelten, in Aluminium eingeschlossenen Leberstücks zwischen zwei ultrakalten Blöcken unter kontrolliertem Hochdruck die Überlebensfähigkeit des Gewebes nach dem Auftauen deutlich verbessern kann. Durch die Kombination aus schnellerer, gleichmäßigerer Kühlung und durch Druck veränderten Wassereigenschaften begrenzt die Methode das Wachstum schädlicher Eiskristalle, während sie dennoch eine moderate, klinisch vertraute DMSO-Konzentration verwendet. Für den Laien lautet die Botschaft: Intelligente Ingenieurslösungen — wie wir Gewebe verpacken und kühlen — können genauso wichtig sein wie die eingesetzten Chemikalien. Dieser doppelseitige, hochdruckgestützte Ansatz könnte ein Zwischenschritt hin zu sichererem, zuverlässigeren Lagern von Lebergewebe und schließlich auch anderer Organe für Forschung und Therapie sein.
Zitation: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Schlüsselwörter: Kryokonservierung, Lebergewebe, Vitrifikation, Hochdruckkühlung, eisfreies Einfrieren