Clear Sky Science · de
DANEELpath Open-Source-Tools zur digitalen Analyse für histopathologische Forschung an Neuroblastom-Modellen
Warum winzige Tumoren im Gel wichtig sind
Krebs ist nicht nur eine Ansammlung entarteter Zellen; es ist ein komplettes Umfeld, in dem Zellen miteinander und mit dem umgebenden Gerüst kommunizieren. Bei Kinderkrebserkrankungen wie dem Neuroblastom kann diese umgebende Stützstruktur das Tumorwachstum fördern und die Behandlung behindern. Diese Studie stellt DANEELpath vor, eine kostenlose Open-Source-Sammlung digitaler Werkzeuge, die Mikroskopbilder von im Labor gezüchteten Mini-Tumoren in reichhaltige, quantitative Karten verwandelt. Damit hilft sie Forschern zu verstehen, wie Tumorzellen sich anordnen, wie sie auf experimentelle Wirkstoffe reagieren und wie diese Erkenntnisse zu besseren Therapien für Kinder beitragen könnten.
Kleine Tumorwelten im Labor erzeugen
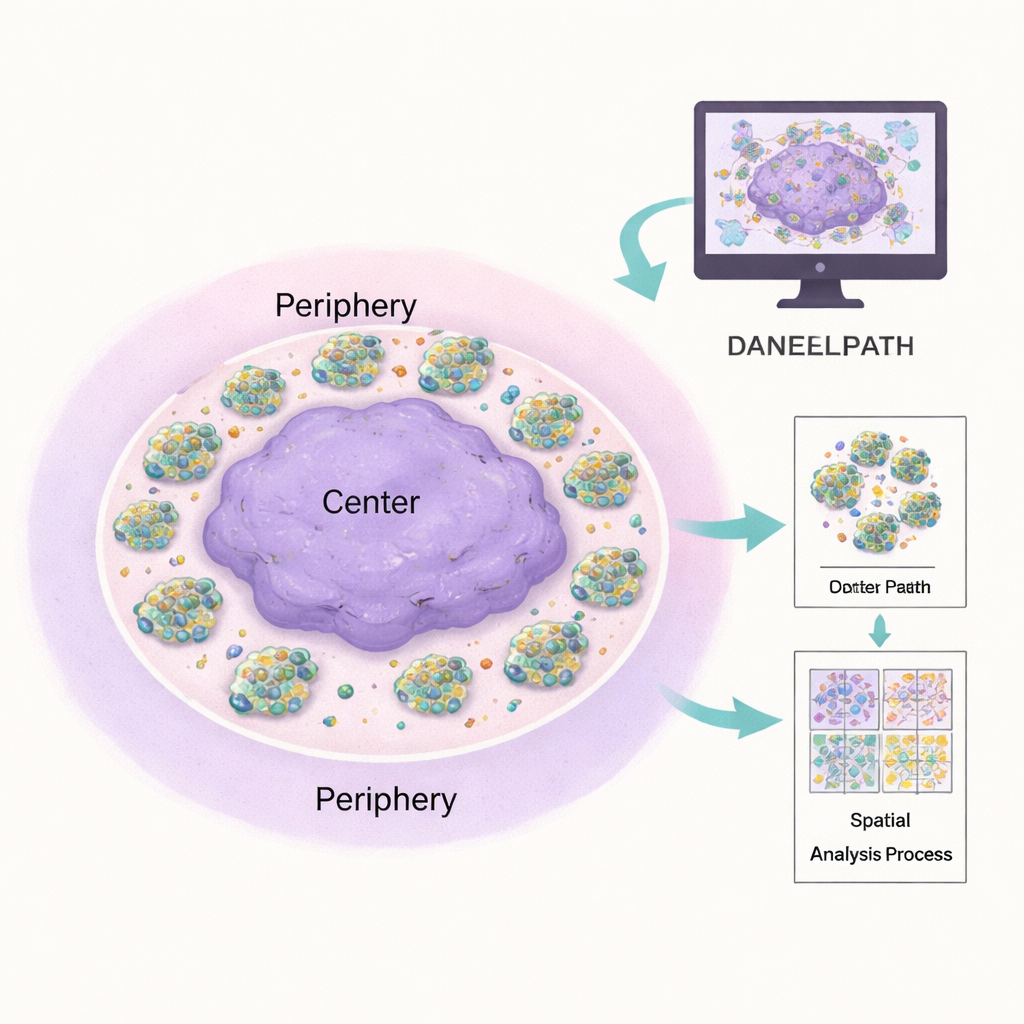
Um die komplexe Umgebung eines echten Tumors nachzubilden, züchten die Forschenden Neuroblastom-Zellen in weichen 3D-Hydrogelen aus Gelatine und Seide. In dieser Umgebung bilden die Zellen auf natürliche Weise runde Cluster, ähnlich winzigen Tumoren. Ein wichtiger Faktor ist Vitronectin, ein klebendes Protein in der extrazellulären Matrix, das die Zellhaftung fördert und zu aggressiverem Verhalten beitragen kann. Das Team bereitete Hydrogele mit und ohne zusätzliche Vitronectin vor und setzte einige davon Cilengitid aus, einem experimentellen Wirkstoff, der an Vitronectin-gebundene Zellrezeptoren blockiert. Nach mehreren Wochen Wachstum wurden die Gele aufgeschnitten, gefärbt und als hochauflösende Whole-Slide-Bilder gescannt, wodurch für jede Mini-Tumor-Welt eine digitale Version entstand.
Komplexe Bilder in messbare Muster verwandeln
Die traditionelle Pathologie beruht auf dem geschulten Auge am Mikroskop, was mächtig, aber schwer zu standardisieren und zu skalieren ist. DANEELpath integriert sich in die beliebte Open-Source-Plattform QuPath und automatisiert einen Großteil dieser Arbeit. Mit Deep-Learning-Modellen vom U-Net-Typ kann das Toolkit jede Zellansammlung in gängigen Färbungen präzise umreißen, selbst wenn Cluster von wenigen Zellen bis zu Hunderten variieren. Anschließend wendet es mathematische Methoden an, um jedes unregelmäßig geformte Hydrogel in einen ausgeglichenen "Zentrum"- und "Peripherie"-Ring zu teilen, sodass Vergleiche zwischen inneren und äußeren Regionen fair sind, unabhängig von der Form des Gels. Damit konnten die Autor:innen bestätigen, dass Neuroblastom-Cluster tendenziell dichter zum Hydrogelrand hin sind und dass dieses Muster sich je nach Vitronectin-Gehalt und Wirkstoffbehandlung verändert.
Abstände zwischen Zellen und Nachbarschaft der Cluster messen
Über das reine Zählen von Clustern hinaus untersucht DANEELpath, wie Zellen und Cluster räumlich angeordnet sind. Innerhalb jedes Clusters findet ein weiteres Werkzeug einzelne Zellkerne und misst den Abstand zum nächsten Nachbarn, um zusammenzufassen, wie dicht die Zellen gepackt sind. Zwischen Clustern bietet das Toolkit drei Arten, "Nachbarn" zu definieren, einschließlich einer Methode auf Grundlage von Voronoi-Diagrammen, die Einflusszonen um jedes Cluster zieht. Durch den Vergleich dieser Messungen unter unterschiedlichen Bedingungen zeigten die Forschenden, dass Cilengitid verändert, wie viele benachbarte Cluster ein großes Cluster hat und wie diese Nachbarn verteilt sind — aber in Abhängigkeit davon, ob dem Gel Vitronectin zugesetzt wurde. Das unterstreicht, wie die umgebende Matrix und mechanisch wirksame Medikamente gemeinsam die Tumororganisation formen.
Den Halo um Tumorcluster sehen
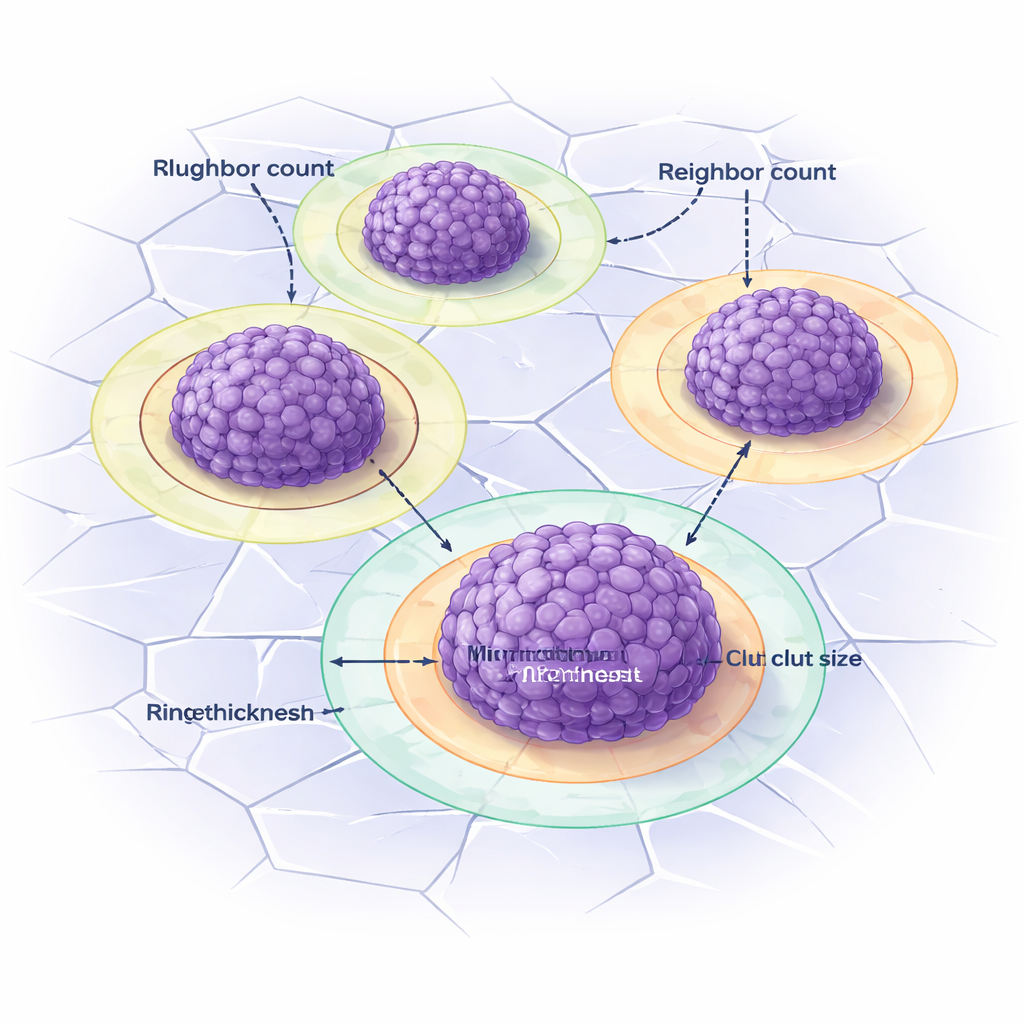
Vitronectin bildet in diesen Modellen oft auffällige Ringe um Cluster: eine helle "Korona", wenn nur zellproduziertes Vitronectin vorhanden ist, und einen blassen Halo, wenn zusätzliches Vitronectin ins Gel eingebaut wurde. Diese Ringe mit bloßem Auge vom Clusterkern zu trennen, ist schwierig. DANEELpath begegnet dem, indem es zunächst Voronoi-basierte Einflussregionen um jedes Cluster zieht und diese dann nur soweit nach außen erweitert, dass der Ring erfasst wird, ohne Nachbarn zu überlappen. Einfache Bildkontrast-Regeln werden benutzt, um Koronen und Halos zu erkennen, und das Toolkit misst automatisch deren Dicke. Ähnliche Strategien wurden auch auf echte Patientenproben angewendet, zum Beispiel um Immunzellen am Rand von Tumorregionen zu kartieren oder Zonen um Blutgefäße zu definieren, um zu untersuchen, wie Vitronectin und andere Marker im menschlichen Neuroblastom angeordnet sind.
Was das für die zukünftige Krebsforschung bedeutet
Im Kern verwandelt diese Arbeit statische pathologische Bilder in detaillierte, reproduzierbare Messungen darüber, wie Tumorzellen und ihr Umfeld organisiert sind. Für Nicht-Spezialisten bedeutet das: Forschende können nun leichter testen, wie neue Wirkstoffe, Gerüstmaterialien oder genetische Veränderungen nicht nur das Tumorwachstum beeinflussen, sondern wie sich Wachstum räumlich gestaltet. Da DANEELpath Open-Source ist, über eine grafische Oberfläche läuft und auf normalen Computern funktioniert, senkt es die Einstiegshürden für Labore weltweit, fortgeschrittene Bildanalysen zu übernehmen. Mit der Zeit könnten solche Werkzeuge helfen, Muster in 3D-Modellen und Patientenproben mit klinischen Ergebnissen zu verknüpfen und so gezieltere und effektivere Behandlungen für Kinder mit Hochrisiko-Neuroblastom zu leiten.
Zitation: Vieco-Martí, I., López-Carrasco, A., Navarro, S. et al. DANEELpath open source digital analysis tools for histopathological research in neuroblastoma models. Sci Rep 16, 6162 (2026). https://doi.org/10.1038/s41598-026-37134-5
Schlüsselwörter: Neuroblastom, digitale Pathologie, 3D-Hydrogele, extrazelluläre Matrix, Deep Learning