Clear Sky Science · de
Iteratives Multiblock‑Framework zur Erkennung neurologischer Störungen auf Basis hochfrequenter EEG‑Signale
Warum Gehirnwellen für eine frühe Diagnose wichtig sind
Alzheimer und Parkinson schädigen das Gehirn oft Jahre bevor Symptome deutlich werden, doch Ärzten fehlen nach wie vor schnelle und zuverlässige Instrumente, um sie früh zu erkennen. Diese Studie stellt eine neue Methode vor, Hirnwellen, aufgezeichnet mittels Elektroenzephalographie (EEG), zu lesen, die sich auf die schnellsten Rhythmen des Gehirns konzentriert. Durch sorgfältiges Säubern dieser verrauschten Signale und deren Einspeisung in ein erklärbares System der künstlichen Intelligenz zeigen die Autoren, dass sich neurologische Probleme mit einer Genauigkeit erkennen lassen, die vielen bestehenden Ansätzen ebenbürtig ist und sie teilweise übertrifft.
Den schnellsten Gehirnrhythmen lauschen
EEG zeichnet winzige Spannungsänderungen an der Kopfhaut auf, wenn Netzwerke von Neuronen feuern. Traditionell richten Mediziner und Forscher den Blick vor allem auf langsamere Rhythmen wie Alpha‑ und Theta‑Wellen. Wachsende Evidenz deutet jedoch darauf hin, dass hochfrequente „Gamma“‑Aktivität, oberhalb von etwa 30 Hertz, frühe Anzeichen von Erkrankungen offenbaren kann – von subtilen Gedächtnisstörungen bis zu Bewegungsstörungen. Leider sind diese schnellen Signale leicht von Muskelzuckungen, Augenblinzeln und elektrischen Störungen überlagert. Standardwerkzeuge wie die bekannten Fourier‑ und Wavelet‑Transformationen funktionieren am besten, wenn Signale über Zeit stabil sind, was bei realen EEG‑Aufnahmen oft nicht der Fall ist. Deshalb war ein Großteil der klinisch relevanten Details in hochfrequenter Aktivität schwer zu extrahieren und leicht fehlzuinterpretieren.
Verrauschte Hirnsignale bereinigen
Um dieses Problem anzugehen, entwerfen die Autoren eine mehrstufige „Pipeline“, die EEG‑Analyse eher wie eine sorgfältig konstruierte Produktionskette als einen einzelnen magischen Algorithmus behandelt. Zunächst verwenden sie einen Ansatz aus der Hilbert–Huang‑Transformation kombiniert mit einer modifizierten empirischen Moduszerlegung. Einfach gesagt zerlegt diese Methode ein unruhiges Signal automatisch in einfachere Bausteine, die den tatsächlichen Schwankungen des Gehirns besser folgen. Anschließend werden Komponenten verworfen, die sich wie Rauschen verhalten – basierend auf ihrem geringen Energie‑ und Komplexitätsgehalt – während schnelle Oszillationen im Gamma‑Bereich erhalten bleiben. Diese zweistufige Filterung verbessert das Signal‑Rausch‑Verhältnis erheblich und verwandelt eine überlagerte Rohspur in eine sauberere Darstellung hochfrequenter Hirnaktivität, die eher echte neuronale Ereignisse als zufällige Artefakte widerspiegelt. 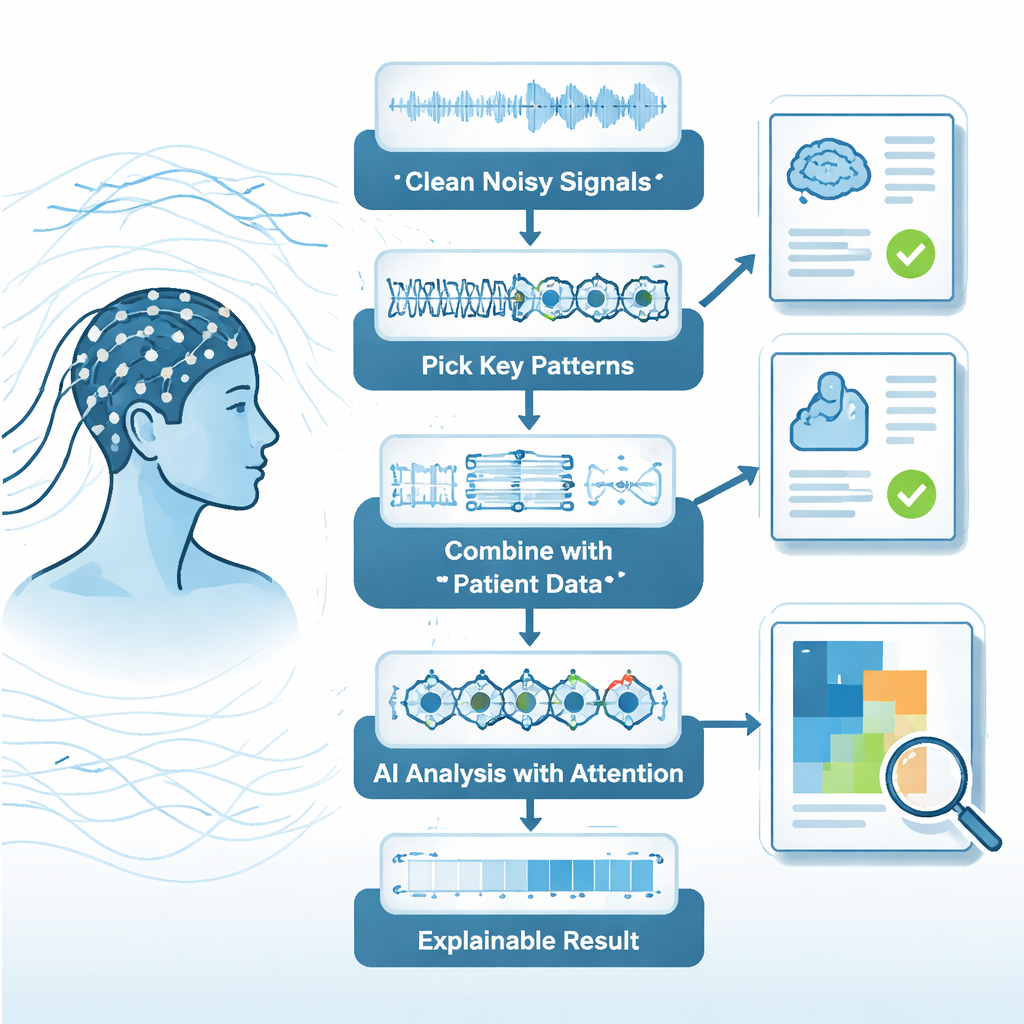
Die aufschlussreichsten Muster finden
Sobald die Signale bereinigt sind, konzentriert sich das Framework auf die informativsten Merkmale. Eine Wavelet‑Packet‑Transformation unterteilt jede EEG‑Komponente in mehrere Frequenzbänder, und ein Maß namens Shannon‑Entropie bewertet, wie komplex und aussagekräftig jedes Band ist. Bänder mit niedrigen Werten – die eher Redundanz als Einsicht hinzufügen – werden verworfen, wodurch der Merkmalsraum um etwa 60 % schrumpft, während rund 95 % der klinisch relevanten Information erhalten bleiben. Entscheidenderweise verlässt sich das System nicht allein auf das EEG. Klinische Details wie Alter, Geschlecht und Krankengeschichte werden mathematisch mit den EEG‑Merkmalen mittels kanonischer Korrelationsanalyse in Einklang gebracht. Diese Fusion erzeugt einen gemeinsamen Raum, in dem subtile Verknüpfungen zwischen Gehirnaktivität und klinischem Kontext für einen Computer leichter zu erkennen sind.
Wie die KI aus Gehirnwellen lernt
Die verschmolzenen Daten werden anschließend von einem Deep‑Learning‑Modell analysiert, das speziell für zeitvariierende Hirnsignale entwickelt wurde. Die Architektur kombiniert Faltungs‑Schichten, die nach lokalen Mustern über Kanäle und Frequenzen suchen, mit rekurrenten Schichten, die verfolgen, wie sich diese Muster Sekunde für Sekunde entwickeln. Ein „Attention“‑Mechanismus gewichtet Zeitabschnitte höher, die besonders diagnostisch erscheinen – ähnlich wie ein Kliniker, der sich auf einen auffälligen Aktivitätsausbruch in einer Aufzeichnung fokussiert. Um nicht als Blackbox zu fungieren, enthält das System Erklärungsinstrumente wie Grad‑CAM und integrierte Gradienten. Diese liefern visuelle Karten und Scores, die hervorheben, welche Frequenzen, Zeitfenster und klinischen Variablen jede Vorhersage am stärksten beeinflusst haben. In Tests an zwei großen öffentlichen EEG‑Datenbanken erreichte das Framework etwa 94 % Genauigkeit, mit Sensitivitäten und Spezifitäten über 92 % und übertraf damit mehrere starke Vergleichsmethoden. 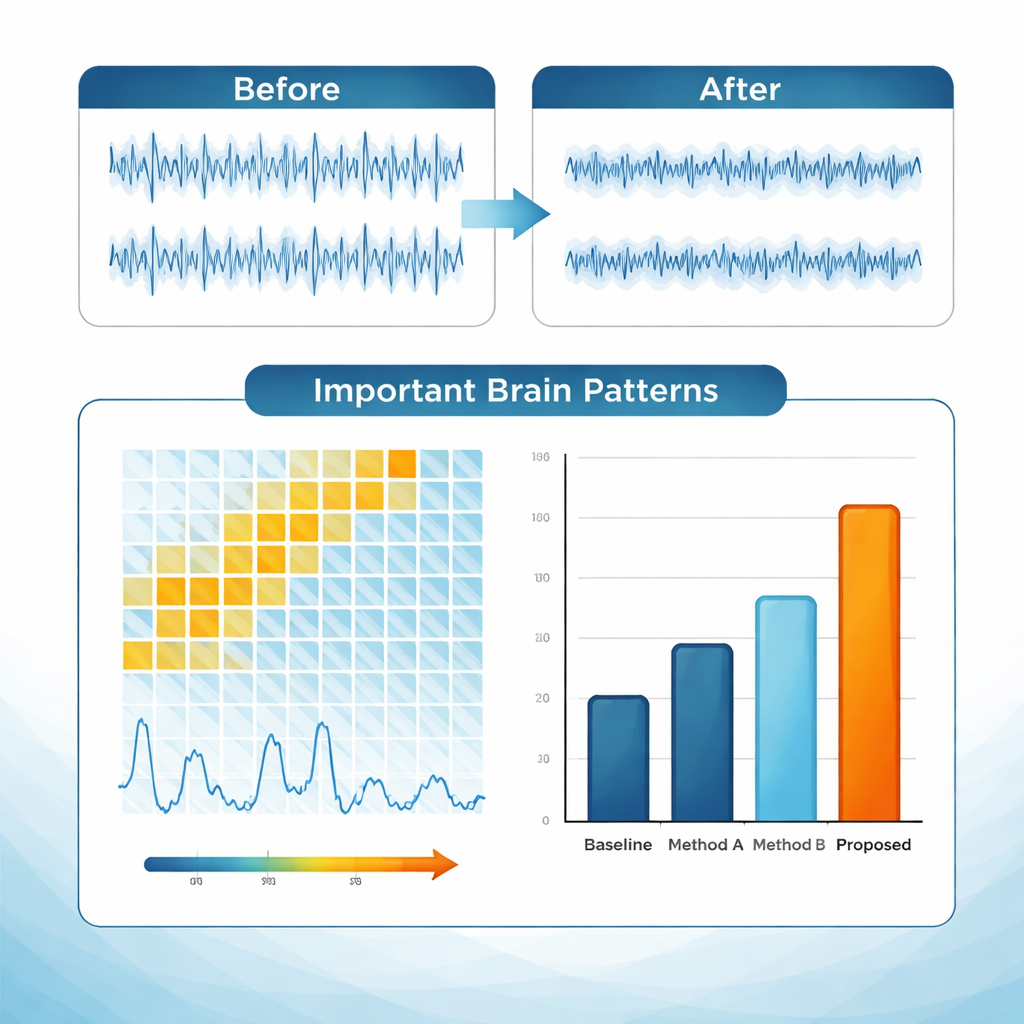
Was das für Patientinnen und Patienten bedeuten könnte
Für Laien ist die Quintessenz: Diese Arbeit zeigt, wie ein sorgfältig gestuftes, erklärbares KI‑System komplizierte, verrauschte EEG‑Aufnahmen in klare, klinisch verwertbare Erkenntnisse verwandeln kann. Durch die bessere Nutzung schneller Gehirnrhythmen und deren Integration mit routinemäßigen Patientendaten erkennt das Framework frühe Anzeichen von Erkrankungen wie Alzheimer und Parkinson und zeigt den Ärzten zugleich, warum es zu seinen Schlussfolgerungen gelangt ist. Obwohl weitere Prüfungen an alltäglichen klinischen und tragbaren EEG‑Daten erforderlich sind, weist dieser Ansatz auf künftige Bettenrand‑ oder sogar heimische Werkzeuge hin, die neurologische Probleme früher melden, Behandlungsentscheidungen unterstützen und letztlich die Lebensqualität von Millionen Menschen mit erhöhtem Risiko neurodegenerativer Erkrankungen verbessern könnten.
Zitation: Agrawal, R., Dhule, C., Shukla, G. et al. Iterative multiblock framework for high frequency EEG based neurological disorder detection. Sci Rep 16, 5995 (2026). https://doi.org/10.1038/s41598-026-37126-5
Schlüsselwörter: EEG, neurologische Störungen, Alzheimer‑Krankheit, Parkinson‑Krankheit, Gehirnwellen