Clear Sky Science · de
Vergleichende Analyse überwachten Lernens und Ensemble-Modellen mit unüberwachter Exploration zur Vorhersage der Alzheimer-Krankheit
Warum Frühwarnung wichtig ist
Die Alzheimer-Krankheit raubt Menschen schleichend Erinnerung und Unabhängigkeit, oft lange bevor eine eindeutige Diagnose gestellt wird. Familien, Ärztinnen und Ärzte sowie Gesundheitssysteme profitieren davon, wenn Warnzeichen früh erkannt werden, denn nur dann können Behandlung, Planung und Unterstützung den größten Unterschied machen. Diese Studie stellt eine pragmatische Frage: Können sorgfältig gestaltete Computerprogramme, trainiert mit routinemäßigen klinischen Daten und Hirnscans, Demenz zuverlässiger erkennen als die heute üblichen Werkzeuge — und zugleich verborgene Muster in der Krankheitsentwicklung offenlegen?
Patientendaten in nutzbare Signale verwandeln
Die Forschenden nutzten eine bekannte Datensammlung namens OASIS-2, die 150 ältere Erwachsene im Alter von 60 bis 96 Jahren über mehrere Jahre begleitet. Für jeden Besuch enthält der Datensatz Basisinformationen wie Alter, Bildungsjahre und sozioökonomischen Status sowie kognitive Testergebnisse und aus MRT-Aufnahmen abgeleitete Messwerte, etwa das Gesamtvolumen des Gehirns. Bevor Vorhersagen möglich waren, bereinigte das Team die Daten, entfernte Identifikatoren und zweifelhafte Fälle, füllte eine kleine Anzahl fehlender Werte auf und normierte alle numerischen Messgrößen auf eine gemeinsame Skala. Sie gingen außerdem ein zentrales reales Problem an: Im Datensatz waren deutlich mehr gesunde als demente Personen vertreten. Damit die Modelle nicht einfach meist „keine Demenz“ vorhersagen, verwendeten die Forschenden Gewichtungsschemata, die Fehler bei der kleineren, dementen Gruppe während des Trainings stärker gewichten.
Klassische Werkzeuge gegen Modell-Teams vergleichen
Mit diesem aufbereiteten Datensatz verglichen die Autoren vertraute Methoden des maschinellen Lernens mit fortgeschritteneren „Ensembles“, die mehrere Modelle zu einem stärkeren Prädiktor kombinieren. Zur klassischen Gruppe gehörten logistische Regression, Entscheidungsbäume, Support-Vektor-Maschinen und Random Forests. Die Ensemble-Gruppe umfasste AdaBoost, XGBoost und ein Mehrheitswahl-Modell, das drei abgestimmte Klassifizierer kombinierte. Alle Modelle wurden an einem Teil der Daten trainiert und an zurückgehaltenen Fällen getestet; die Leistung wurde anhand von Genauigkeit, der Fähigkeit, demente Personen korrekt zu identifizieren (Recall), und der Fläche unter der ROC-Kurve beurteilt — einer Zusammenfassung, wie gut das Modell gesunde von kranken Fällen trennt. 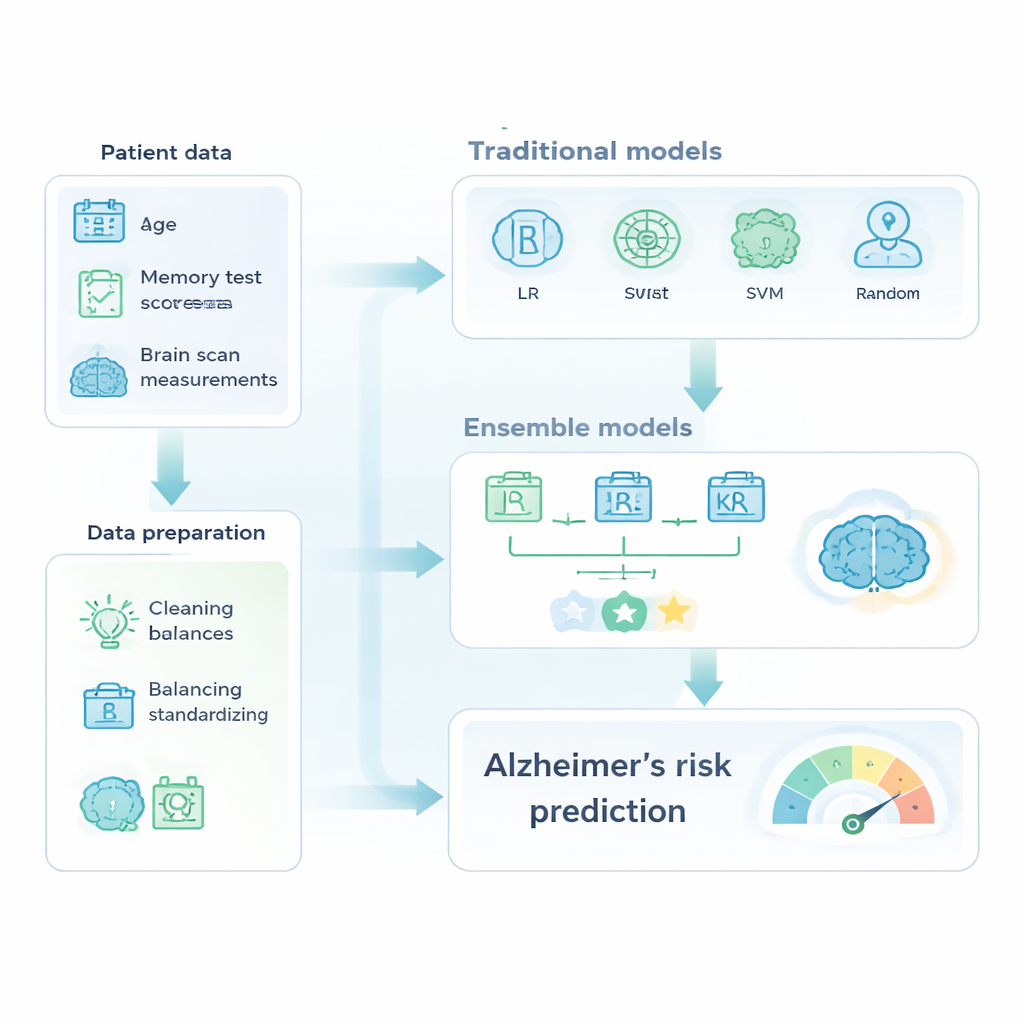
Wenn viele Modelle einen einzelnen schlagen
Die direkte Gegenüberstellung war eindeutig. Während die besten traditionellen Methoden ordentlich abschnitten, erreichten sie ein Plateau nahe den in früheren Studien berichteten Werten, mit Testgenauigkeiten im unteren bis mittleren 80-Prozent-Bereich. Im Gegensatz dazu erzielte das Mehrheitswahl-Ensemble etwa 95 Prozent Genauigkeit und einen ähnlich hohen ROC-Wert und übertraf damit die häufig zitierte Marke von 92 Prozent. Auch AdaBoost und andere Ensemble-Modelle schnitten besser ab als jedes einzelne traditionelle Modell. Dieser Vorteil entsteht, weil unterschiedliche Algorithmen verschiedene Aspekte der Daten erfassen; indem man sie „abstimmen“ lässt, glättet das Ensemble individuelle Eigenheiten und Überanpassungen und führt zu stabileren Vorhersagen. Der Preis für diesen Gewinn ist geringere Transparenz: Es ist schwieriger, auf einen Blick nachzuvollziehen, warum ein Ensemble eine bestimmte Entscheidung getroffen hat, verglichen mit einer einfachen Regression oder einem einzelnen Baum. 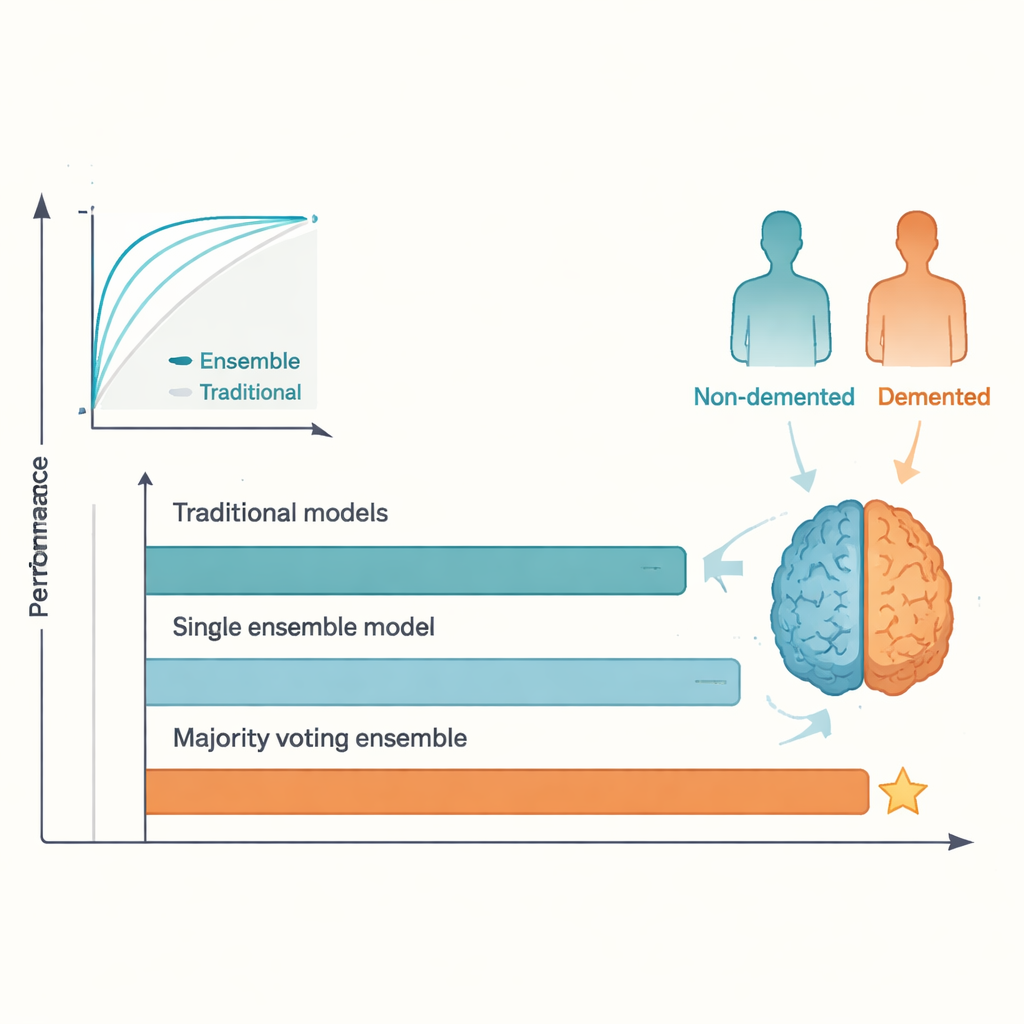
Suche nach natürlichen Gruppierungen in den Daten
Neben der Frage, wer Demenz hat, untersuchten die Forschenden auch, wie sich Patientinnen und Patienten natürlicherweise gruppieren, unabhängig von Diagnoseetiketten. Dafür wandelten sie alle kontinuierlichen Variablen in geordnete Kategorien um — etwa Alters- oder Gehirnvolumenbereiche — und wendeten eine Technik namens Multiple Korrespondenzanalyse an, um diese reichhaltigen Informationen auf einige zugrundeliegende Dimensionen zu komprimieren. Anschließend nutzten sie k-Means-Clustering, um die Punkte in eine kleine Anzahl kohärenter Gruppen zu partitionieren. Einige Cluster waren von Menschen mit erhaltenem Gehirnvolumen und normalen kognitiven Werten dominiert, andere enthielten Personen mit geringem Gehirnvolumen, schlechten Testergebnissen und schwereren Demenzbewertungen. Die Tatsache, dass sich diese unüberwachten Cluster gut mit dem klinischen Status deckten, legt nahe, dass die Daten ein starkes, konsistentes Signal über Krankheitsrisiko und -verlauf enthalten.
Was das für Patientinnen, Patienten und Kliniker bedeutet
Für Laien ist das Fazit klar: Sorgfältig konzipierte Modell-Teams des maschinellen Lernens können Alzheimer-assoziierte Demenz in strukturierten klinischen Daten genauer erkennen als ältere Methoden, und zwar mit Informationen, die viele Kliniken bereits erheben. Gleichzeitig zeigen explorative Techniken, dass Menschen in unterschiedliche Profile der Gehirngesundheit und kognitiven Leistungsfähigkeit fallen, was auf verschiedene Verläufe der Erkrankung hindeutet. Obwohl die Studie durch ihre überschaubare Stichprobengröße und die Komplexität der Interpretation von Ensemble-Modellen limitiert ist, zeigt sie, dass die Kombination aus leistungsfähiger Vorhersage und sorgfältiger explorativer Analyse sowohl die Früherkennung schärfen als auch unser Verständnis dafür vertiefen kann, wie Alzheimer Fuß fasst.
Zitation: Amr, Y., Gad, W., Leiva, V. et al. Comparative analysis of supervised and ensemble models with unsupervised exploration for alzheimer’s disease prediction. Sci Rep 16, 7322 (2026). https://doi.org/10.1038/s41598-026-37122-9
Schlüsselwörter: Alzheimer-Krankheit, Demenzvorhersage, maschinelles Lernen, Ensemble-Modelle, Gehirnbildgebung