Clear Sky Science · de
PERK/ATF4/LAMP3-Achse trägt zum aggressiven Phänotyp von hepatozellulären Karzinomzellen als Reaktion auf chronische Ethanolbelastung bei
Wie Alkohol Leberkrebs gefährlicher machen kann
Viele Menschen wissen, dass starker Alkoholkonsum die Leber schädigen kann, doch weniger ist bekannt darüber, wie Alkohol das Verhalten von Leberkrebs verändern kann. Diese Studie untersucht, was in Leberkrebszellen passiert, wenn sie über längere Zeit Alkohol ausgesetzt sind. Die Forschenden decken einen bislang wenig beachteten Stressweg in den Zellen auf, der Tumoren invasiver, widerstandsfähiger gegen Zelltod und rückfallanfälliger macht — und zeigen, dass das Blockieren dieses Weges im Labor diese Aggressivität abschwächen kann.
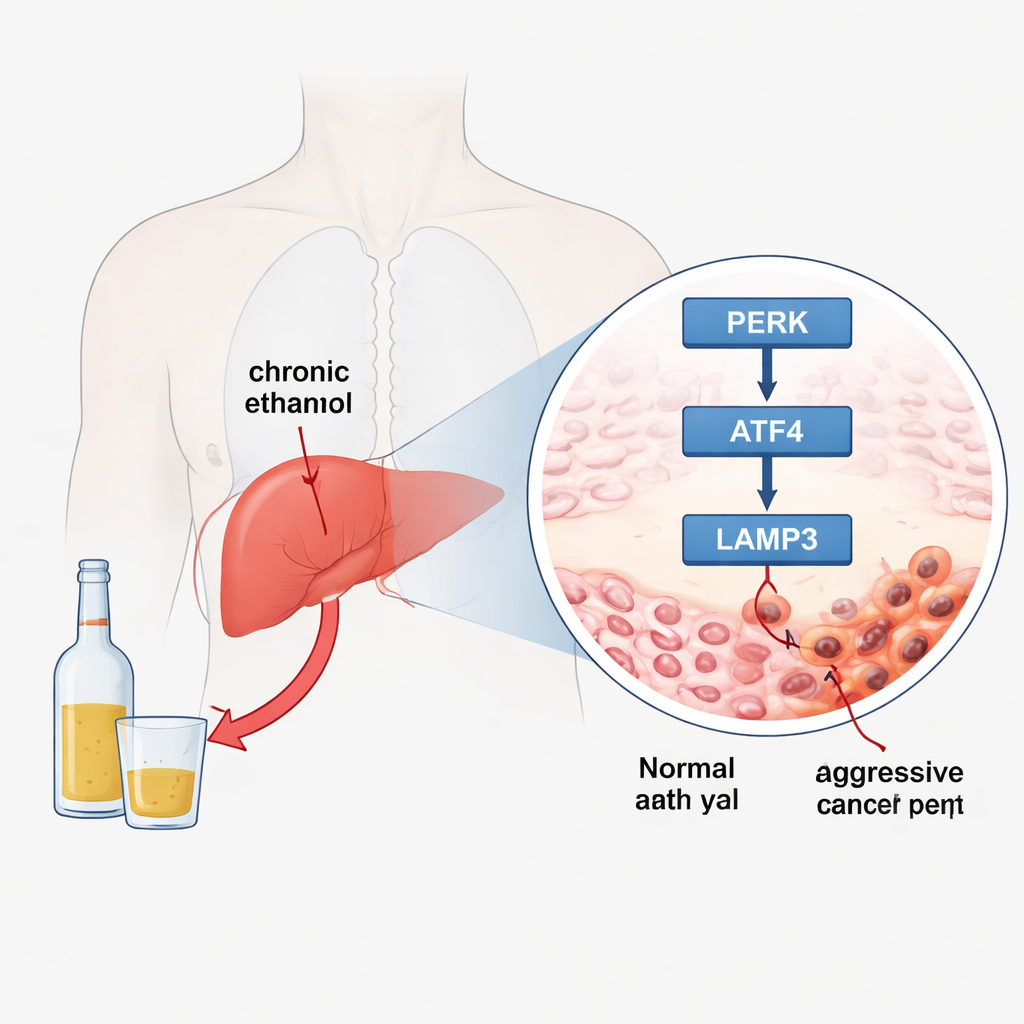
Ein genauerer Blick auf alkoholbedingten Leberkrebs
Leberkrebs, insbesondere das hepatozelluläre Karzinom, gehört weltweit zu den häufigsten und tödlichsten Krebserkrankungen. Während Infektionen wie Hepatitis B und C als Ursachen intensiv untersucht wurden, sind Krebserkrankungen, die mit langfristigem Alkoholkonsum zusammenhängen, weniger gut verstanden. Menschen mit starkem Alkoholkonsum erfahren anhaltende Schädigungen ihrer Leberzellen, die wiederholt unter Stress geraten, weil sie Alkohol und dessen toxische Abbauprodukte verarbeiten müssen. Die Autorinnen und Autoren wollten wissen, ob dieser andauernde Stress bestimmte molekulare Schalter umlegt, die alkoholassoziierte Lebertumoren in einen aggressiveren Zustand drängen als Tumoren, die durch andere Ursachen entstehen.
Zellulärer Stress: Wenn die Proteinfabrik versagt
Im Inneren jeder Zelle fungiert das endoplasmatische Retikulum wie eine Werkstatt zum Falten von Proteinen. Wird diese Werkstatt überlastet, schaltet sich ein eingebautes Alarmsystem, die sogenannte ungefaltete Proteinantwort, ein. Ein Zweig dieses Alarms, die PERK–ATF4–LAMP3-Achse, kann Zellen entweder helfen, Stress zu überstehen, oder, wenn der Stress zu groß wird, sie zum Selbstmord treiben. Die Forschenden setzten drei humanen Leberkarzinomzelllinien über mehrere Tage unterschiedlichen Ethanolmengen aus, um chronischen Alkoholkonsum nachzuahmen. In zwei dieser Modelle beobachteten sie eine starke Aktivierung der PERK–ATF4–LAMP3-Achse sowie eine Zunahme von Faktoren, die mit Entzündung (NF‑κB), Neubildung von Blutgefäßen (VEGF‑A) und Fett‑ und Cholesterinproduktion (über SREBP‑Gene) assoziiert sind. Gleichzeitig akkumulierten die Zellen vermehrt Triglyceride und Cholesterin, was den Fettleberveränderungen ähnelt, die bei starken Trinkern häufig vorkommen.
Von ruhenden Zellen zu „beweglichen“ Tumoren
Die Aktivierung dieses Stresswegs veränderte nicht nur Genprofile — sie veränderte das Verhalten der Krebszellen. Unter chronischer Ethanolbelastung wurden Leberkrebszellen deutlich besser darin, sich zu bewegen und Barrieren in Labortests zu durchdringen, Eigenschaften, die im Körper einer Metastasierung entsprechen. Sie bildeten zudem deutlich mehr Sphären in speziellen Kulturen mit geringer Haftung, ein Hinweis auf erhöhte „Stemness“, also einen größeren Pool robuster, rückfallgefährdeter Krebszellen. Zugleich unterliefen weniger Zellen den programmierten Zelltod, sodass beschädigte und potenziell gefährliche Zellen überlebten. Die Zellen erzeugten mehr reaktive Sauerstoffspezies — chemisch reaktive Moleküle, die DNA und Proteine weiter schädigen können — und schufen so einen Teufelskreis aus Stress und Überleben, der das Tumorwachstum begünstigt.
Den Stresszweig ausschalten, um den Tumor zu zähmen
Das Team testete anschließend, ob das Abschalten der PERK-Achse diese alkoholbedingten Veränderungen umkehren kann. Sie behandelten ethanol-exponierte Leberkrebszellen mit einem oral verfügbaren PERK-Inhibitor namens GSK2606414. Dieses Medikament reduzierte die Aktivierung wichtiger nachgeschalteter Akteure (ATF4 und LAMP3), verringerte den oxidativen Stress und senkte die Expression vieler Gene, die mit Tumorwachstum und Entzündung verknüpft sind. Funktionell wurden die Krebszellen weniger invasiv und beweglich, und ihre Fähigkeit, krebsstammzellähnliche Sphären zu bilden, brach zusammen — unter PERK-Blockade bildeten sich gar keine Sphären. Wichtig ist, dass die Inhibition auch die Apoptose wiederherstellte, sodass mehr beschädigte Zellen eliminiert wurden, statt zu verweilen. Normale, unbehandelte Zellen, die nur dem Inhibitor ausgesetzt waren, zeigten keine größeren schädlichen Veränderungen, was darauf hindeutet, dass dieser Ansatz vornehmlich stressgeprimierte, alkoholexponierte Tumorzellen trifft.
Was das für Menschen mit starkem Alkoholkonsum bedeuten könnte
Für Nicht‑Spezialistinnen und -Spezialisten lautet die Kernbotschaft: Langfristige Alkoholexposition bewirkt mehr, als nur das Risiko für Leberkrebs zu erhöhen — sie kann bestehende Lebertumoren durch Aktivierung eines spezifischen Stresswegs in eine härtere, schwerer zu behandelnde Form einprogrammieren. Diese in Zelllinien durchgeführte Studie zeigt, dass das Blockieren der PERK–ATF4–LAMP3-Achse dieses aggressive Verhalten abschwächen und den Zelltod wieder ermöglichen kann. Während diese Befunde noch in Tiermodellen und schließlich in Studien am Menschen bestätigt werden müssen, weisen sie auf neue medikamentöse Strategien hin, die besonders für Menschen mit alkoholassoziiertem Leberkrebs nützlich sein könnten und die Bemühungen ergänzen, den Alkoholkonsum zu reduzieren oder einzustellen und die allgemeine Lebergesundheit zu verbessern.
Zitation: Goyal, H., Kaur, J. PERK/ATF4/LAMP3-arm contributes to the aggressive phenotype of hepatocellular carcinoma cells in response to the chronic ethanol exposure. Sci Rep 16, 6188 (2026). https://doi.org/10.1038/s41598-026-37114-9
Schlüsselwörter: alkoholassoziierter Leberkrebs, zelluläre Stresswege, PERK-Signalweg, Tumoraggressivität, Leberkrebstherapie