Clear Sky Science · de
Seneszenz-assoziierte LncRNAs TRMP und TRMP-S fördern Magenkrebs durch Aktivierung von IGFL4
Warum diese Forschung wichtig ist
Magenkrebs gehört nach wie vor zu den tödlichsten Krebsarten weltweit, vor allem weil er häufig spät entdeckt wird und schwer zu behandeln sein kann. Diese Studie zeigt, wie zwei bislang wenig untersuchte genetische Moleküle, TRMP und TRMP-S, das Wachstum und die Ausbreitung von Magen-Tumoren fördern. Indem sie die Abfolge von Ereignissen offenlegt, die diese LncRNAs in Krebszellen und in der Immunumgebung des Tumors auslösen, weist die Arbeit auf neue Möglichkeiten hin, Patienten früher zu diagnostizieren und gezieltere, wirksamere Therapien zu entwickeln.
Verborgene Signale in unserer DNA
Die meisten Menschen denken bei Genen an Baupläne für Proteine, doch unsere DNA produziert auch lange nichtkodierende RNAs (LncRNAs), die keine Proteine bilden, aber das Zellverhalten stark beeinflussen können. TRMP und seine kürzere Spleiß-Variante TRMP-S sind solche LncRNAs. Zuvor wurden sie mit Alterungsprozessen und der Kontrolle des Zellzyklus in Lungen- und Darmzellen in Verbindung gebracht, ihre Rolle beim Magenkrebs war jedoch unbekannt. Da LncRNAs als Diagnosemarker und Therapieziele dienen können, untersuchten die Autorinnen und Autoren, ob TRMP und TRMP-S Magenepithelzellen in Richtung Krebs treiben und wie sie mit anderen Molekülen interagieren könnten.
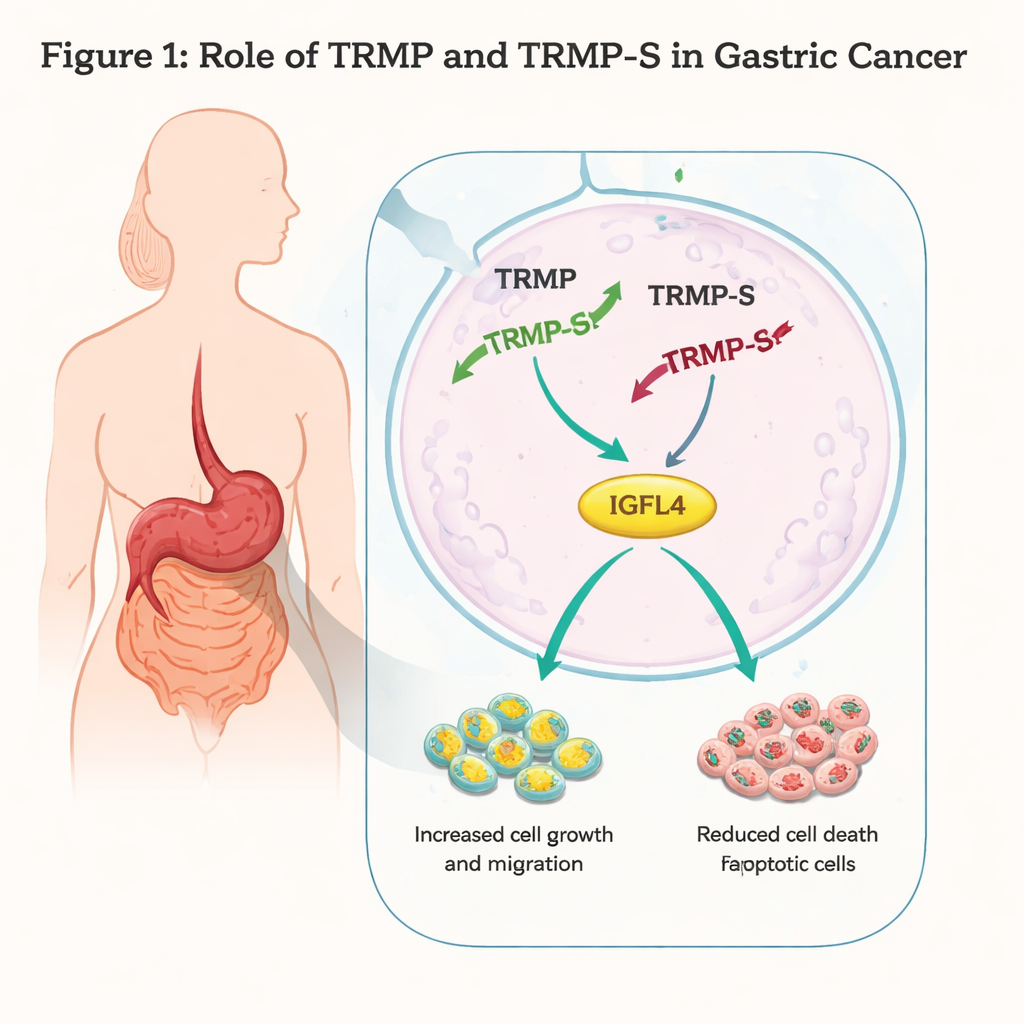
Ein Krebsgasfuß vom Netz nehmen
Die Forschenden arbeiteten mit zwei humanen Magenkrebszelllinien, AGS und MKN45, und setzten genetische Werkzeuge ein, um die Mengen von TRMP-S und TRMP zu reduzieren. Bei Stilllegung von TRMP-S wuchsen die Krebszellen langsamer, bildeten weniger Kolonien und waren weniger in der Lage, künstliche Barrieren zu überwinden oder Wunden in einer Zellkultur zu schließen. Durchflusszytometrie und Proteinanalysen zeigten, dass mehr Zellen programmierter Zelltod (Apoptose) durchliefen und der Zellzyklus in der G1-Phase blockiert wurde, einem wichtigen Kontrollpunkt vor der DNA-Replikation. Die Spiegel von p73, einem Mitglied der Tumorsuppressor-Familie p53, stiegen bei Verlust von TRMP-S an, was mit stärkerer Zellzykluskontrolle und vermehrtem Zelltod übereinstimmt. Zusammen deuten diese Ergebnisse darauf hin, dass TRMP-S normalerweise wie ein Gaspedal für Magenkrebszellen wirkt.
Ein wichtiger Partner: das IGFL4-Signal
Um zu verstehen, wie TRMP und TRMP-S ihre Effekte ausüben, wertete das Team umfangreiche Patientendatensätze aus dem Cancer Genome Atlas und einer koreanischen Magenkrebs-Kohorte aus. Sie suchten nach Genen, die sowohl in Tumoren übermäßig hoch exprimiert waren als auch positiv mit TRMP-Leveln korrelierten, und erstellten ein Sechsgene-Risikomodell, das das Überleben der Patienten vorhersagte — höhere Werte standen mit schlechteren Ergebnissen in Verbindung. Unter diesen Genen stach eines hervor: IGFL4, ein Familienmitglied, das mit insulinähnlichen Wachstumsfaktoren verwandt ist, welche bekanntlich in vielen Krebsarten Wachstum und Überleben fördern. In Magenkrebszellen führte das Herunterregulieren von TRMP-S zu deutlich geringeren RNA- und Proteinspiegeln von IGFL4, während ein RNA-Immunpräzipitations-Assay zeigte, dass sowohl TRMP als auch TRMP-S physisch an das IGFL4-Protein binden. Direkte Reduktion von TRMP hatte denselben dämpfenden Effekt auf IGFL4, was darauf hindeutet, dass diese LncRNAs helfen, dieses wachstumsfördernde Signal zu stabilisieren oder dessen Produktion zu unterstützen.
Ausbreitung verlangsamen und das Immunsystem umgestalten
Als die Forschenden IGFL4 selbst mit kleinen interferierenden RNAs stilllegten, wuchsen Magenkrebszellen langsamer, migrierten weniger und zeigten eine geringere Fähigkeit, Membranen zu durchdringen und Wunden zu schließen. Die Analyse von Patiententumordaten ergab, dass IGFL4 in Magen-Tumoren deutlich höher exprimiert war als im normalen Magengewebe und ebenfalls in vielen anderen Krebsarten erhöht vorkam. Wichtig ist, dass Tumoren mit hoher IGFL4-Expression charakteristische Muster der Immunzellinfiltration zeigten: mehr undifferenzierte Makrophagen (M0) und weniger Plasmazellen, Monozyten, Eosinophile und Neutrophile. Computergestützte Immun‑Scores deuten darauf hin, dass Tumoren mit hohem IGFL4 besser auf moderne Immuntherapien, die Immun-Checkpoints blockieren, ansprechen könnten, weshalb IGFL4 helfen könnte, Patientinnen und Patienten zu identifizieren, die gute Kandidaten für diese Behandlungen sind.
Eine kleine RNA, die dagegenhält
Die Studie enthüllte auch ein Gegengewicht zu diesem krebsfördernden Signalweg. Durch Korrelation von microRNA- und Genexpression in Patientendaten identifizierten die Autorinnen und Autoren miR-129-5p als eine kleine RNA, die negativ mit TRMP und IGFL4 verbunden ist. In Magenkrebszellen reduzierte die Zugabe von miR-129-5p die IGFL4-Spiegel und verlangsamte das Wachstum, während das Blockieren von miR-129-5p IGFL4 erhöhte und die Proliferation beschleunigte. Eine weitere Kandidaten-microRNA, miR-4739, beeinflusste IGFL4 nicht messbar und wurde ausgeschlossen. Diese Ergebnisse stützen eine Regulationskette, in der TRMP und TRMP-S, miR-129-5p und IGFL4 ein Netzwerk bilden, das fein steuert, wie aggressiv Magenkrebszellen wachsen und wie sie mit ihrer Umgebung interagieren.
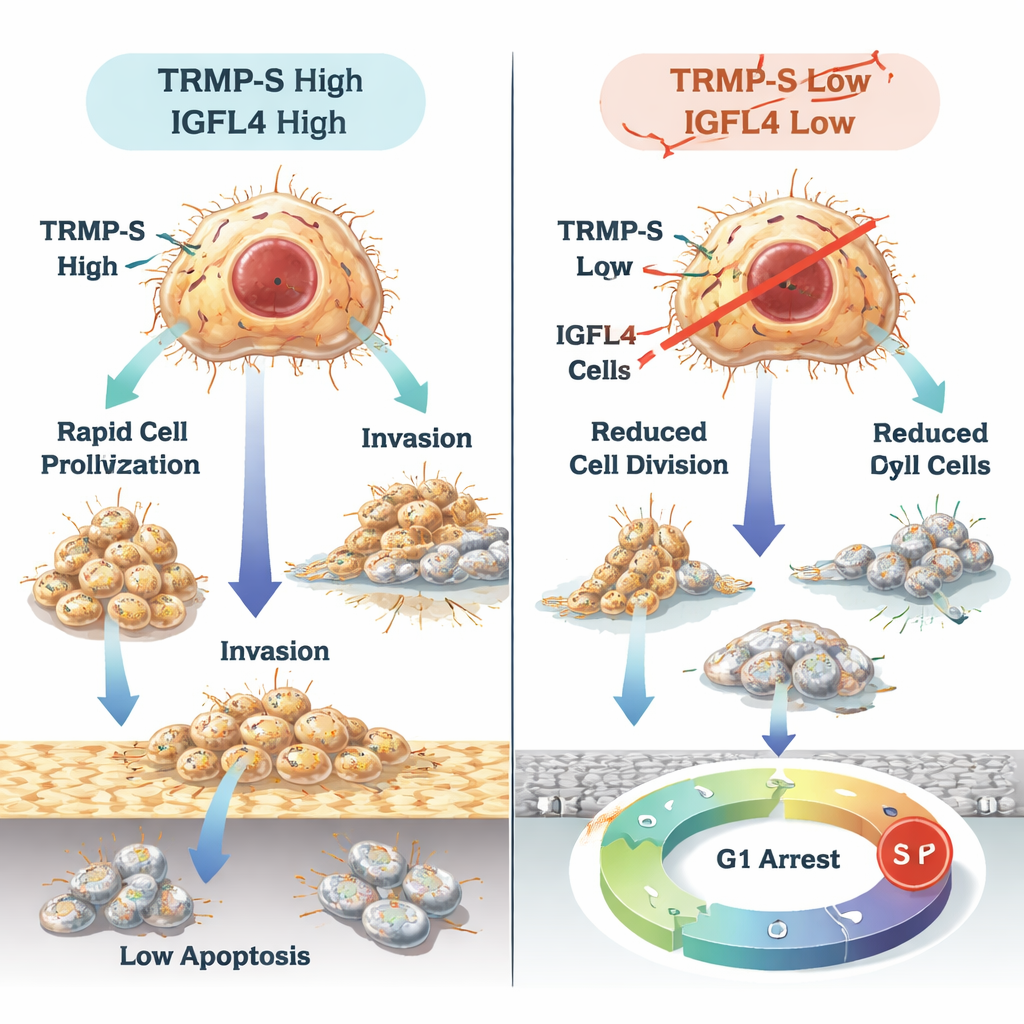
Was das für Patientinnen und Patienten bedeuten könnte
Einfach gesagt zeigt diese Arbeit, dass TRMP und TRMP-S als unsichtbare Regisseure wirken, die IGFL4 einschalten und Magenkrebszellen helfen, zu wachsen, sich auszubreiten und natürliche Bremsmechanismen zu umgehen. Gleichzeitig wirkt die kleine RNA miR-129-5p als Bremse auf IGFL4, und IGFL4 selbst prägt, wie Immunzellen Tumoren umgeben und wie gut Therapien funktionieren, die das Immunsystem aktivieren. Obwohl weitere Forschung und klinische Prüfungen nötig sind, stellen TRMP, TRMP-S, IGFL4 und miR-129-5p zusammen vielversprechende Marker für Prognoseabschätzungen und potenzielle neue Zielstrukturen für Medikamente dar, die darauf abzielen, Magenkrebs zu verlangsamen oder zu stoppen.
Zitation: Zhang, M., Mi, Y., Li, F. et al. Senescence-associated LncRNAs TRMP and TRMP-S promote gastric cancer by activating IGFL4. Sci Rep 16, 6740 (2026). https://doi.org/10.1038/s41598-026-37106-9
Schlüsselwörter: Magenkrebs, lange nichtkodierende RNA, TRMP, IGFL4, Tumormikroumgebung