Clear Sky Science · de
Identifizierung von RBX1 als Regulator der LIPT1-Transkription und seine Rolle beim kupferinduzierten Zelltod in GBM-Zellen
Warum Kupfer und Hirntumoren wichtig sind
Glioblastoma multiforme ist eine der tödlichsten Formen von Hirnkrebs, wobei die meisten Patientinnen und Patienten trotz aggressiver Operationen, Bestrahlung und Chemotherapie nur kurz nach der Diagnose überleben. Diese Studie untersucht einen unerwarteten Verbündeten gegen diese Tumoren: das Metall Kupfer. Die Forschenden analysieren eine neu erkannte Form des Zelltods, die durch Kupfer ausgelöst wird, und identifizieren einen molekularen Weg, der Ärzten helfen könnte, diesen Prozess zu nutzen, um Tumore zu schwächen und möglicherweise die Immunantwort gegen Krebszellen zu verstärken.
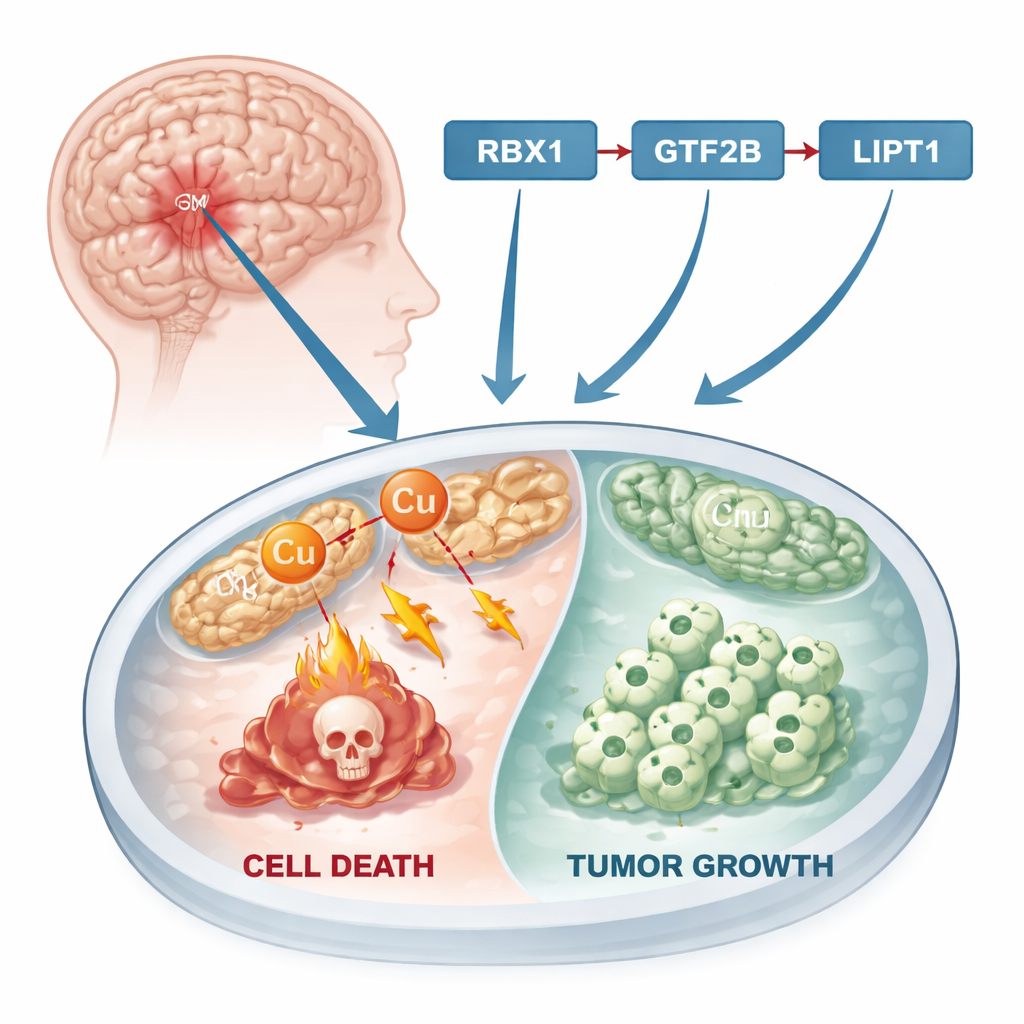
Ein neuer Weg, wie Zellen sterben
Jahrzehntelang lag der Fokus der Krebsforschung auf bekannten Formen des Zelltods wie der Apoptose, bei der beschädigte Zellen sich geordnet abschalten. Kürzlich entdeckten Wissenschaftlerinnen und Wissenschaftler jedoch einen anderen Weg, den man als kupferinduzierten Zelltod oder „Cuproptose“ bezeichnet. Bei diesem Prozess reichert sich überschüssiges Kupfer in den Kraftwerken der Zelle, den Mitochondrien, an. Dort stört es zentrale Proteine, führt zur Bildung toxischer Aggregate und tötet schließlich die Zelle. Da viele Tumore einen veränderten Metallstoffwechsel und höhere Kupferwerte als normales Gewebe aufweisen, bietet die Cuproptose einen potenziellen Angriffspunkt: Wenn Forschende Tumorzellen gezielt in diese kupfergetriebene Richtung drängen können, ließe sich das Krebswachstum möglicherweise bremsen oder stoppen.
Fokussierung auf ein Schlüsselgen beim Glioblastom
Die Autorinnen und Autoren begannen mit einer Bestandsaufnahme von Genen, die bereits mit Cuproptose in Verbindung gebracht wurden, und untersuchten ihr Verhalten in Glioblastom-Proben im Vergleich zu normalem Hirngewebe. Ein Gen stach besonders hervor: LIPT1. Es war in Glioblastomgewebe und in mehreren Glioblastomzelllinien stärker aktiv als in normalen Gehirnzellen. Wichtig ist, dass Patientinnen und Patienten, deren Tumoren eine höhere LIPT1-Aktivität zeigten, tendenziell längere rezidivfreie Intervalle nach der Behandlung hatten. Hohe LIPT1-Werte standen außerdem mit einer größeren Präsenz von CD8-T-Zellen in Zusammenhang, den immunologischen Frontkämpfern gegen Krebs, was darauf hindeutet, dass dieses Gen das Tumorumfeld gegenüber einer Immunantwort anfälliger machen könnte.
Was passiert, wenn der kupfergetriebene Todesmechanismus gedämpft wird
Um zu prüfen, ob LIPT1 tatsächlich die Empfindlichkeit gegenüber kupferinduziertem Zelltod beeinflusst, setzte das Team Glioblastomzellen einem kupferbindenden Medikamentenkombinat aus, das zuverlässig Cuproptose auslöst. Anschließend nutzten sie genetische Werkzeuge, um die LIPT1-Spiegel zu senken. Wurde LIPT1 unterdrückt, zeigten die Tumorzellen eine erhöhte Resistenz gegen kupferinduzierte Abtötung, überlebten besser und wiesen stärkere Wanderungs- und Invasionsfähigkeiten auf — Merkmale, die mit aggressiverem Krebsverhalten verbunden sind. In gemischten Kulturen aus Tumorzellen und menschlichen CD8-T-Zellen reduzierte eine Absenkung von LIPT1 außerdem die Freisetzung immunologischer Botenstoffe und machte die Krebszellen für T-Zellen schwerer zu zerstören. Zusammengenommen deuten diese Experimente darauf hin, dass LIPT1 die Sensitivität gegenüber kupferinduziertem Zelltod erhöht und antitumorale Immunaktivität unterstützt.
Der Weg nach oben bis zu RBX1
Die nächste Fragestellung war, warum LIPT1 im Glioblastom hochreguliert ist. Durch die Kombination mehrerer großer Gen- und Proteindatenbanken identifizierten die Forschenden einen Transkriptionsfaktor — eine Art Hauptschalter für Genaktivität — namens GTF2B, der in der Nähe des LIPT1-Gens bindet und dessen Expression vermutlich steigert. Sie fragten dann, was GTF2B selbst reguliert. Ein zweites Protein, RBX1, erschien als starker Kandidat. RBX1 ist Teil des zellulären Systems zum Markieren und Entsorgen, das andere Proteine für den Abbau kennzeichnet. In Glioblastomzellen waren RBX1-Spiegel niedriger als in normalem Hirngewebe, während GTF2B und LIPT1 erhöht waren. Laborassays zeigten, dass RBX1 kleinen „Abbau mich“-Markern an GTF2B anbringen kann, die zu dessen Abbau führen; wurde RBX1 erhöht, sanken GTF2B-Spiegel und LIPT1-Aktivität, und das Blockieren der zellulären Abbaumaschinerie kehrte diesen Effekt um.
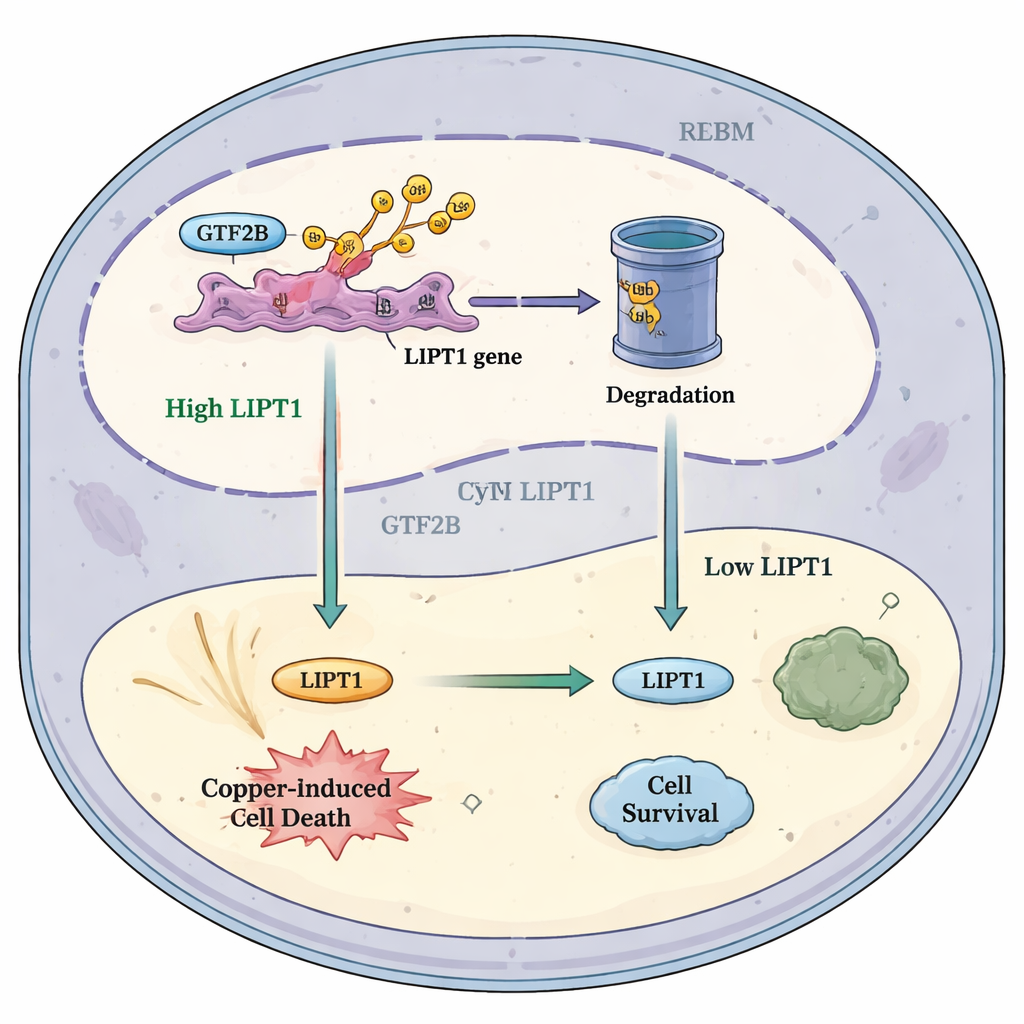
Wie dieser Signalweg künftigen Therapien nutzen könnte
Unter Einbeziehung dieser Befunde stellen die Autorinnen und Autoren ein schlichtes Modell vor: Unter gesunden Bedingungen hält RBX1 GTF2B in Schach und begrenzt dessen Aktivierung des LIPT1-Gens. Im Glioblastom führt ein reduziertes RBX1 zu weniger Abbau von GTF2B. Überschüssiges GTF2B steigert dann LIPT1, erhöht die Empfindlichkeit der Tumorzellen gegenüber kupferinduziertem Zelltod und zieht mehr krebsbekämpfende Immunzellen an. Dieses Modell legt nahe, dass eine gezielte Feinabstimmung des RBX1–GTF2B–LIPT1-Signalwegs, möglicherweise in Kombination mit kupferorientierten Wirkstoffen und Immuntherapien, das Gleichgewicht in Hirntumoren zugunsten der Selbstzerstörung verschieben könnte. Obwohl noch viel Arbeit nötig ist, bevor sich diese Idee klinisch umsetzen lässt, hebt die Studie eine vielversprechende Schnittstelle von Metallbiologie, Genregulation und Krebsimmunologie hervor, die neue therapeutische Wege für eine der hartnäckigsten Krebsarten eröffnen könnte.
Zitation: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Schlüsselwörter: Glioblastom, kupferinduzierter Zelltod, LIPT1, Tumorimmunologie, RBX1-Signalweg