Clear Sky Science · de
Integration von maschinellem Lernen und physikbasierten Modellen für das prädiktive Design von mit Gemcitabin beladenen Nanokompositen
Klügere Krebsmedikamente durch Design
Krebsmedikamente wie Gemcitabin können Leben retten, verhalten sich aber oft eher wie grobe Werkzeuge statt präzise Instrumente: Sie bauen sich schnell ab, verfehlen ihr Ziel und verursachen starke Nebenwirkungen. Diese Studie untersucht, wie Computer Forschenden helfen können, neue winzige Arzneiträger am Bildschirm „vorzutesten“ statt nur im Labor, um Gemcitabin-Behandlungen wirksamer, langlebiger und für Patientinnen und Patienten potenziell sicherer zu machen.
Warum winzige Träger wichtig sind
Konventionelle Chemotherapie überflutet den Körper mit Wirkstoffmolekülen, die überall zirkulieren und nicht nur im Tumor ankommen. Nanokomposite—künstlich hergestellte Partikel, tausendfach kleiner als ein Sandkorn—bieten eine Möglichkeit, Gemcitabin zu verpacken, sodass es im Blut geschützt ist und gezielter an Krebszellen abgegeben wird. Zwei Kennzahlen entscheiden weitgehend, ob ein Design nützlich ist. Die Beladungs-Effizienz (loading efficiency) sagt, wie viel Wirkstoff sich in jedem Partikel befindet, während die Einkapselungs-Effizienz (encapsulation efficiency) angibt, welcher Bruchteil des ursprünglich eingesetzten Wirkstoffs erfolgreich eingeschlossen und nicht verschwendet wurde. Hohe Werte beider Kennzahlen bedeuten weniger Injektionen, weniger Trägermaterial und eine bessere Chance, den Tumor stark zu treffen, ohne den Rest des Körpers zu überlasten.
Vom Trial-and-Error zum datengeleiteten Design
Diese Nanoträger von Hand zu entwickeln ist, als würde man ein Radio mit hunderten Reglern abstimmen—Partikelgröße, Oberflächenladung, Materialien, Beschichtungen und Herstellungsverfahren wirken alle auf komplexe Weise zusammen. Bisher veränderten Forschende meist ein oder zwei Parameter gleichzeitig und maßen das Ergebnis, ein langsamer und teurer Zyklus, der nur einen kleinen Ausschnitt des Gesamtbildes zeigt. In dieser Arbeit sammelten die Autorinnen und Autoren 59 sorgfältig geprüfte Gemcitabin-Nanocarrier-Rezepte aus der wissenschaftlichen Literatur und ergänzten sie um zusätzliche, physikbasierte Beispiele, die am Computer erzeugt wurden. Dieser kombinierte Datensatz ermöglichte es ihnen, mehrere Ansätze des maschinellen Lernens—Computerprogramme, die Muster aus Daten lernen—zu testen, um Beladungs- und Einkapselungseffizienzen allein aus den Designentscheidungen vorherzusagen.
Physik als Steuerung der Algorithmen
Die meisten Systeme des maschinellen Lernens sind mächtige Kurvenanpasser: Sie erkennen Muster, wissen aber nicht, wann eine Vorhersage gegen Naturgesetze verstößt. Um unrealistische Vorhersagen zu vermeiden, entwickelten die Forschenden eine hybride Methode, die Daten mit grundlegenden physikalischen Regeln darüber verbindet, wie Wirkstoffmoleküle sich bewegen, binden und in einem geschlossenen System ins Gleichgewicht kommen. In ihrem Rahmen wird jede Vorhersage, die zum Beispiel bedeuten würde, mehr Wirkstoff zu erzeugen als ursprünglich hinzugefügt wurde oder die Diffusion von Molekülen durch ein Material zu ignorieren, während des Trainings sanft bestraft. Dieser „physikinformierte“ Ansatz lenkt das Modell zu Antworten, die chemisch und physikalisch sinnvoll sind, besonders in Bereichen des Designraums, in denen reale Messungen knapp sind.
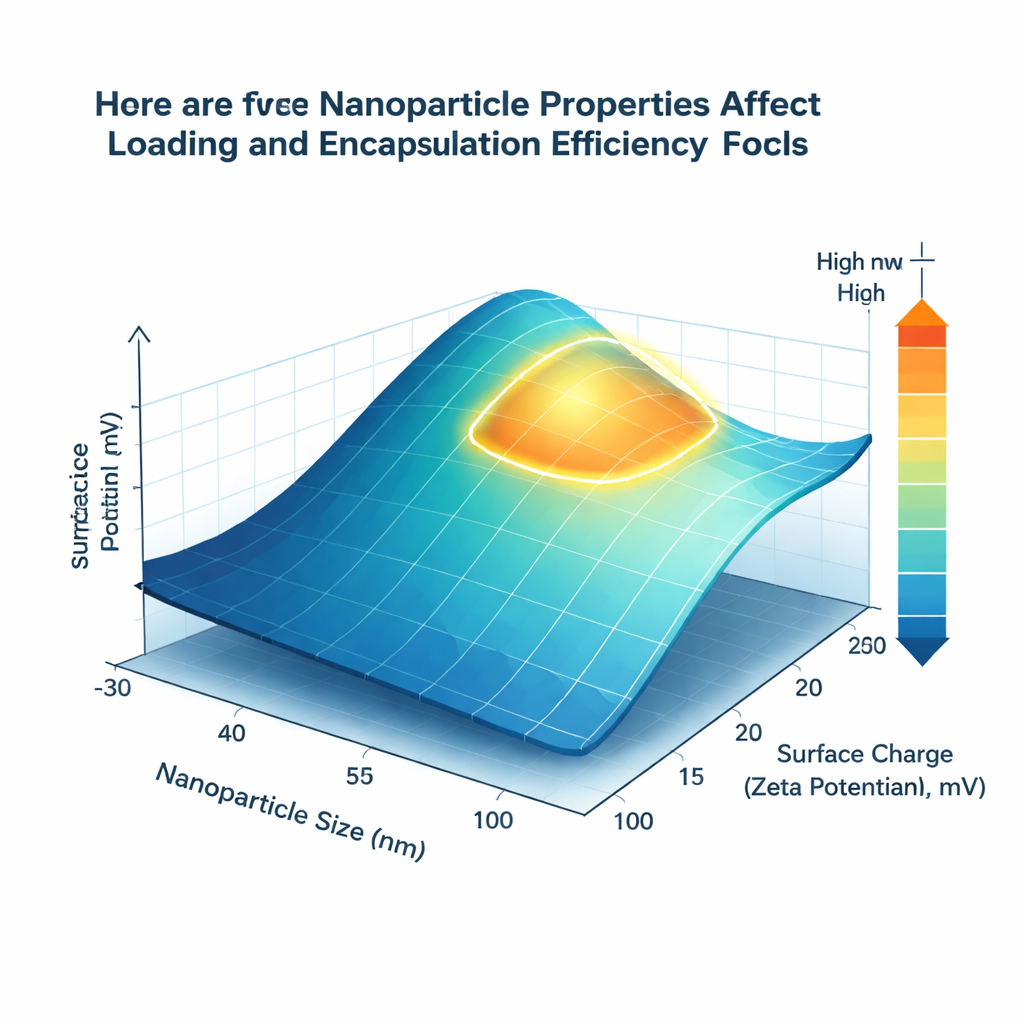
Was die Modelle herausfanden
Unter den getesteten Techniken lieferte ein fortgeschrittener Ensemble-Algorithmus namens XGBoost die genauesten Vorhersagen und stimmte gut mit berichteten experimentellen Ergebnissen für beide Schlüsselkennzahlen überein. Doch über die Genauigkeit hinaus wollte das Team verständliche Gestaltungsregeln. Mit einer Methode namens SHAP, die bewertet, wie stark jeder Faktor die Vorhersage nach oben oder unten treibt, fanden sie heraus, dass Partikelgröße und Oberflächenladung beständig die Leistung dominieren. Nanocarrier mit einem Durchmesser von etwa 80 bis 150 Nanometern boten die beste Balance zwischen Oberfläche und Innenvolumen und verbesserten sowohl Beladung als auch Einkapselung. Eine leicht positive Oberflächenladung im Bereich von etwa +15 bis +25 Millivolt stand in Zusammenhang mit besserer Bindung von Gemcitabin, wahrscheinlich weil die positiv geladenen Trägeroberflächen günstig mit den negativ geladenen Gruppen des Wirkstoffs interagieren.
Eine digitale Karte für künftige Krebstherapien
Das Endergebnis ist kein fertiges Medikament, sondern ein leistungsfähiges Planungswerkzeug. Die Studie liefert eine Art „Design-Karte“, die Forschende zu Nanocarrier-Rezepten leitet, die Gemcitabin wahrscheinlich gut aufnehmen und schützen, während Millionen wenig aussichtsreicher Kombinationen ausgeklammert werden. Die Autorinnen und Autoren betonen, dass ihre Vorhersagen noch durch neue Labor- und Tierversuche bestätigt werden müssen und dass ihr Datensatz—wenn auch sorgfältig zusammengestellt—in der Größe moderat ist. Trotzdem zeigt dieses physikbewusste maschinelle Lernframework, wie Computer helfen können, die Suche nach besseren Wirkstoffträgern für Krebs zu verkleinern, Kosten zu senken und den Weg von Ideen zu präziseren, patientenfreundlicheren Therapien zu beschleunigen.
Zitation: Rahdar, A., Fathi-karkan, S. & Shirzad, M. Integrating machine learning and physics-based modeling for predictive design of gemcitabine-loaded nanocomposites. Sci Rep 16, 6268 (2026). https://doi.org/10.1038/s41598-026-37098-6
Schlüsselwörter: Nanomedizin, Gemcitabin, Arzneistoffabgabe, Maschinelles Lernen, Nanopartikel