Clear Sky Science · de
Automatisierte Quantifizierung tumorinfiltrierender Lymphozyten mittels maschinellem Lernen enthüllt prognostische und immunogenomische Merkmale beim Lungenkrebs
Warum das Zählen winziger Immunzellen in Lungentumoren wichtig ist
Lungenkrebs gehört nach wie vor zu den tödlichsten Krebsarten, doch nicht alle Tumoren verhalten sich gleich. Manche werden stark von Immunzellen überwacht, die ins Tumorgewebe eindringen, andere bleiben nahezu unberührt. Diese tumorinfiltrierenden Lymphozyten, kurz TILs, geben Hinweise darauf, wie ein Patient voraussichtlich abschneiden wird und ob er von modernen Immuntherapien profitieren könnte. Das Problem ist: Bislang werden TILs meist mit bloßem Auge unter dem Mikroskop gezählt, was langsam und subjektiv ist. Die Studie stellt eine aktuelle Frage: Kann man maschinelles Lernen einsetzen, um diese Zellen auf routinemäßigen histologischen Schnitten automatisch zu messen, und was verrät das über die Biologie des Lungenkrebses und das Überleben der Patienten?
Aus normalen Schnitten digitale Karten erstellen
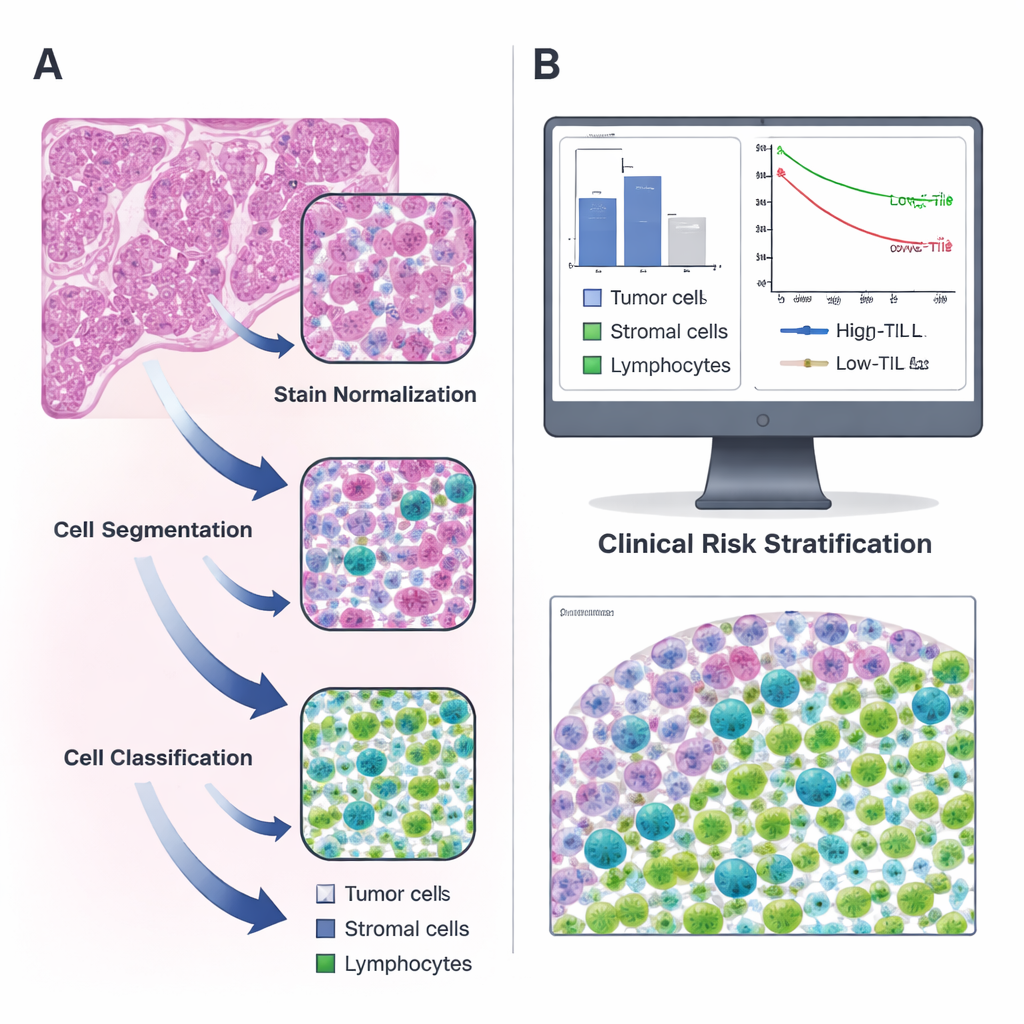
Die Forschenden konzentrierten sich auf das Lungenadenokarzinom, eine häufige Form von Lungenkrebs, und nutzten öffentliche Daten aus dem Cancer Genome Atlas sowie eine unabhängige Patientengruppe aus ihrem eigenen Krankenhaus. Für jeden Patienten analysierten sie routinemäßig mit Hämatoxylin‑ und Eosin‑(H&E) gefärbte Gewebeschnitte, die rosa‑violetten Bilder, die jeder Pathologe gut kennt. Mit der Open‑Source‑Software QuPath bauten sie eine schrittweise Pipeline auf: Zuerst korrigierten sie Farbunterschiede zwischen den Schnitten; anschließend verwendeten sie einen Watershed‑Algorithmus, um überlappende Zellkerne zu trennen; schließlich klassifizierte ein trainierter Computer jede erkannte Zelle als Tumorzelle, Stroma oder Lymphozyt. Zwei erfahrene Pathologen überprüften und korrigierten die Arbeit der Maschine wiederholt, bis sie die verschiedenen Zelltypen zuverlässig eigenständig erkannte.
Verknüpfung von Immunzellzahlen mit dem Patientenoutcome
Sobald das System Zellen zuverlässig identifizieren konnte, berechnete das Team die Anzahl an Lymphozyten pro Quadratmillimeter Tumorgewebe für mehr als 300 Patienten. Sie stellten fest, dass die TIL‑Spiegel stark variierten und im Mittel nur einen kleinen Anteil aller Zellen ausmachten. Mithilfe eines statistischen Verfahrens zur Bestimmung des informativsten Cut‑offs wählten sie 135 TILs pro Quadratmillimeter als Grenze zwischen „hohen“ und „niedrigen“ TIL‑Tumoren. Patienten, deren Tumoren diesen Schwellenwert überschritten, lebten länger als solche mit geringer Immunzellinfiltration, und dieses Muster zeigte sich sowohl in der Ursprungs‑ als auch in der Validierungsgruppe. Anders gesagt: Eine einfache Zahl aus einem automatisierten Tool erfasste bedeutende Unterschiede im Überleben und bestätigte frühere, aufwändigere Studien, die manuelle Zählungen verwendet hatten.
Wie immunreiche Tumoren „unter der Haube" aussehen
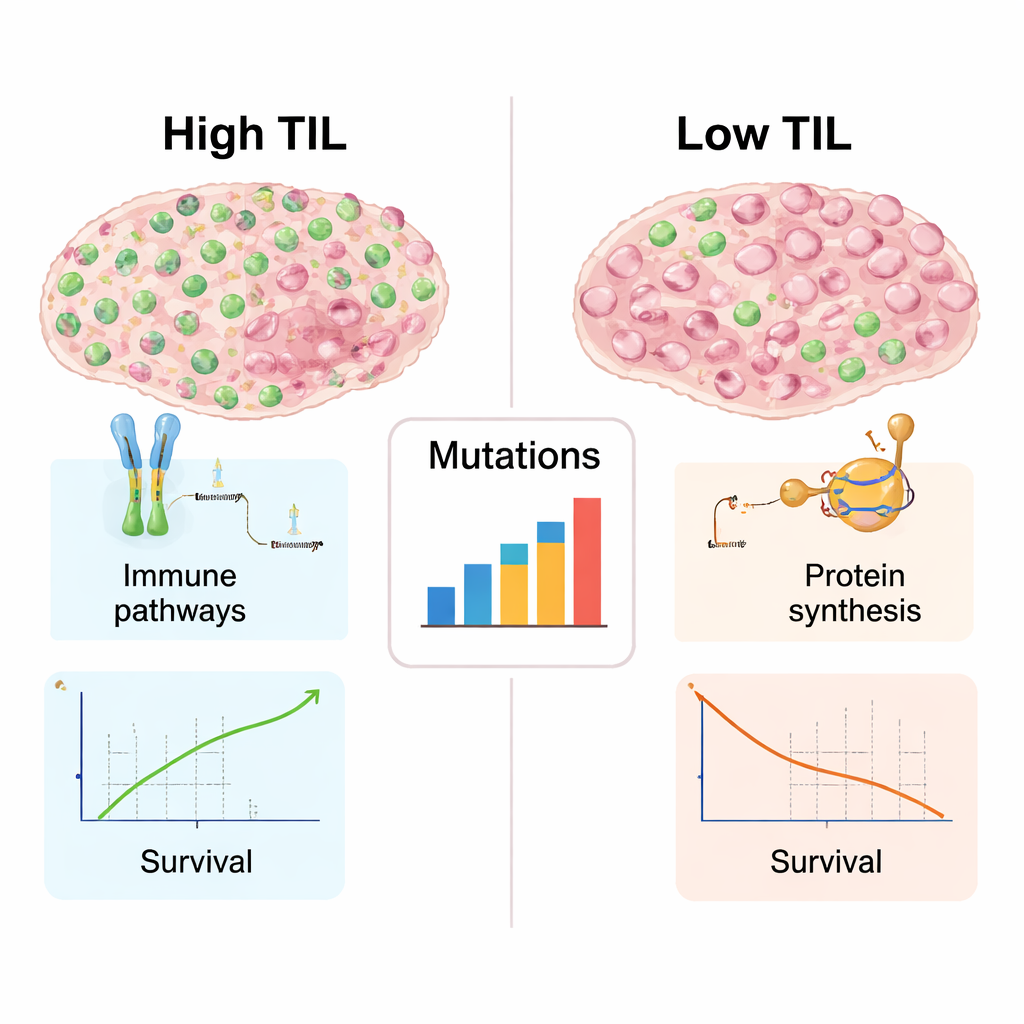
Da für viele dieser Tumoren genetische und molekulare Daten vorlagen, konnten die Autorinnen und Autoren untersuchen, was hohe‑TIL‑ von niedrige‑TIL‑Tumoren über einfache Zellzahlen hinaus unterscheidet. Tumoren, die vor Lymphozyten strotzten, zeigten stärkere Signaturen immunologischer Aktivität: Gene, die an der Erkennung abnormer Proteine, an deren Präsentation an T‑Zellen und an der Koordinierung einer Immunantwort beteiligt sind, waren stärker aktiviert. Diese Tumoren wiesen außerdem eine größere Vielfalt an DNA‑Mutationen auf, die neuartige Ziele für das Immunsystem schaffen können. Im Gegensatz dazu favorisierten die niedrigen‑TIL‑Tumoren Gene, die mit Ribosomenaufbau und Proteinsynthese verknüpft sind — ein Hinweis auf hoch aktives Wachstum, aber relativ ruhige Immunbeteiligung. Diese Trennung spiegelt den inzwischen vertrauten Gegensatz zwischen „heißen“ Tumoren, die reich an Immunzellen sind und eher auf Immuntherapie ansprechen, und „kalten“ Tumoren wider, die vom Immunsystem weitgehend ignoriert werden.
Dem Computer beibringen, den Immunstatus vorherzusagen
Die Forschenden gingen einen Schritt weiter und fragten, ob ein kompakter Satz bildbasierter Merkmale vorhersagen kann, ob ein Tumor in die Kategorie hoch‑ oder niedrig‑TIL fällt, ohne jeden Lymphozyten explizit zu zählen. Sie fassten subtile Texturmuster in den Schnitten — wie sich Pixelintensitäten in kleinen Nachbarschaften ändern — in sogenannten Haralick‑Merkmalen zusammen und kombinierten diese mit dem klinischen Tumorstadium in einem Random‑Forest‑Modell. In Kreuzvalidierung trennte dieser Klassifikator hoch‑ von niedrig‑TIL‑Tumoren mit hoher Genauigkeit, und er behielt eine angemessene Leistung in einer unabhängigen Krankenhauskohorte. Wichtig ist, dass der gesamte Ansatz auf Standardrechnern mit frei verfügbarer Software läuft, was darauf hindeutet, dass viele Pathologielabore ihn prinzipiell ohne spezielle Hardware übernehmen könnten.
Was das für die künftige Versorgung von Lungenkrebspatienten bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft: Ein Computer kann lernen, routinemäßige Lungenkrebs‑Schnitte so zu lesen, dass er erfasst, wie stark das Immunsystem den Tumor angegriffen hat. Hohe Werte infiltrierender Lymphozyten deuten auf einen aktiveren Immunkampf, eine reichere Mutationslandschaft und ein besseres Gesamtüberleben hin. Obwohl noch weitere Untersuchungen nötig sind — insbesondere bei Patienten, die tatsächlich mit Immuntherapien behandelt wurden — könnte diese automatisierte Methode irgendwann Ärzten helfen, Tumoren schnell und konsistent in immunologische „heiße“ und „kalte“ Kategorien einzuteilen. Das könnte wiederum Entscheidungen darüber leiten, wer am wahrscheinlichsten von immunbasierten Therapien profitiert, und neue Strategien anstoßen, um kalte Tumoren aufzuwärmen.
Zitation: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
Schlüsselwörter: Lungenadenokarzinom, tumorinfiltrierende Lymphozyten, maschinelles Lernen, digitale Pathologie, Krebsimmuntherapie