Clear Sky Science · de
Untersuchung des molekularen Wirkmechanismus von Celastrol, das CTNNB1/STAT3 anvisiert, zur Hemmung des Uveamelanoms basierend auf Netzwerkpharmakologie und Multi-Omics-Analyse
Traditionelle Medizin trifft auf Augenkrebs
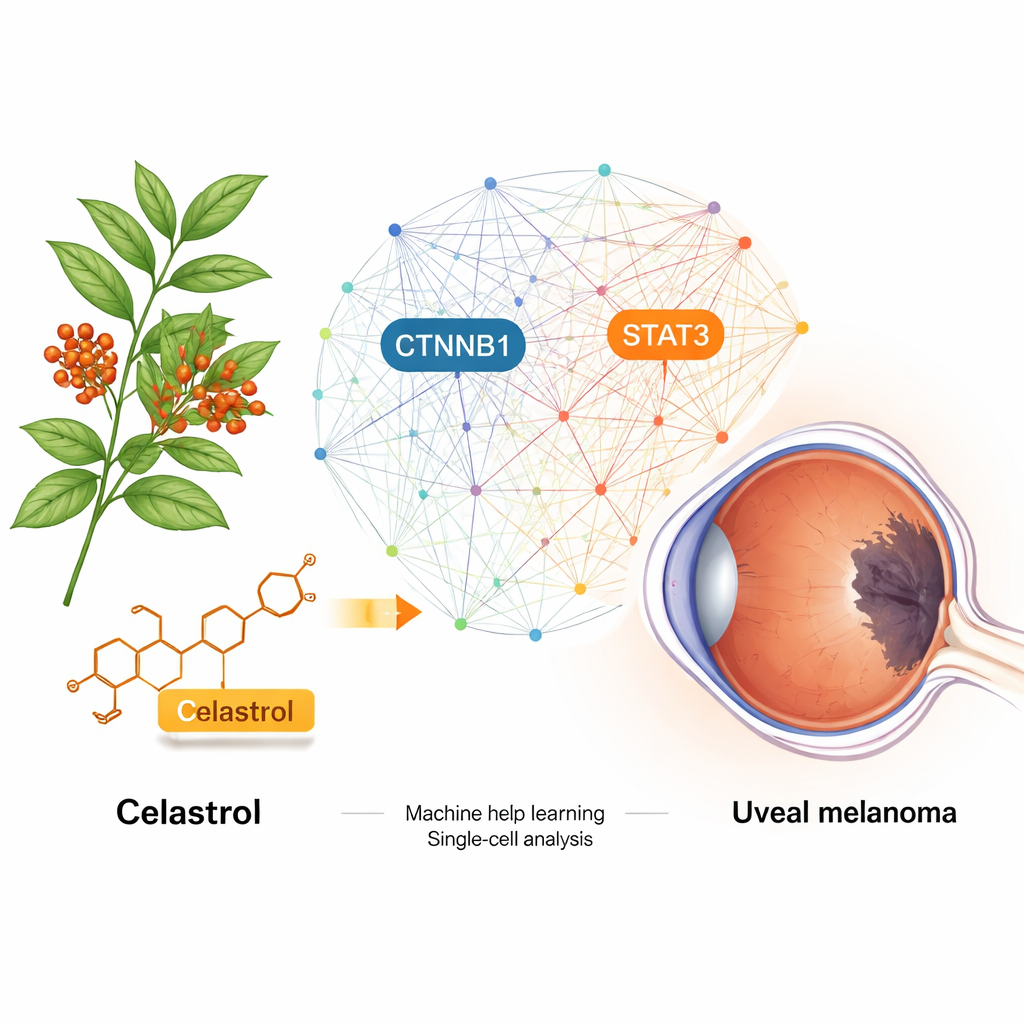
Das Uveamelanom ist eine seltene, aber tödliche Krebserkrankung, die im Inneren des Auges entsteht. Sobald sie metastasiert, ändern die heutigen Behandlungsoptionen das Ergebnis kaum. Diese Studie untersucht, ob Celastrol — ein aus einer traditionellen chinesischen Heilpflanze isolierter Wirkstoff — für den Einsatz gegen diesen Krebs repositioniert werden kann. Durch die Kombination von Big-Data-Biologie, Computersimulationen und Laborversuchen legen die Forschenden dar, wie Celastrol wichtige molekulare Schalter abschalten könnte, die dem Uveamelanom Wachstum und Ausbreitung ermöglichen.
Was diesen Augentumor so gefährlich macht
Das Uveamelanom ist der häufigste primäre Augentumor bei Erwachsenen, und bei etwa der Hälfte der Betroffenen kommt es schließlich zu Metastasen, meist in der Leber. In diesem Stadium wird das Überleben oft in Monaten gemessen. Standardbehandlungen wie Operation, Strahlentherapie und lokale Therapien können den Primärtumor im Auge kontrollieren, doch systemisch wirkende Medikamente waren bislang nur begrenzt erfolgreich und können schwere Nebenwirkungen verursachen. Deshalb suchen Wissenschaftlerinnen und Wissenschaftler nach Wirkstoffen, die sowohl das Tumorwachstum hemmen als auch besser verträglich sind — ein Bereich, in dem Naturstoffe wie Celastrol großes Interesse wecken.
Eine natürliche Verbindung unter der Lupe
Celastrol stammt aus Tripterygium wilfordii, einer Pflanze, die in der traditionellen chinesischen Medizin lange verwendet wird. Frühere Arbeiten zeigten, dass es das Wachstum verschiedener Krebsarten verlangsamen kann, doch seine Wirkung beim Uveamelanom war unklar. Das Team begann damit, zahlreiche biomedizinische Datenbanken auszuwerten, um vorherzusagen, an welche Proteine im Menschen Celastrol binden könnte und welche Proteine stark mit Uveamelanom assoziiert sind. Beim Vergleich dieser Listen fanden sie 46 überlappende Kandidaten. Mit computergestützten Werkzeugen zur Kartierung von Protein‑Interaktionen reduzierten sie diese Zahl auf einige wenige „Hub“-Moleküle, die als Kontrollpunkte wesentlicher Wachstums‑ und Überlebenswege in Tumorzellen fungieren.
Fokussierung auf zwei Hauptschalter
Um die kritischsten Akteure zu bestimmen, kombinierten die Forschenden Tumor-Genexpressionsdaten von Patientinnen und Patienten aus The Cancer Genome Atlas mit drei verschiedenen maschinellen Lernverfahren. Alle drei Ansätze liefen auf zwei Gene hinaus: CTNNB1, ein zentraler Bestandteil des Wnt‑Signalwegs, der Zellwachstum antreibt, und STAT3, ein Schlüsselfaktor für Entzündung, Überleben und Immunflucht. Weitere Analysen von Bulk-Tumorproben und Einzelzell-RNA-Sequenzierungen zeigten, dass diese Gene in Uveamelanomzellen stark aktiv sind, insbesondere in aggressiveren Zelluntergruppen, und mit Veränderungen der umliegenden Immunzellen verbunden sind. Kurz: CTNNB1 und STAT3 erscheinen als Hauptschalter, die dem Tumor helfen, zu gedeihen und das Immunsystem zu unterdrücken.
Von Computermodellen zu lebenden Zellen
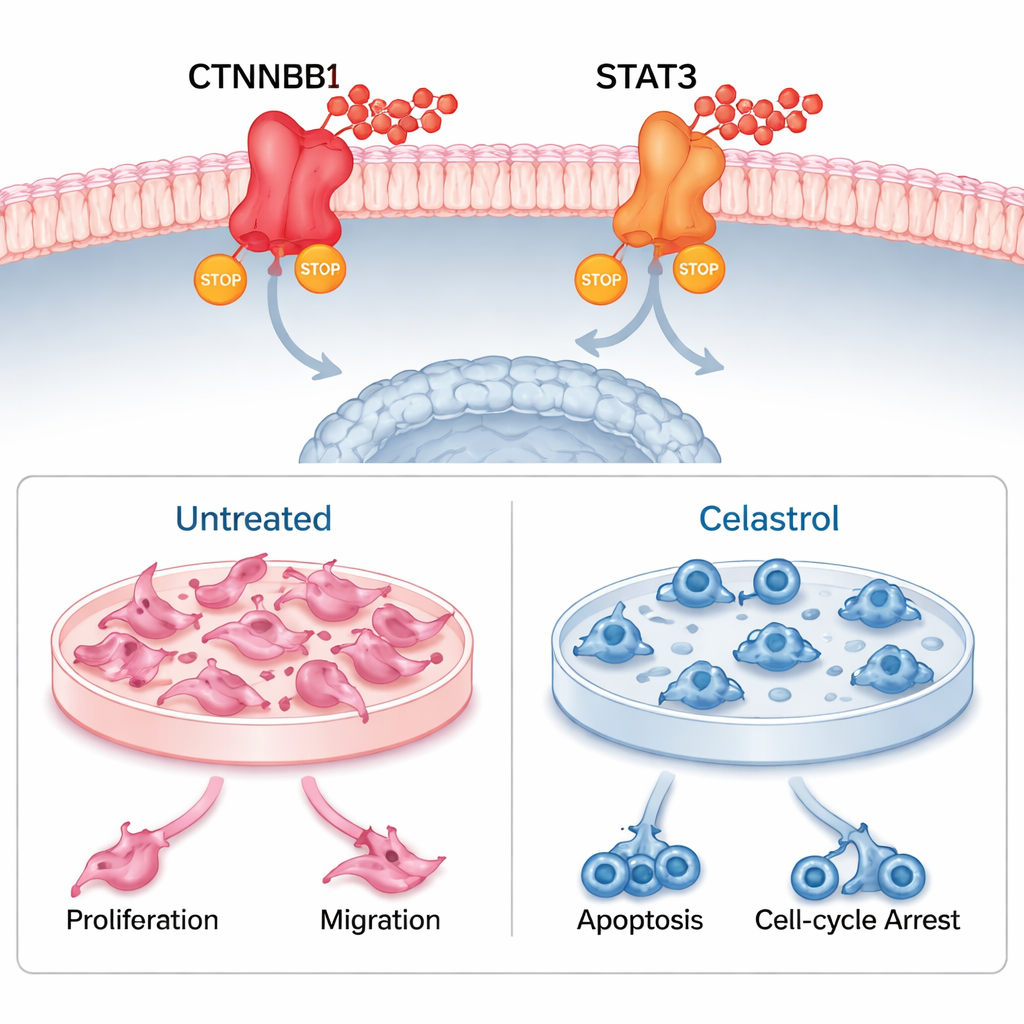
Das Team nutzte anschließend molekulares Docking und ausgedehnte molekulardynamische Simulationen, um zu testen, ob Celastrol physikalisch an CTNNB1 und STAT3 binden kann. Die virtuellen Experimente deuteten auf eine starke und stabile Bindung hin, gestützt von mehreren Wasserstoffbrücken und enger Verpackung um das Molekül. Danach folgten Laborversuche: Menschliche Uveamelanomzellen und eine verwandte Mausmelanomzelllinie wurden mit Celastrol behandelt. In beiden Zelllinien reduzierte Celastrol deutlich das Überleben und die Koloniebildung, verlangsamte die Migration in Wundheilungsassays und löste programmierte Zellsterblichkeit aus. Zudem führte es zu einem Stopp an bestimmten Zellzyklusphasen, wodurch die Zellteilung verhindert wurde. Messungen der Genaktivität und Proteinspiegel zeigten, dass Celastrol CTNNB1 und STAT3 deutlich herunterreguliert — ein Beleg dafür, dass es seine vorhergesagten Ziele in lebenden Zellen trifft.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt deuten die Ergebnisse darauf hin, dass Celastrol das Uveamelanom bekämpft, indem es CTNNB1 und STAT3 gleichzeitig ausschaltet. Diese Doppelwirkung verlangsamt nicht nur Tumorwachstum und -ausbreitung, sondern könnte auch die Immunumgebung des Tumors so umgestalten, dass sie eine krebsbekämpfende Reaktion begünstigt. Zwar wurden die Untersuchungen bislang in Zellen und Computersimulationen durchgeführt — nicht in Patientinnen, Patienten oder Tiermodellen — doch sie legen eine solide Grundlage für weitergehende Tests. Für nichtfachliche Leser ist die Kernbotschaft: Eine Verbindung mit Wurzeln in der traditionellen Medizin hat sich als wissenschaftlich plausibler Kandidat für eine neue Klasse von Augenkrebs‑Therapien herauskristallisiert, die sowohl den Tumor als auch dessen zelluläres Umfeld adressiert.
Zitation: Li, Z., Xi, R., Han, X. et al. Research on the molecular mechanism of celastrol targeting CTNNB1/STAT3 to inhibit uveal melanoma based on network pharmacology and multi-omics analysis. Sci Rep 16, 6140 (2026). https://doi.org/10.1038/s41598-026-37061-5
Schlüsselwörter: Uveamelanom, Celastrol, Augenkrebs, Krebs-Signalgebung, Tumormikroumgebung