Clear Sky Science · de
Ein einheitliches multimodales Transformer‑Framework zur Vorhersage des Rückfalls bei Brustkrebs und zur Überlebensanalyse
Warum die Vorhersage eines Krebsrückfalls wichtig ist
Für viele Frauen bringt das Ende der Brustkrebstherapie Erleichterung, aber oft bleibt die Frage: Kommt die Krankheit zurück, und wenn ja, wann und wie schwer? Heute basieren Nachsorgepläne häufig auf groben Durchschnittswerten statt auf der einzigartigen Kombination von Faktoren, die jede Patientin ausmachen. Diese Studie stellt ein neues System der künstlichen Intelligenz vor, das Ärzten eine klarere, stärker personalisierte Einschätzung sowohl des Rückfallrisikos als auch der zu erwartenden krebsfreien Zeit geben soll.
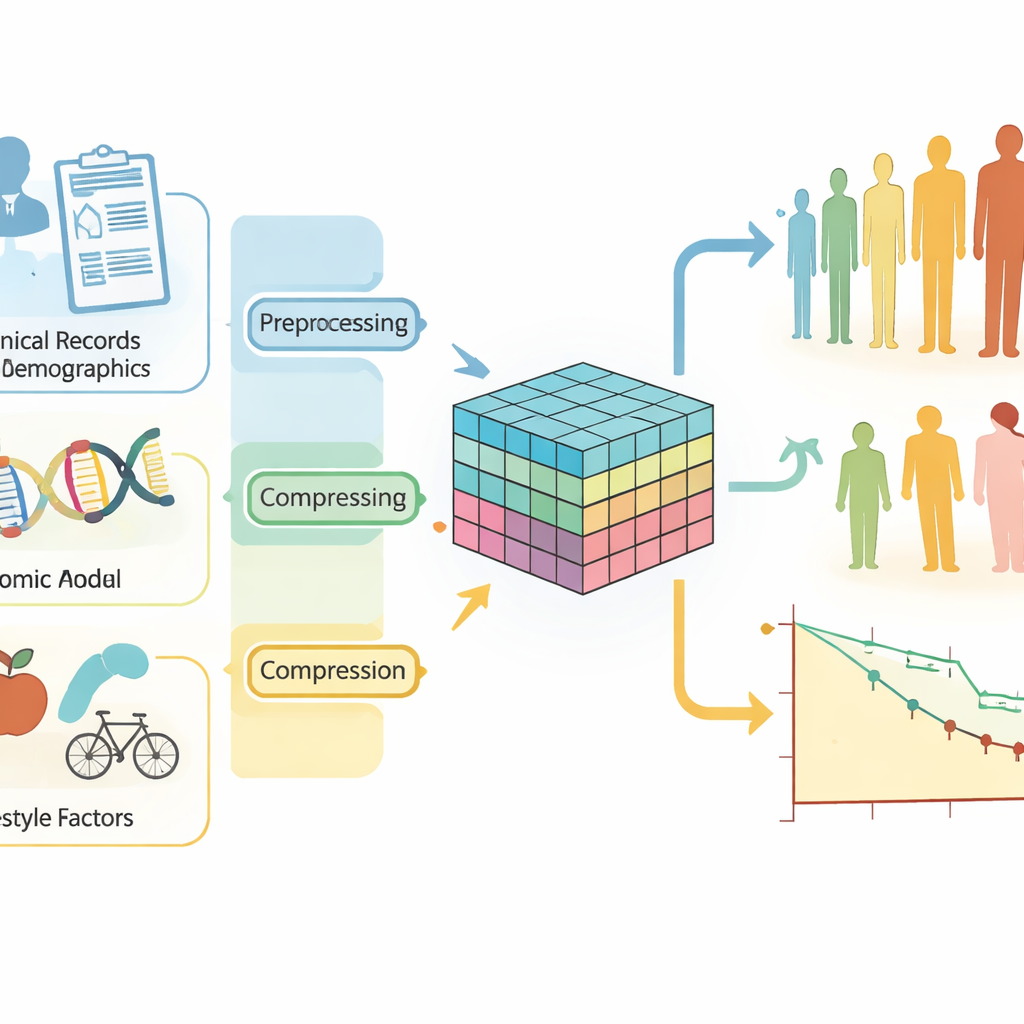
Verschiedene Patientendaten zusammenführen
Ein Rückfall von Brustkrebs ist kein einheitliches Ereignis. Er kann als neuer Tumor in derselben Brust auftreten, sich in benachbarte Lymphknoten ausbreiten oder als Fernmetastase in Organen wie Lunge oder Knochen vorkommen. Jede Form hat unterschiedliche Konsequenzen für Behandlung und Prognose. Gleichzeitig wird das Risiko von vielen miteinander verflochtenen Einflüssen bestimmt: Tumorcharakteristika, Genaktivität, Alter, Menopausenstatus, Körpergewicht, Rauchen und mehr. Traditionelle statistische Werkzeuge haben Schwierigkeiten mit diesem Mix aus klinischen, genetischen und Lebensstil‑Daten. Sie gehen oft von einfachen, linearen Zusammenhängen aus und stützen sich auf handgefertigte Risikoscores, die die wahre Komplexität moderner Krebsdaten nicht erfassen können.
Ein einheitliches intelligentes Modell statt getrennter Werkzeuge
Die Forscher entwickelten ein einziges Deep‑Learning‑Framework, das zwei Aufgaben zugleich löst: Es sagt voraus, welche von vier Rückfallformen für eine Patientin am wahrscheinlichsten ist, und schätzt mittels Überlebensanalyse den Zeitpunkt dieses Ereignisses. Anstatt getrennte Modelle für „Kommt er zurück?“ und „Wann kommt er zurück?“ zu bauen, lernt das System beide Antworten gemeinsam. Im Inneren nutzt es eine Transformer‑Architektur — dieselbe Modellklasse, die viele moderne Sprachwerkzeuge antreibt — um subtile Muster und Fernverknüpfungen in den Daten zu entdecken. Dieser einheitliche Ansatz soll das Denken von Onkologen widerspiegeln, die viele Hinweise gleichzeitig abwägen, statt isolierte Berechnungen durchzuführen.
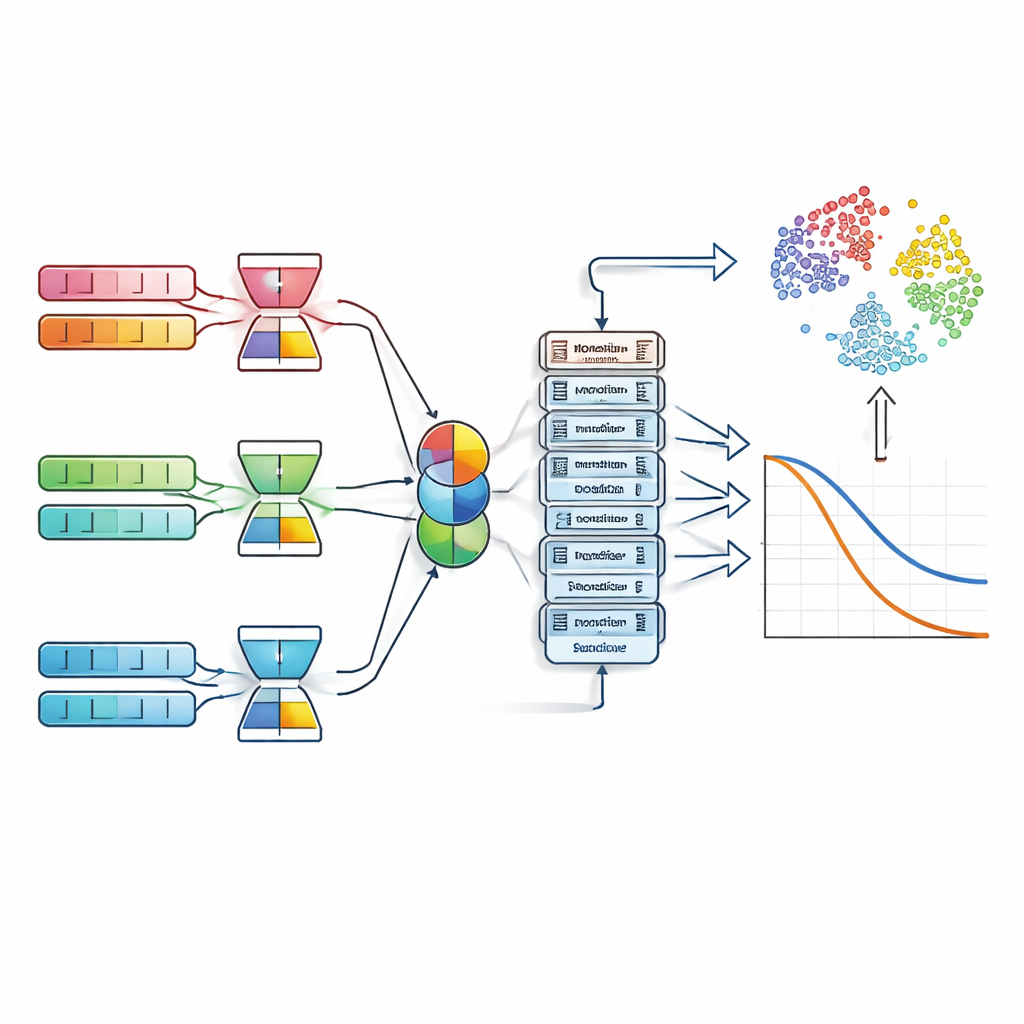
Wie das System Muster in Gesundheitsdaten liest
Um das Modell zu versorgen, stellte das Team eine große multizentrische Sammlung von Brustkrebsdaten aus fünf etablierten Quellen zusammen. Diese umfassen Tausende von Patientinnen mit detaillierten klinischen Messwerten, Genexpressionsprofilen, demografischen Angaben und Lebensstilindikatoren. Da solche Daten rauschbehaftet und hochdimensional sein können — insbesondere die zehntausenden Genaktivitätsmessungen — durchläuft jede Datenart zunächst einen „Denoising‑Autoencoder“. Dieser Schritt komprimiert jede Modalität in eine sauberere, kompakte Repräsentation, die wichtige biologische Signale erhält und Zufälligkeiten herausfiltert.
Lernen, was für jede Patientin am wichtigsten ist
Nach der Kompression fügt das Modell die Merkmale nicht einfach zusammen. Stattdessen wendet es einen Modalitäts‑Attention‑Mechanismus an, der lernt, wie viel Gewicht klinischen, genetischen oder Lebensstil‑Informationen für jede einzelne Patientin beizumessen ist. Bei einigen Patientinnen dominieren vielleicht Tumorgröße und Hormonrezeptorstatus; bei anderen ist ein bestimmtes Genmuster oder die Raucheranamnese aussagekräftiger. Diese gewichteten Signale werden zu einem einzelnen Patientenprofil verschmolzen und von gestapelten Transformer‑Schichten verarbeitet, die mittels Self‑Attention modellieren, wie verschiedene Risikofaktoren miteinander interagieren. Aus dieser gemeinsamen Repräsentation sagt ein Zweig die Rückfallart voraus, während ein anderer einen kontinuierlichen Risikoscore schätzt, der in Überlebenskurven über fünf und zehn Jahre übersetzt werden kann.
Leistung, Validierung und Interpretierbarkeit
In Tests über die fünf Datensätze hinweg übertraf das einheitliche System konstant Standardmethoden wie logistische Regression, Support‑Vector‑Machines, Random Forests, klassische Cox‑Überlebensmodelle und einfachere neuronale Netze. Es erreichte etwa 98–99 % Genauigkeit bei der Klassifizierung der Rückfallart und einen hohen Konkordanzindex — ein etabliertes Maß dafür, wie gut die prognostizierte Reihenfolge des Überlebens mit der Realität übereinstimmt. Cross‑Dataset‑Experimente, bei denen das Modell in einer Kohorte trainiert und in einer anderen getestet wurde, zeigten, dass es besser generalisierte als konkurrierende Ansätze. Um zu vermeiden, dass es zu einer mysteriösen „Black Box“ wird, nutzten die Autoren außerdem Erklärungswerkzeuge, die hervorheben, welche Merkmale jede Vorhersage am stärksten beeinflussten. Tumorgröße, HER2‑Status, Rauchen, Menopausenstatus, Alter bei Diagnose und BRCA1‑Mutationen erwiesen sich als besonders wichtig und stimmen gut mit dem aktuellen medizinischen Wissen überein.
Was das für Patientinnen und Ärzte bedeutet
Die Kernbotschaft der Studie ist, dass ein einziges, sorgfältig gestaltetes KI‑System viele Informationsstränge integrieren kann, um ein reichhaltigeres, zuverlässigeres Bild des Rückfallrisikos und des Überlebens bei Brustkrebs zu liefern. Obwohl es noch prospektive Prüfungen in der klinischen Praxis benötigt, könnte das Framework eines Tages Ärzten helfen, Überwachungspläne zu individualisieren, Behandlungen zu wählen und Patientinnen mit größerer Sicherheit zu beraten. Für Patientinnen könnte dies in Nachsorgeplänen resultieren, die besser ihrem tatsächlichen Risiko entsprechen — unnötige Ängste und Untersuchungen für einige reduzieren und andere identifizieren, die von engerer Überwachung oder aggressiverer Therapie profitieren könnten.
Zitation: Malik, S., Patro, S.G.K., Al-Nussairi, A.K.J. et al. A unified multi modal transformer framework for breast cancer recurrence prediction and survival analysis. Sci Rep 16, 8334 (2026). https://doi.org/10.1038/s41598-026-37046-4
Schlüsselwörter: Rückfall bei Brustkrebs, Überlebensvorhersage, multimodales Deep Learning, Transformer‑Modell, personalisierte Onkologie