Clear Sky Science · de
Potenzielle Biomarker für frühe Zahnfleischentzündungen: Untersuchung von CD5+ B-Zellen, Speichelzytokinen und dem oralen Mikrobiom
Warum Ihr Zahnfleisch für den ganzen Körper wichtig ist
Blutendes Zahnfleisch lässt sich leicht übersehen, doch die dahinterstehende Entzündung kann leise den Knochen abbauen, der die Zähne hält, und steht in Zusammenhang mit Herzkrankheiten, Diabetes und anderen Leiden. In dieser Studie wurde untersucht, ob frühe Warnzeichen für solche Schäden in einer alltäglichen Probe – Speichel – zusammen mit bestimmten Immunzellen im Blut und der Bakterienzusammensetzung unter dem Zahnfleisch gefunden werden können. Zuverlässige frühe Marker könnten Zahnärzten helfen, Hochrisikopatienten lange vor irreversiblem Zahnverlust zu erkennen.
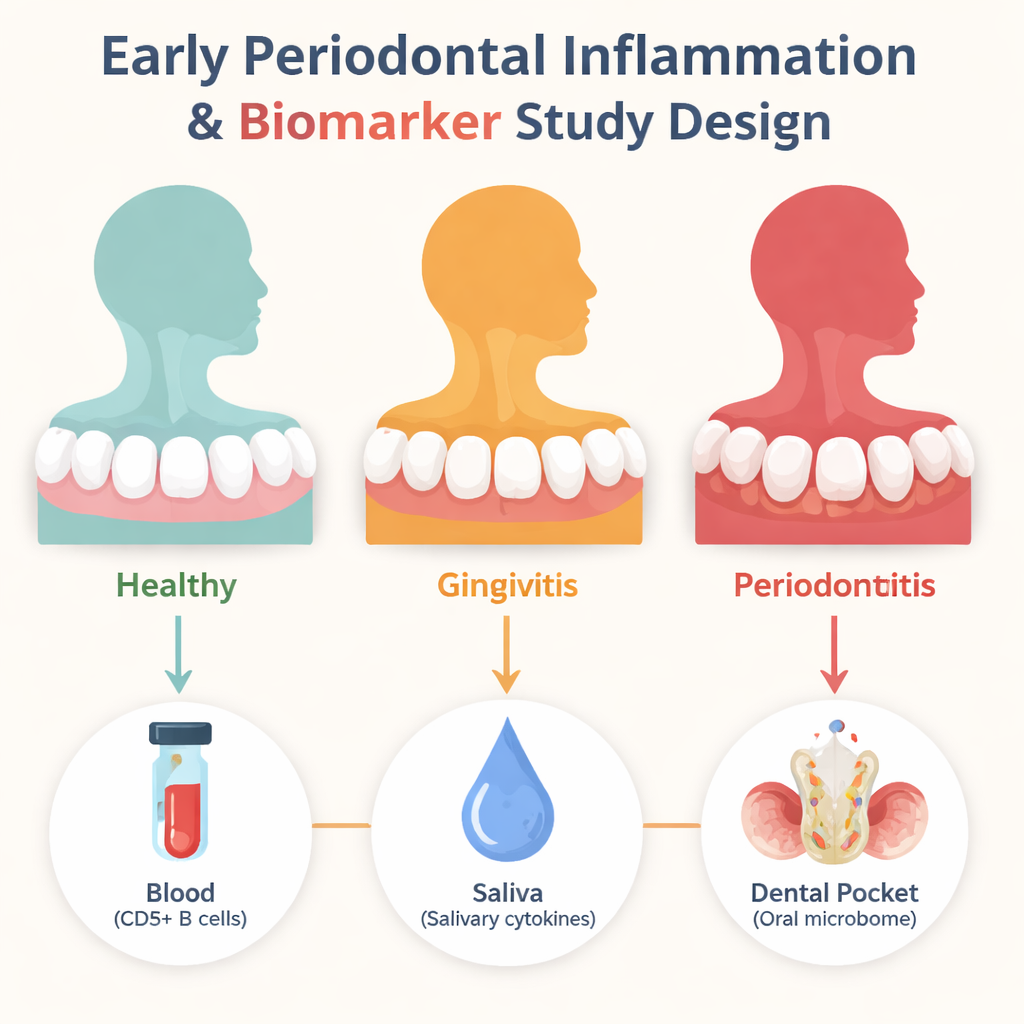
Auf der Suche nach frühen Warnlichtern
Die Forschenden konzentrierten sich auf drei Hinweisarten. Erstens untersuchten sie eine spezielle Gruppe von Immunzellen im Blut, die CD5-positiven B-Zellen genannt werden und bei schwerer Zahnfleischerkrankung sowie rheumatoider Arthritis mit Knochenabbau und Autoimmunreaktionen in Verbindung gebracht wurden. Zweitens bestimmten sie Dutzende von Signaleiweißen, sogenannten Zytokinen, im Speichel, die als chemische Alarme wirken, wenn Gewebe gereizt sind. Drittens sequenzierten sie bakterielle DNA aus Flüssigkeit aus Zahnfleischtaschen, um zu sehen, wie sich das orale Mikrobiom verschiebt, wenn Gesundheit in Gingivitis und dann in moderate Parodontitis übergeht. Sechzig nichtrauchende Erwachsene wurden anhand von Taschentiefen, Blutungs- und Plaque-Werten sorgfältig in gesund, Gingivitis bzw. moderate chronische Parodontitis eingeteilt.
Immunzellen im Blut bleiben still
Auf Basis früherer Arbeiten bei fortgeschrittener Erkrankung erwartete das Team, dass Menschen mit Parodontitis bereits erhöhte Zahlen CD5-positiver B-Zellen im Blut zeigen könnten, als Zeichen einer systemischen Reaktion auf chronische Zahnfleischinfektion. Überraschenderweise waren die Gesamtkonzentrationen dieser Zellen in allen drei Gruppen im Wesentlichen gleich und lagen bei etwa einem Fünftel aller B-Zellen. Selbst bei Aufschlüsselung nach Entwicklungsstadien – unreif, naiv und mehrere Gedächtniszelltypen – zeigte sich kein statistisch signifikanter Trend. Einige Gedächtniszellen, insbesondere solche, die mit langanhaltenden Reaktionen assoziiert sind, zeigten eine Tendenz zu geringeren Werten bei Erkrankten, was darauf hindeuten könnte, dass sie das Blut verlassen, um sich im entzündeten Zahnfleisch anzusammeln; größere Studien sind jedoch nötig, um diesen subtilen Befund zu bestätigen.
Speichel und Bakterien erzählen eine stärkere Geschichte
Im Gegensatz dazu spiegelten Speichel und die bakterielle Gemeinschaft unter dem Zahnfleisch deutlich den Erkrankungsstand wider. Menschen mit Parodontitis hatten ungefähr das Doppelte des Medianwerts des Chemokins IL-8 im Speichel im Vergleich zu Gesunden oder Gingivitis-Teilnehmenden und zeigten wesentlich häufiger nachweisbares IL-17A sowie Hinweise auf Aktivität von IL-6 und IL-1β. Diese Moleküle locken Immunzellen an und fördern knochenabbauende Prozesse, weshalb ihr Anstieg darauf hindeutet, dass entzündliche Kreisläufe bereits in moderater Erkrankung aktiv sind. Gleichzeitig zeigte die DNA-Sequenzierung, dass gesunde Münder von harmlosen, sauerstoffliebenden Bakterien wie Rothia und Streptococcus dominiert waren. Bei Gingivitis und besonders bei Parodontitis verschob sich das Gleichgewicht hin zu sauerstoffscheuen, gramnegativen Arten wie Tannerella, Fusobacterium, Treponema und Fretibacterium, die als bekannte oder neu erkannte Täter beim Zahnfleischabbau gelten.
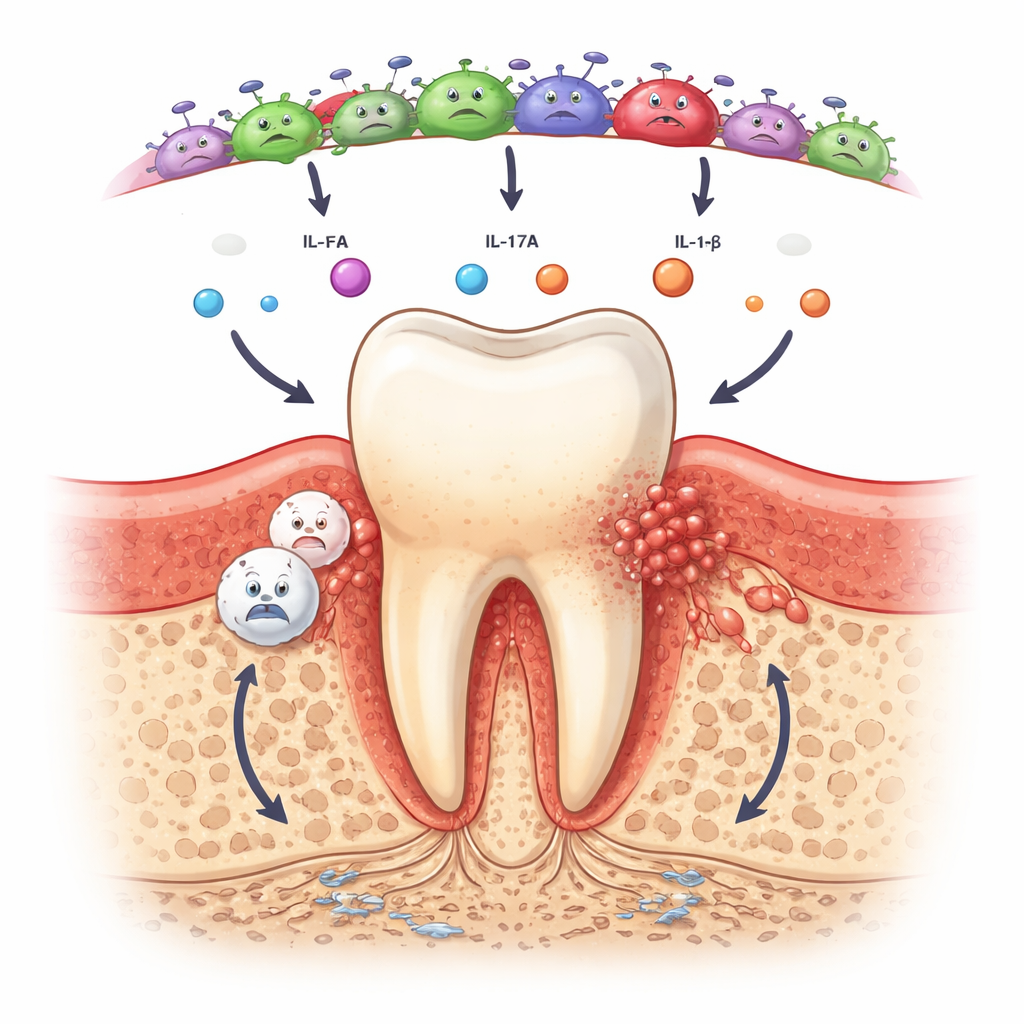
Frühe Hinweise auf ein Hochrisiko‑Signatur
Durch die Kombination von Statistik und maschinellem Lernen identifizierte das Team bakterielle Gruppen, die gesund von krank am besten unterschieden. Zwei Stämme von Tannerella forsythia und mehrere Fretibacterium‑Arten erwiesen sich als besonders aussagekräftig, während eine Rothia‑Art auf gesünderes Zahnfleisch hinwies. Ein aufschlussreicher Befund kam aus der Gingivitis‑Gruppe: Die IL‑8‑Spiegel im Speichel korrelierten eng mit der Häufigkeit einer bakteriellen Gattung namens Megasphaera. Dieser Zusammenhang trat in gesunden Mündern oder bei ausgeprägter Parodontitis nicht auf, was darauf hindeutet, dass Megasphaera zusammen mit IL‑8 als Indikator für ein frühes Stadium fungieren könnte, solange der Schaden noch begrenzt und potenziell reversibel ist. Die Stichprobengröße war jedoch begrenzt, und die Autorinnen und Autoren betonen, dass solche Muster in größeren, langfristigen Studien geprüft werden müssen, bevor sie für die Versorgung nutzbar sind.
Was das für Patientinnen und Patienten bedeutet
Für Menschen, die sich um ihr Zahnfleisch sorgen, lautet die Kernbotschaft: Der Körper sendet frühe biochemische Warnsignale, aber diese zeigen sich stärker lokal im Speichel und in den Zahnfleischbakterien als in zirkulierenden Immunzellen, solange die Erkrankung noch moderat ist. Routinemäßige Bluttests auf CD5‑positive B‑Zellen werden wahrscheinlich keine frühe Parodontitis anzeigen. Vielversprechender ist stattdessen ein kombiniertes Speichel‑und‑Mikrobiom‑Panel, das mehrere Zytokine – insbesondere IL‑8 und IL‑17A – zusammen mit Schlüsselbakterien wie Tannerella, Fretibacterium und Megasphaera erfasst. Wenn dies validiert wird, könnte ein solcher einfacher Mundtest Zahnärzten helfen, Hochrisikopatienten früher zu erkennen, Reinigungen und Therapien anzupassen und möglicherweise sowohl Zahnverlust als auch einige der übergeordneten Gesundheitsprobleme zu verhindern, die mit chronischer Zahnfleischentzündung verbunden sind.
Zitation: Gottschalk, E.C., Chabanovska, O., Vasudevan, P. et al. Potential biomarkers for early periodontal inflammation: investigating CD5+ B cells, salivary cytokines and oral microbiome. Sci Rep 16, 7192 (2026). https://doi.org/10.1038/s41598-026-37044-6
Schlüsselwörter: Zahnfleischerkrankung, orales Mikrobiom, Speichelbiomarker, Parodontitis, Entzündung