Clear Sky Science · de
Durch maschinelles Lernen ermöglichte Vorhersage der hämorrhagischen Transformation nach Thrombektomie mithilfe quantitativer DSA
Warum das für Schlaganfallpatienten wichtig ist
Wenn jemand einen schweren Schlaganfall erleidet, können Ärztinnen und Ärzte in manchen Fällen das Gerinnsel aus der Hauptarterie des Gehirns mit einem winzigen Gerät entfernen — ein Eingriff, der als mechanische Thrombektomie bezeichnet wird. Das hat die Schlaganfallversorgung revolutioniert, doch viele Patientinnen und Patienten erholen sich trotzdem schlecht, weil bei einigen nach dem Eingriff neue Blutungen im Gehirn auftreten. Die hier beschriebene Studie stellt eine einfache, aber entscheidende Frage: Lassen sich Informationen, die während der Intervention ohnehin erhoben werden, zusammen mit modernen Methoden des maschinellen Lernens nutzen, um vorherzusagen, welche Patienten am ehesten bluten und zusätzlichen Schutz benötigen?
Weiter denken als „Arterie offen oder verschlossen“
Heute wird der Erfolg einer Thrombektomie meist danach beurteilt, ob die zuvor verschlossene Arterie auf der Angiographie — einer Art Echtzeit-Röntgenfilm der Gefäße — wieder offen erscheint. Diese grobe Bewertung zeigt jedoch nicht, was in den kleinen, nachgeschalteten Gefäßen des Gehirns passiert, wo der eigentliche Schaden und die Blutung entstehen. Einige Patientinnen und Patienten mit scheinbar perfekter Wiedereröffnung großer Gefäße entwickeln dennoch schwere Hirnblutungen, eine Komplikation, die als hämorrhagische Transformation bezeichnet wird. Die Autoren vermuteten, dass detailliertere Messungen des Blutflusses in diesen kleinen Gefäßen, gewonnen aus derselben Angiographie, verborgene Hinweise darauf enthalten könnten, wer gefährdet ist.
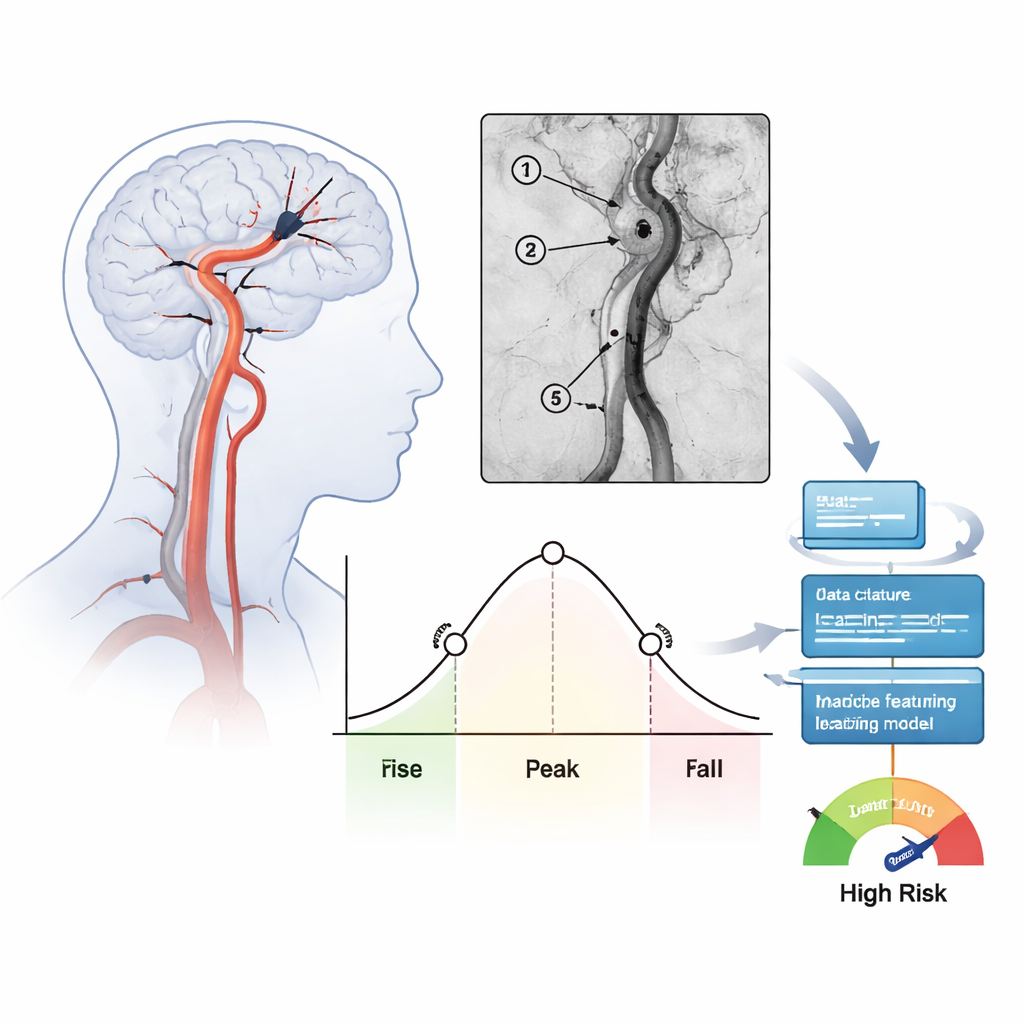
Angiographie-Filme in Zahlen verwandeln
Das Team untersuchte 171 Personen, die innerhalb eines Jahres an einem einzigen Krankenhaus wegen schwerer Schlaganfälle im vorderen Hirnkreis behandelt wurden. Nachdem die Ärztinnen und Ärzte das Gerinnsel entfernt und den Blutfluss wiederhergestellt hatten, wurden Standardansichten der Angiographie aufgezeichnet und anschließend analysiert, wie sich das injizierte Kontrastmittel an mehreren Schlüsselpunkten entlang der behandelten Arterie ein- und auswaschte. Für jede Region berechneten sie zeitliche Kennwerte wie die mittlere Verweilzeit (mean transit time) und die Breite des Hauptkontrastanlaufs (full width at half maximum). Diese Zahlen fassen zusammen, ob das Blut langsam und gleichmäßig fließt oder schnell in einem schmalen Puls hindurchschießt. Insgesamt wurden für jede Patientin bzw. jeden Patienten 39 solcher Flussmerkmale extrahiert und auf Übereinstimmung zwischen unabhängigen Bewertern geprüft.
Den Computer beibringen, riskante Muster zu erkennen
Die Forschenden nutzten dann eine Reihe gängiger Methoden des maschinellen Lernens, um zu prüfen, ob diese Flussmerkmale — allein oder kombiniert mit einfachen klinischen Daten wie Alter und Schlaganfallschwere — Patientinnen und Patienten, die später eine Hirnblutung entwickelten, von denen ohne Blutung unterscheiden konnten. Um Überanpassung zu vermeiden, verwendeten sie zunächst fünf verschiedene Verfahren zur Merkmalsauswahl, um die informativsten Messgrößen herauszufiltern, und teilten die Daten wiederholt mit Kreuzvalidierung in Trainings- und Testsets auf. Unter vielen getesteten Kombinationen schnitt ein vergleichsweise einfaches Modell — logistische Regression, abgestimmt mit einem "Elastic Net"-Merkmalsfilter — am besten ab. Wenn es nur auf angiographieabgeleiteten Flussmaßen beruhte, trennte es Patientinnen und Patienten mit und ohne Blutung mit einer mittleren Fläche unter der ROC-Kurve von etwa 0,81. Mit hinzugefügten klinischen Faktoren stieg die Leistung auf ungefähr 0,86, was darauf hindeutet, dass das Modell ein starkes Entscheidungsinstrument sein könnte.
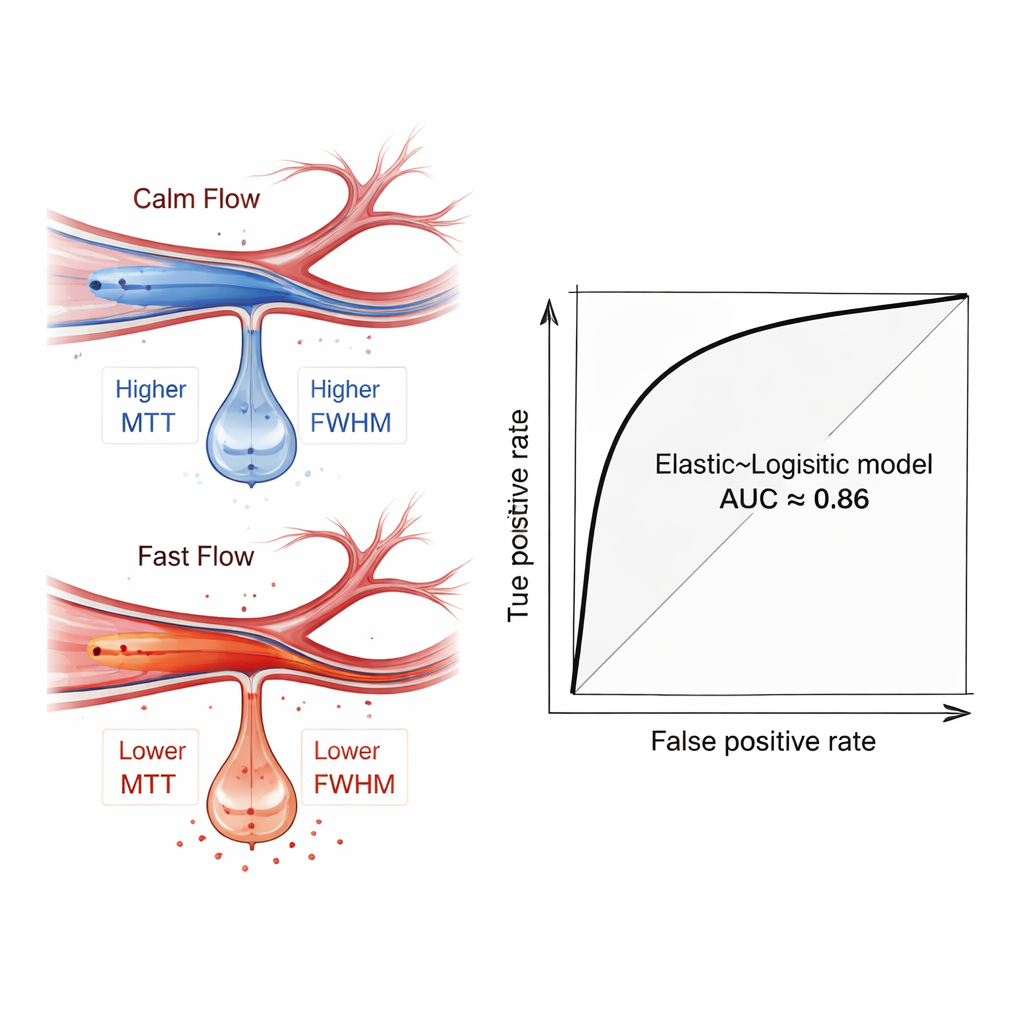
Was die Blutfluss-Signale offenbarten
Bei der Analyse der trainierten Modelle nutzten die Autorinnen und Autoren eine Interpretierbarkeitstechnik namens SHAP, um zu ermitteln, welche Merkmale am wichtigsten waren. Messgrößen, die erfassten, wie lange und wie breit der Flusspuls war — besonders in einem weiter entfernten Ast der Arteria cerebri media — hoben sich als Schlüsselfaktoren hervor. Patientinnen und Patienten, die später bluteten, zeigten tendenziell einen schnelleren, fokussierteren Fluss in diesen distalen Gefäßen, sichtbar durch kürzere Transitzeiten und schmalere Peaks. Dieses Muster ist ein hämodynamischer Fingerabdruck von „Hyperperfusion“, einem Zustand, in dem zuvor unterversorgtes, verletzliches Hirngewebe nach plötzlicher Hochgeschwindigkeits-Perfusion eher zu einem Leck und zu Blutungen neigt. Wichtig ist, dass dieses Signal auch dann sichtbar wurde, wenn einfache Gruppenvergleiche keine dramatischen statistischen Unterschiede zeigten — was den Wert einer multivariaten, maschinengestützten Analyse unterstreicht.
Wie sich das an der Krankenbettseite auswirken könnte
Weil die Methode Bilder verwendet, die während der Thrombektomie ohnehin angefertigt werden, sind keine zusätzlichen Untersuchungen, kein zusätzliches Kontrastmittel und keine zusätzliche Strahlung erforderlich. Sobald die Regionen von Interesse markiert sind — ein Schritt, der derzeit ein paar Minuten dauert — kann der Computer automatisch Flussmaße berechnen und eine personalisierte Abschätzung des Blutungsrisikos erzeugen. Grundsätzlich könnte dies Ärzten helfen, Blutdruckziele anzupassen, zu entscheiden, wie aggressiv blutverdünnende Medikamente eingesetzt werden sollten, und bei als hochriskant eingestuften Patientinnen und Patienten frühere CT-Scans zu planen. Die Autorinnen und Autoren mahnen jedoch zur Vorsicht: Ihre Studie ist retrospektiv und stammt aus einem einzigen Zentrum, weshalb größere, multizentrische Studien erforderlich sind, bevor das Werkzeug die Routineversorgung leiten kann. Dennoch liefert sie einen klaren Proof of Concept: Indem man Schlaganfall-Angiographien in reichhaltige numerische Daten verwandelt und maschinelles Lernen darauf ansetzt, können wir über die einfache Frage „Ist die Arterie offen?“ hinausgehen hin zu „Ist die Mikrozirkulation des Gehirns sicher?“ — eine Verschiebung, die letztlich mehr Patientinnen und Patienten vor gefährlichen Nachbehandlungsblutungen bewahren könnte.
Zitation: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Schlüsselwörter: Schlaganfall, mechanische Thrombektomie, Hirnblutung, maschinelles Lernen, Angiographie