Clear Sky Science · de
Auswirkungen neuberoendokriner-tumorspezifischer systemischer Behandlungen auf Expression und Funktion von CXCR4 in neuroendokrinen Tumorzellen
Warum das für die künftige Krebsversorgung wichtig ist
Wenn bestimmte seltene Krebserkrankungen des Darms und der Bauchspeicheldrüse aggressiver werden, sprechen sie oft nicht mehr auf die üblichen gezielten Therapien an. Ärztinnen, Ärzte und Forschende brauchen dringend neue Möglichkeiten, diese hartnäckigen Tumoren sichtbar zu machen und anzugreifen. Die vorliegende Studie stellt eine praktische Frage mit großer Tragweite: Verändern die Chemotherapeutika und gezielten Wirkstoffe, die Patienten bereits erhalten, einen wichtigen Tumormarker namens CXCR4, der als diagnostischer „Leuchtfeuer“ und als Therapieziel entwickelt wird?
Ein sich veränderndes Ziel auf aggressiven Tumorzellen
Neuroendokrine Neoplasien sind seltene Tumoren, die aus hormonproduzierenden Zellen entstehen, meist im Darm oder in der Bauchspeicheldrüse. In frühen, weniger aggressiven Stadien zeigen diese Tumoren häufig ein Oberflächenmolekül, den Somatostatinrezeptor 2, den Ärztinnen und Ärzte mit speziellen radioaktiven Wirkstoffen sowohl sichtbar machen als auch therapieren können. Mit zunehmender Aggressivität verlieren die Tumoren diesen Marker jedoch oft, was Erkennung und gezielte Therapie erschwert. Gleichzeitig schalten viele von ihnen einen anderen Oberflächenrezeptor ein, CXCR4, der mit schnellerem Wachstum, Fernmetastasen und schlechterer Prognose verbunden ist. Da sich CXCR4 mit einem PET-Tracer darstellen lässt und potenziell mit radioaktiven oder gegen Antikörper gerichteten Therapien angegriffen werden kann, gilt er als vielversprechendes „Backup“-Ziel, wenn Standardoptionen versagen.
Prüfung realer Medikamente in Tumorzellmodellen
Die Forschenden wollten wissen, wie die bereits eingesetzten Wirkstoffe gegen hochgradige neuroendokrine Tumoren CXCR4 selbst beeinflussen. Wenn diese Medikamente CXCR4 unbeabsichtigt reduzieren, könnten sie nachfolgende CXCR4-basierte Bildgebung oder Therapien schwächen — sie könnten aber auch die Aggressivität des Tumors dämpfen. Das Team arbeitete mit drei verschiedenen humanen Tumorzelllinien, die aggressive Krankheitsformen repräsentieren, darunter eine hybride Linie, die schwer behandelbare Tumoren gut nachahmt. Die Zellen wurden sechs gängigen Substanzen ausgesetzt: den Chemotherapeutika Cisplatin, Etoposid, Streptozotocin, 5‑Fluorouracil, dem oralen Temozolomid und dem zielgerichteten mTOR-Inhibitor Everolimus. Nach der Behandlung bestimmten die Forschenden CXCR4 auf Gen- und Proteinebene und prüften, wie gut die Zellen weiterhin einen CXCR4-suchenden PET-Tracer aufnehmen konnten.
Einige Wirkstoffe dämpfen das CXCR4-Signal
Die Ergebnisse zeigten, dass nicht alle Krebsmedikamente gleich auf diesen Rezeptor wirken. Cisplatin reduzierte die CXCR4-Genaktivität deutlich in zwei der drei Zelllinien und verringerte die Traceraufnahme in zwei Zelllinien signifikant — ein Hinweis darauf, dass weniger funktionsfähige Rezeptoren für den Tracer vorhanden waren. Temozolomid und Everolimus senkten ebenfalls CXCR4-Mengen auf Gen- und Proteinebene in mehreren Zelltypen, wenngleich sich dies nicht stets in einem statistisch klaren Rückgang der Traceraufnahme niederschlug. Demgegenüber hatten Etoposid und Streptozotocin kaum Einfluss auf CXCR4, während 5‑Fluorouracil nur mäßige Veränderungen bewirkte, die die Tracerbindung nicht stark veränderten. Insgesamt deutet das Muster darauf hin, dass Cisplatin, Temozolomid und Everolimus CXCR4 in diesen aggressiven Tumorzellen dämpfen können, während die anderen Wirkstoffe es größtenteils unbeeinflusst lassen.
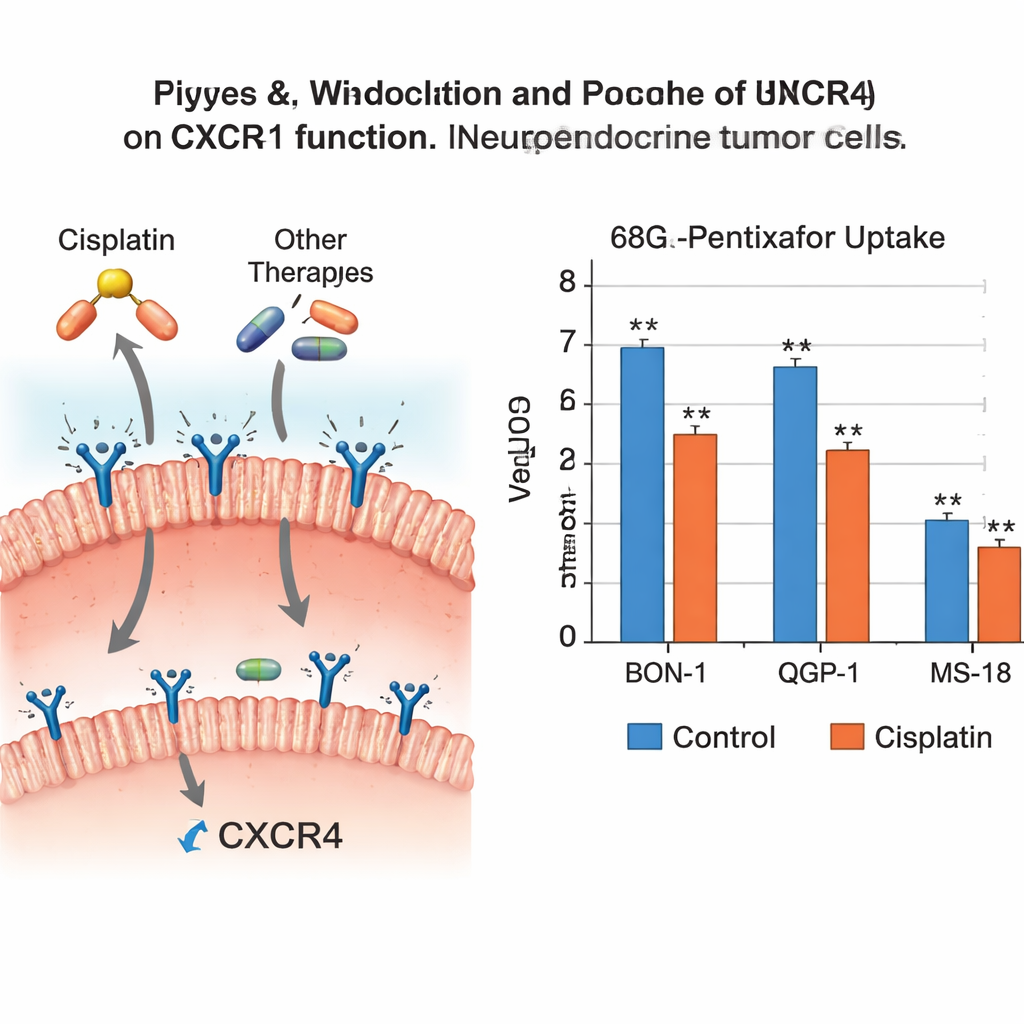
Folgen für Bildgebung und Zeitpunkt der Behandlung
Diese Befunde haben eine doppelte Bedeutung für die Patientenversorgung. Einerseits kann die Dämpfung von CXCR4 Teil der Wirkmechanismen von Cisplatin, Temozolomid und Everolimus sein, durch die das Tumorwachstum und die Metastasierung gebremst werden, da hohe CXCR4-Werte mit Invasivität und Streuung verbunden sind. Andererseits können anhaltende Behandlungen, die CXCR4 unterdrücken, dazu führen, dass CXCR4-basierte PET-Scans das Ausmaß der Erkrankung unterschätzen und CXCR4-gerichtete radioaktive Therapien weniger Andockstellen vorfinden. Die Studie legt nahe, dass eine gleichzeitige Kombination von CXCR4-gerichteten Behandlungen mit diesen systemischen Medikamenten kaum dazu führen wird, dass die CXCR4-Fokussierten Therapien besser wirken — sie könnte diese vielmehr abschwächen.
Ein neues Puzzleteil für personalisierte Therapie
Für Nicht-Fachleute ist die zentrale Erkenntnis: Ein Tumormarker kann gleichzeitig zwei Rollen spielen — er kann ein Warnsignal für aggressives Verhalten sein und zugleich ein nützlicher Ansatzpunkt für Bildgebung und gezielte Behandlung. Diese Forschung zeigt, dass etablierte Krebsmedikamente diesen Marker leise nach oben oder unten regulieren können. Praktisch kann das beeinflussen, wann CXCR4-basierte Scans und Therapien geplant werden sollten — idealerweise dann, wenn der Rezeptor am stärksten exprimiert ist — und helfen zu erklären, warum bestimmte Behandlungen bei schnell wachsenden neuroendokrinen Tumoren wirksam sind. Zwar stammen die Ergebnisse aus Zellmodellen und müssen an Patientinnen und Patienten bestätigt werden, sie stellen aber einen wichtigen Schritt in Richtung klügerer Abfolge von Therapien für Menschen mit diesen schwierigen Tumoren dar.
Zitation: Däubler, C., Böttcher, C., Landwehr, LS. et al. Impact of neuroendocrine neoplasm-specific systemic treatments on expression and function of CXCR4 in neuroendocrine tumor cells. Sci Rep 16, 4339 (2026). https://doi.org/10.1038/s41598-026-37026-8
Schlüsselwörter: neuroendokrine Tumoren, CXCR4, Cisplatin, Everolimus, zielgerichtete Bildgebung