Clear Sky Science · de
Ein entwickelter M13-Phagen–rGO elektrochemischer Biosensor zur schnellen Erkennung von Virusprotein in komplexen Matrizes
Warum schnelle Virustests weiterhin wichtig sind
Die COVID-19-Pandemie machte deutlich, wie wichtig es ist, Viren schnell zu erkennen — nicht nur bei Patienten, sondern auch an Orten wie Abwässern und in Lebensmittelverarbeitungsanlagen. Heutige Labortests sind leistungsfähig, können aber langsam, teuer und abhängig von empfindlichen biologischen Komponenten sein, die schwer zu transportieren und zu lagern sind. Diese Studie stellt eine neue Art winzigen elektronischen Sensors vor, der gentechnisch veränderte Phagen und eine Schicht aus fortschrittlichem Kohlenstoffmaterial nutzt, um ein Schlüsseloron des SARS-CoV-2-Spike-Proteins in unter einer Sekunde zu erkennen, selbst in unordentlichen Realproben wie Blutserum, Milch und Abwasser.
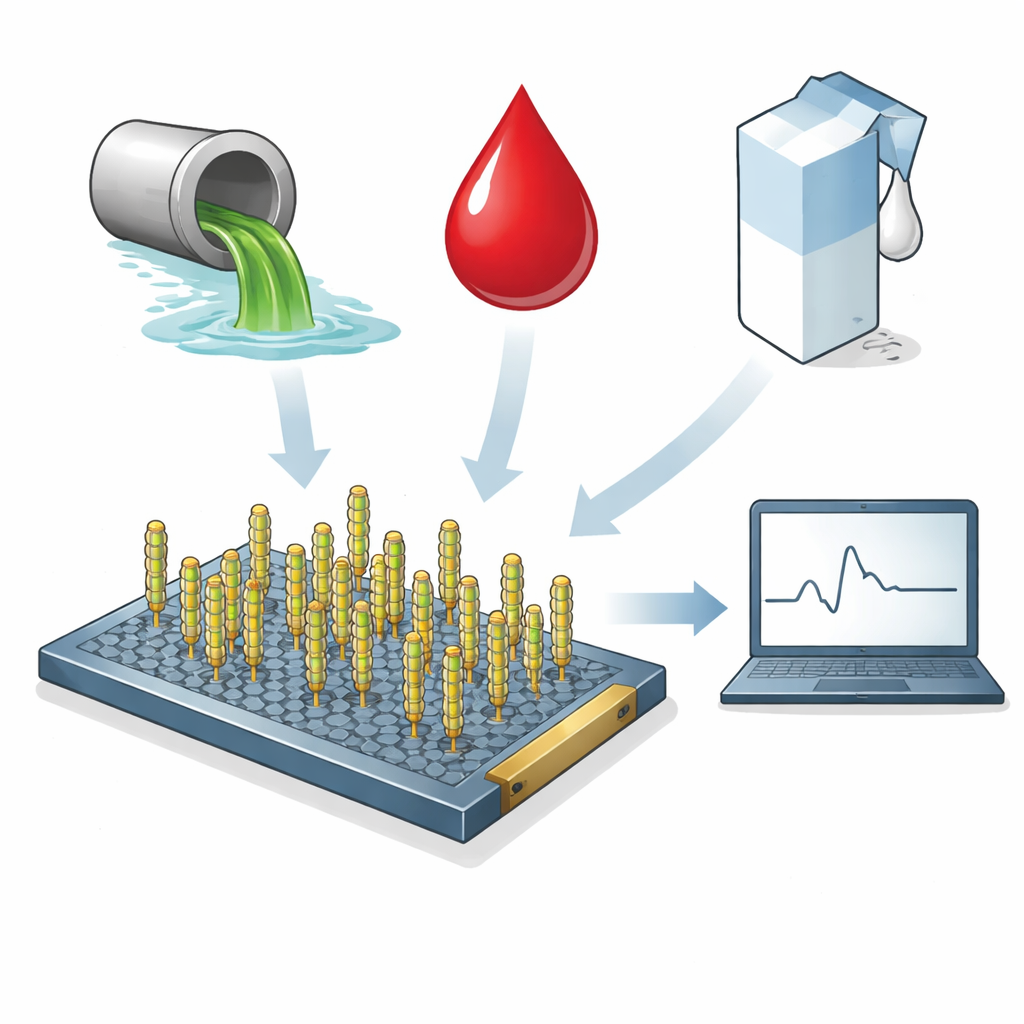
Aus einem harmlosen Virus einen intelligenten Detektor machen
Im Zentrum des Geräts steht M13, ein harmloser Phage, der normalerweise Bakterien befällt. Sein langer, stabförmiger Körper ist mit vielen identischen Hüllproteinen bedeckt, die sich genetisch umprogrammieren lassen. Das Team fügte eines dieser Proteine ein kurzes, maßgeschneidertes Peptid hinzu, damit die M13-Partikel das S1-Fragment des Coronavirus-Spike-Proteins erkennen und daran andocken. Eine zweite Version des Phagen mit einem verschlüsselten (scrambled) Peptid diente als Kontrolle, um zu zeigen, dass die Reaktion von echter Erkennung und nicht von zufälligem Anhaften herrührt.
Auf einer Blase aus atomdünnem Kohlenstoff aufbauen
Um den programmierbaren Phagen in einen Sensor zu verwandeln, befestigten die Forschenden ihn an einer flachen Schicht aus reduziertem Graphenoxid, einer hochleitfähigen Kohlenstoffform, die durch chemische Behandlung von Graphit hergestellt wird. Nachdem Graphenoxid auf kleine Glaschips aufgetragen und erhitzt worden war, um es in reduziertes Graphenoxid umzuwandeln, fügten sie ein Linkermolekül hinzu, das an die Kohlenstoffoberfläche haftet und gleichzeitig an Aminogruppen des Phagen bindet. So entstand eine dichte Schicht von M13-Partikeln, die auf der leitfähigen Fläche verankert sind. Elektronenmikroskopie und Rasterkraftmikroskopie bestätigten, dass jeder Fertigungsschritt die Oberfläche wie erwartet veränderte, und elektrische Messungen zeigten, dass das Hinzufügen des Linkers und anschließend des Phagen den Widerstand stetig erhöhte — ein Hinweis darauf, dass die Oberfläche erfolgreich beschichtet wurde.
Virusbindung als elektrischen Impuls ablesen
Im Gegensatz zu vielen Biosensoren, die zusätzliche Chemikalien oder bewegliche Teile brauchen, funktioniert diese Plattform als einfacher Widerstand unter einer sehr kleinen konstanten Spannung. Wenn das S1-Protein auf die mit Phagen bedeckte Oberfläche trifft und an das präsentierte Peptid bindet, verändert das leicht, wie Ladung durch die Graphenschicht fließt. Das zeigt sich als kurzer Ausreißer im elektrischen Strom, der ungefähr 300 Millisekunden nach Aufbringen eines Tropfens Probe auf den Chip erscheint und dann wieder abklingt, während sich das System beruhigt. Durch Feinabstimmung der angelegten Spannung fand das Team einen optimalen Punkt bei etwa minus 0,8 Millivolt, an dem das Signal echter S1-Bindung stark war, während Hintergrundrauschen und Reaktionen auf nicht verwandte Proteine wie bovines Serumalbumin gering blieben.
Arbeiten in unordentlichen Realproben
Die Forschenden setzten den Sensor dann den Arten komplexer Gemische aus, die empfindliche Laborreagenzien oft überfordern. Sie testeten das Gerät in Pufferlösung, kommunalem Abwasser, fetalem Kälberserum (als Ersatz für Blut) und pasteurisierter Milch, jeweils mit und ohne zugesetztes S1-Protein. Mit einer statistisch definierten Cutoff-Schwelle für ein positives Ergebnis detektierte der Sensor extrem niedrige Proteinkonzentrationen in einfachem Puffer — bis zu etwa 10⁻⁴ Pikogramm pro Milliliter — vergleichbar mit oder besser als viele antibodybasierte Systeme. Im Abwasser markierte das Gerät zuverlässig höhere S1-Werte, während es in Serum und Milch auch niedrigere Konzentrationen konsistent erkannte, jeweils in Bruchteilen einer Sekunde. Wichtig ist, dass ein Kontrollsensor mit dem verschlüsselten Phagen nur wenig auf S1 ansprach, was bestätigt, dass das Signal von der konstruierten Bindungssequenz abhängt. Ein paralleler Sensor mit einem konventionellen Antikörper auf derselben Graphenplattform zeigte ähnliche Leistung, was darauf hindeutet, dass das phagenbasierte System die Sensitivität von Antikörpern erreichen kann, dabei potenziell günstiger und leichter herzustellen ist.

Was das für alltägliche Tests bedeuten könnte
Antikörper, die Arbeitspferde vieler Diagnostika, sind teuer in der Herstellung, hitzeempfindlich und erfordern meist durchgehende Kühlung von der Fabrik bis zur Klinik. Im Gegensatz dazu lassen sich M13-Phagen in Bakterien wie einer einfachen Kultur züchten, tolerieren rauere Bedingungen und lassen sich durch Umschreiben ihres genetischen Codes umprogrammieren. Indem diese Robustheit und Flexibilität mit einer schnellen, stromsparenden elektronischen Auslesung auf Graphen verbunden wird, skizziert die Studie einen Weg zu tragbaren, kostengünstigen Geräten, die an verschiedene Krankheitsmarker oder Kontaminanten angepasst werden könnten, indem einfach das präsentierte Peptid ausgetauscht wird. Die Arbeit befindet sich noch im Proof-of-Concept-Stadium und wurde noch nicht an menschlichen klinischen Proben getestet, weist aber auf eine Zukunft hin, in der handliche Sensoren virale Proteine und andere Biomarker in Kliniken, Abwassersystemen oder sogar Lebensmittelprodukten innerhalb von Sekunden erfassen könnten, ohne die logistischen Anforderungen traditioneller antibodybasierter Tests.
Zitation: Alshehhi, H.Y., Tizani, L., Palanisamy, S. et al. An engineered M13 phage–rGO electrochemical biosensor for rapid detection of viral protein in complex matrices. Sci Rep 16, 9279 (2026). https://doi.org/10.1038/s41598-026-37008-w
Schlüsselwörter: Biosensor, Graphen, Bakteriophage, SARS-CoV-2, elektrochemische Detektion