Clear Sky Science · de
Amplicon-Sequenzierung mit Oxford-Nanopore-Technologien als diagnostische Alternative für kleine Wiederkäuer-Lentiviren bei Schafen
Versteckte Infektionen in alltäglichen Schafbeständen
Weltweit tragen Schafe oft stillschweigend Viren in sich, die ihre Gesundheit schwächen, ihr Leben verkürzen und den Landwirten Geld kosten können — häufig über Jahre hinweg ohne deutliche Symptome. Diese Studie untersucht einen neuen Weg, solche verborgenen Infektionen mit Hilfe einer tragbaren DNA-Sequenzierungstechnologie aufzuspüren und damit einen möglichen Paradigmenwechsel beim Schutz des Tierwohls, der Hofeinnahmen und sogar der Ernährungssicherheit anzustoßen.
Eine langsame, kostspielige Krankheit, die schwer zu erkennen ist
Die Arbeit konzentriert sich auf kleine Wiederkäuer-Lentiviren (SRLV), eine Gruppe von Viren, die Schafe und Ziegen infizieren. Beim Schaf verursachen sie die Maedi-Visna-Krankheit, eine lang anhaltende Infektion, die zu Atemproblemen, Arthritis, Gehirnerkrankungen und chronischer Euterentzündung führen kann. Viele infizierte Tiere zeigen niemals klare Hinweise, dennoch reduziert das Virus die Milchleistung, erhöht die Lammverluste und führt zu frühzeitigem Schlachtfall. In einigen europäischen Milchherden, etwa in Spanien und Griechenland, können rund die Hälfte der Tiere infiziert sein, was diese Krankheit zu einer der wichtigsten in intensiv bewirtschafteten Schafbeständen macht.
Warum aktuelle Tests viele Infizierte übersehen
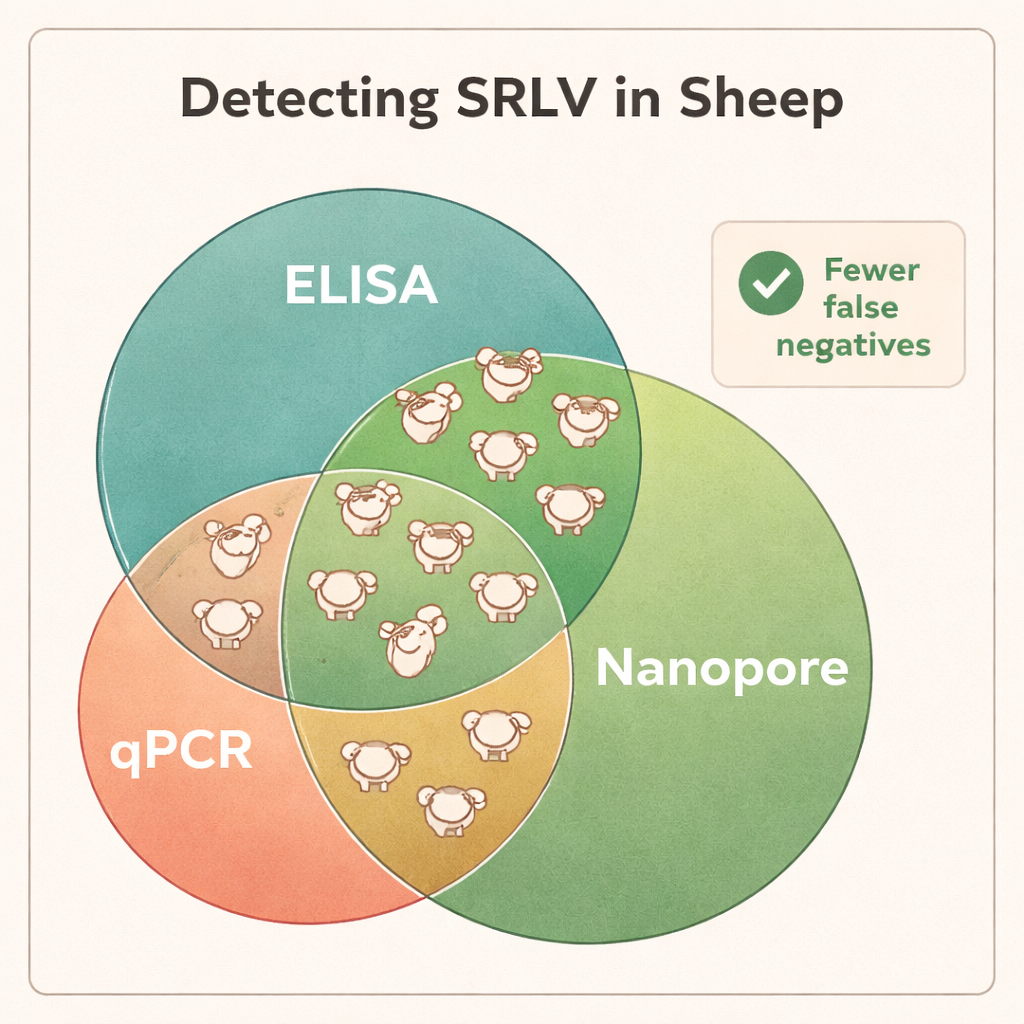
Derzeit verlassen sich Betriebe vorwiegend auf Bluttests, die nach Antikörpern suchen (ELISA), oder auf standardmäßige DNA-Tests (qPCR), um zu entscheiden, welche Tiere infiziert sind und aus der Herde entfernt werden sollten. SRLVs mutieren und rekombinieren jedoch schnell und erzeugen zahlreiche leicht unterschiedliche Virusvarianten. Einige Varianten werden von Antikörpertests nur schwach erkannt, und manche infizierten Schafe entwickeln überhaupt keine starken Antikörperantworten. qPCR, die sehr kurze und spezifische Abschnitte der viralen DNA anvisiert, kann ebenfalls versagen, wenn sich diese Zielregionen verändern. Folglich testen viele tatsächlich infizierte Tiere negativ und verbleiben in der Herde, wo sie das Virus weiterverbreiten.
Echtzeit-DNA-Lesen, um das Virus zu finden
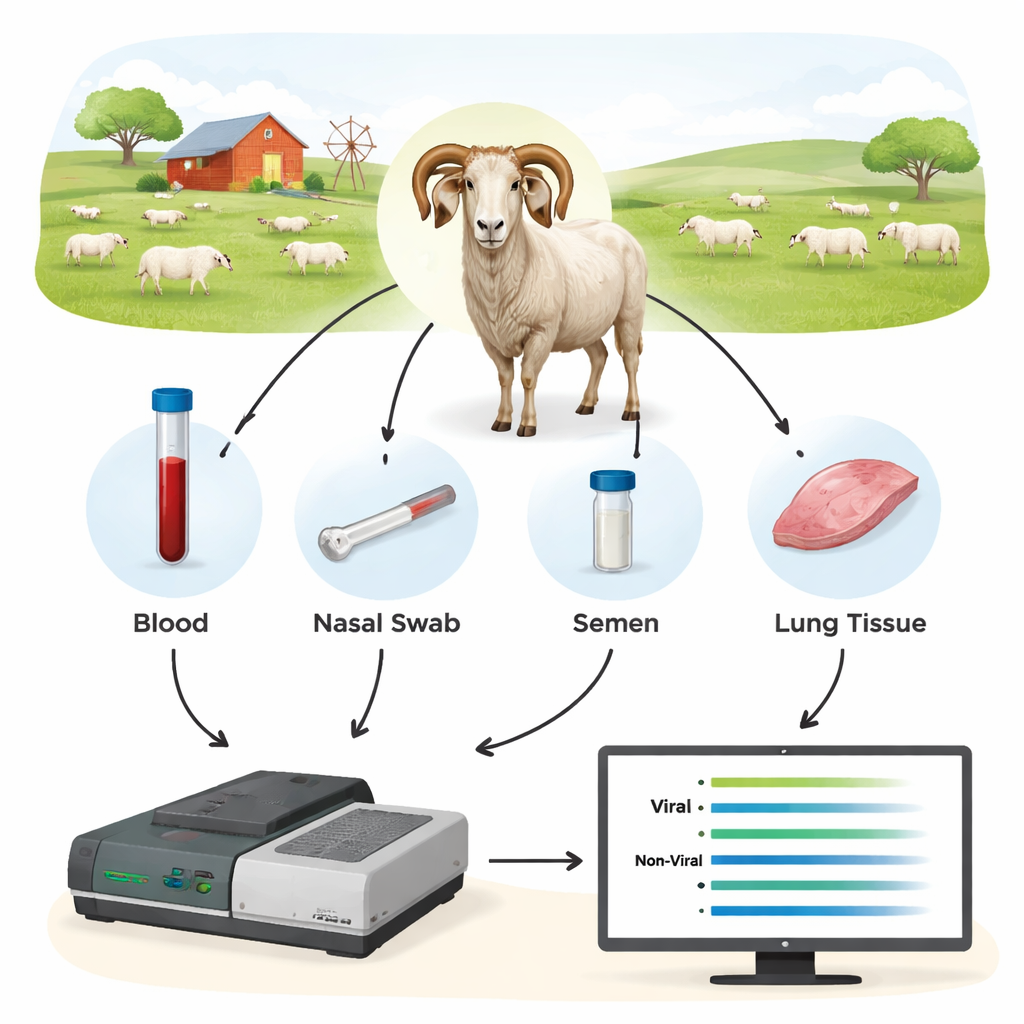
Die Forscher testeten eine Drittgenerations-DNA-Methode namens Oxford Nanopore-Sequenzierung als neue Art diagnostischen Werkzeugs. Anstatt nach einem einzigen, winzigen Stück viraler DNA zu suchen, amplifizierten sie zunächst längere Abschnitte wichtiger Virusgene aus den Proben der Tiere und sequenzierten diese Fragmente dann in Echtzeit auf einem Nanopore-Gerät. Sie sammelten Blut, Nasenabstriche, Samen sowie Zellen aus Blut und Lunge von 44 Widdern und weiteren Schafen, von denen viele bereits mit herkömmlichen Methoden getestet worden waren. Indem sie sich auf virale Regionen konzentrierten, die relativ konserviert, aber dennoch lang genug sind, um den genauen Stamm zu erkennen, konnten die Wissenschaftler sowohl eine Infektion nachweisen als auch bestimmen, welche Virustypen vorhanden waren.
Blut funktioniert am besten — und findet, was andere Tests übersehen
Die Sequenzierung zeigte, dass DNA aus Vollblut das verlässlichste Material zur Entdeckung von SRLV war, obwohl das Virus hauptsächlich in einer kleinen Untergruppe weißer Blutzellen lebt. Lungengewebe stark infizierter Tiere lieferte sehr hohe Mengen viraler DNA, doch solche Proben sind nur nach der Schlachtung verfügbar. Im Gegensatz dazu boten Nasenabstriche, Samen und gereinigte weiße Blutkörperchen zu wenig virales Material für eine konsistente Diagnose. Beim Vergleich der Nanopore-Ergebnisse mit den Standardtests ELISA und qPCR waren die Unterschiede auffällig: Die Nanopore-Sequenzierung bestätigte Infektionen bei allen ELISA-positiven Widdern, zeigte aber gleichzeitig, dass viele ELISA-negative Tiere tatsächlich infiziert waren. In verschiedenen Herden stellten sich etwa 40–45 % der per ELISA als „negativ“ eingestuften Tiere als Virusträger heraus, und qPCR übersah einen noch größeren Anteil. Die Sequenzierungsdaten deckten zudem Koinfektionen mit unterschiedlichen SRLV-Typen in einigen Widdern auf — Informationen, die traditionelle Tests nur schwer liefern können.
Von einfachen Ja/Nein-Antworten zu tieferen Einblicken
Weil Nanopore die tatsächlichen Virussequenzen liest, kann die Methode über eine einfache Ja-oder-Nein-Diagnose hinausgehen. Das Team nutzte die Daten, um Virusstämme zu vergleichen, Stammbäume der in ihren Herden zirkulierenden Viren zu erstellen und subtile Unterschiede in viralen Proteinen zu untersuchen, die erklären könnten, warum manche Tiere von Standard-ELISA-Tests unentdeckt bleiben. Sie zeigten, dass bestimmte Varianten eines Schlüsselvirusproteins, das von kommerziellen Antikörpertests anvisiert wird, sich deutlich zwischen Antikörper-positiven und -negativen Tieren unterscheiden. Solche Informationen könnten mit der Zeit helfen, sowohl serologische Tests als auch Zuchtprogramme zu verfeinern, die auf die Auswahl natürlich resistenter Tiere abzielen.
Was das für Landwirte und Tiergesundheit bedeutet
Für Nicht-Expertinnen und Nicht-Experten ist die Kernbotschaft klar: Indem längere Abschnitte viraler DNA direkt gelesen werden, kann die Nanopore-Sequenzierung mehr infizierte Schafe früher und genauer aufspüren als die derzeit üblichen Routinetests. Sie liefert außerdem Auskunft darüber, welche genauen Virusstämme in einer Herde vorkommen. Obwohl dieser Ansatz noch komplexer und teurer ist als ein einzelner Bluttest, wird die Technologie schneller, günstiger und portabler. Integriert in Kontrollprogramme könnte sie die Zahl der „versteckten“ Träger deutlich reduzieren, die Entwicklung von Impfstoffen und Tests verbessern und die Zucht widerstandsfähiger Tiere unterstützen — wodurch die Schafhaltung nachhaltiger und tiergerechter würde.
Zitation: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
Schlüsselwörter: Schafgesundheit, Lentivirus, Nanopore-Sequenzierung, veterinärdiagnostik, Maedi-Visna