Clear Sky Science · de
Breitband-antimikrobielle Nanopartikel mit geringer Toxizität zur Verhinderung von Biofilmbildung auf urologischen Geräten
Warum medizinische Implantate manchmal gegen uns arbeiten
Die moderne Medizin ist auf Kunststoffschläuche und Implantate angewiesen, um Urin abzuleiten, blockierte Nieren zu entlasten und die sexuelle Funktion wiederherzustellen. Dieselben Geräte können jedoch zu Magneten für Bakterien werden, die schleimige Schutzgemeinschaften bilden, sogenannte Biofilme. Sobald sich ein Biofilm ausgebildet hat, sind Infektionen schwer zu behandeln, und oft müssen Ärzte das Gerät entfernen oder austauschen. In dieser Studie wird eine neue Art mikroskopischer Beschichtung untersucht, bestehend aus Gold und Silber in einer Kohlenstoffhülle, die darauf abzielt, Biofilme bereits im Ansatz zu verhindern.
Das verborgene Problem der klebrigen Keime
Katheter, Ureterenstents und aufblasbare Penisprothesen helfen Hunderttausenden von Patienten, bieten aber gleichzeitig ideale „Wohnfläche“ für Mikroben. Bakterien setzen sich an der Geräteoberfläche fest und sezernieren eine klebstoffartige Matrix aus Zuckern, Proteinen und Fetten, die eine Festung bildet und sie vor Antibiotika und dem Immunsystem schützt. Infolgedessen machen geräteassoziierte Infektionen mehr als ein Viertel aller nosokomialen Infektionen aus und kosten jährlich Hunderte Millionen Dollar. Aktuelle Schutzbeschichtungen auf Basis von Antibiotika oder einfachem Silber haben Schwierigkeiten, Biofilme langfristig zu verhindern, und können zur Zunahme von Antibiotikaresistenzen beitragen.
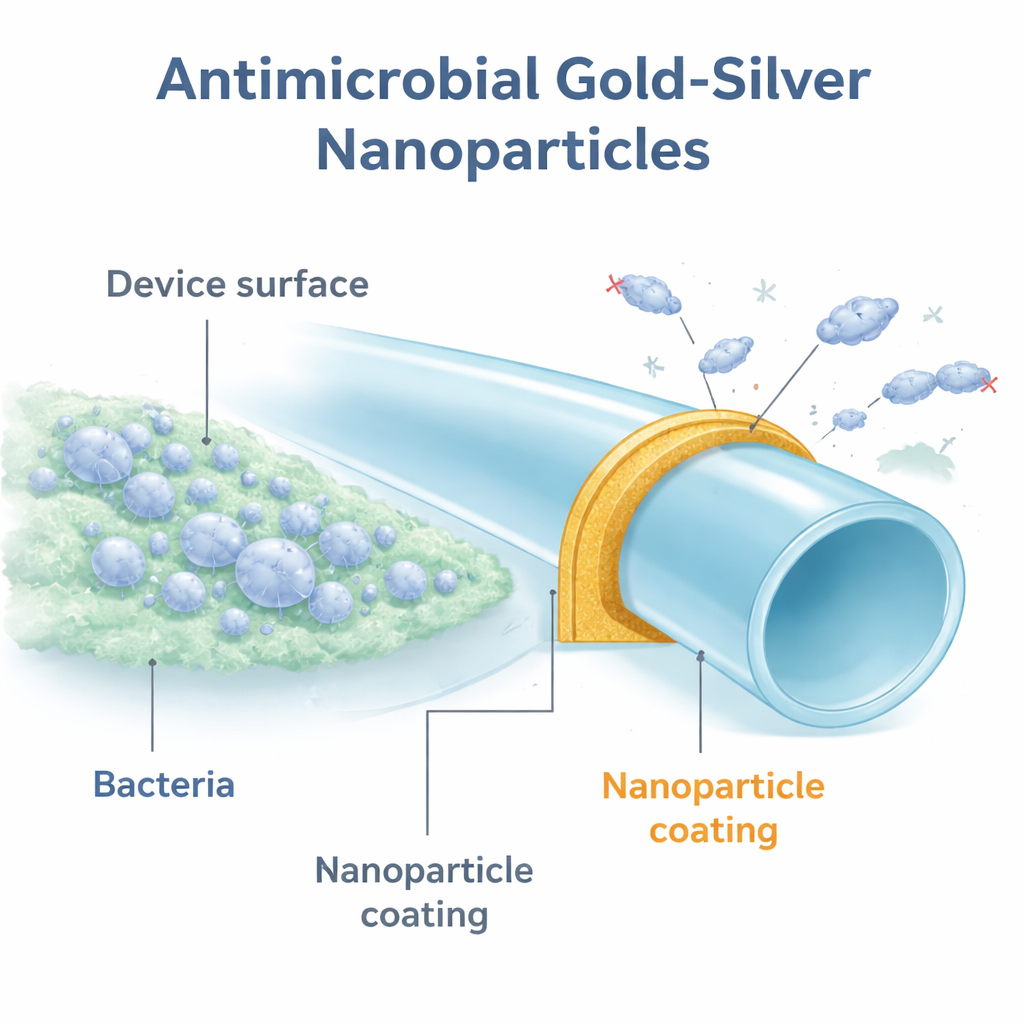
Eine neue Art von Schutzpanzer
Die Forschenden konzentrierten sich auf winzige Metallpartikel von nur wenigen Milliardsteln eines Meters Durchmesser. Diese Nanopartikel wurden um ein Kohlenstoffkäfigmaterial namens Polyhydroxy-fulleren aufgebaut, das als wenig toxisch gilt und die Leistung bestimmter Metalle verbessern kann. Es wurden mehrere Varianten mit unterschiedlichen Metallen hergestellt und kleine Scheiben aus Polyurethan, einem in urologischen Geräten häufig verwendeten Kunststoff, beschichtet. Bei Tests dieser beschichteten Scheiben gegen einen Standardstamm von Escherichia coli zeigten nur die silberhaltigen Partikel starke antibakterielle Effekte. Der klare Favorit war eine Gold–Silber-Kombination, bezeichnet als GSNPs, die die Bakterienzahl im Vergleich zu unbeschichtetem Kunststoff um bis zu das 100.000-Fache reduzierte.
Bekämpfung realer urologischer Keime
Um zu prüfen, ob dieser Effekt über einen Laborstamm hinaus Bestand hat, testete das Team ihre beste Beschichtung gegen sechs Bakterienarten, die direkt aus infizierten Ureterenstents und Penisprothesen isoliert wurden. Dazu gehörten sowohl Gram-positive als auch Gram-negative Arten, die für hartnäckige Infektionen bekannt sind. Bei Bakterienzahlen, die denen in Patienten ähneln, erzielten die GSNP-beschichteten Oberflächen für jeden getesteten Stamm eine 100%ige Reduktion sowohl freischwimmender als auch haftender Bakterien. In separaten Experimenten setzten die Forschenden die Bakterien unterschiedlichen Nanopartikelkonzentrationen in Flüssigkeit aus und schätzten, wie viel GSNP nötig ist, um das Wachstum zu stoppen. Alle Stämme wurden bei oder unter 3 Mikrogramm GSNP pro Milliliter vollständig gehemmt, wobei für einige grampositive Organismen geringfügig höhere Mengen erforderlich waren.
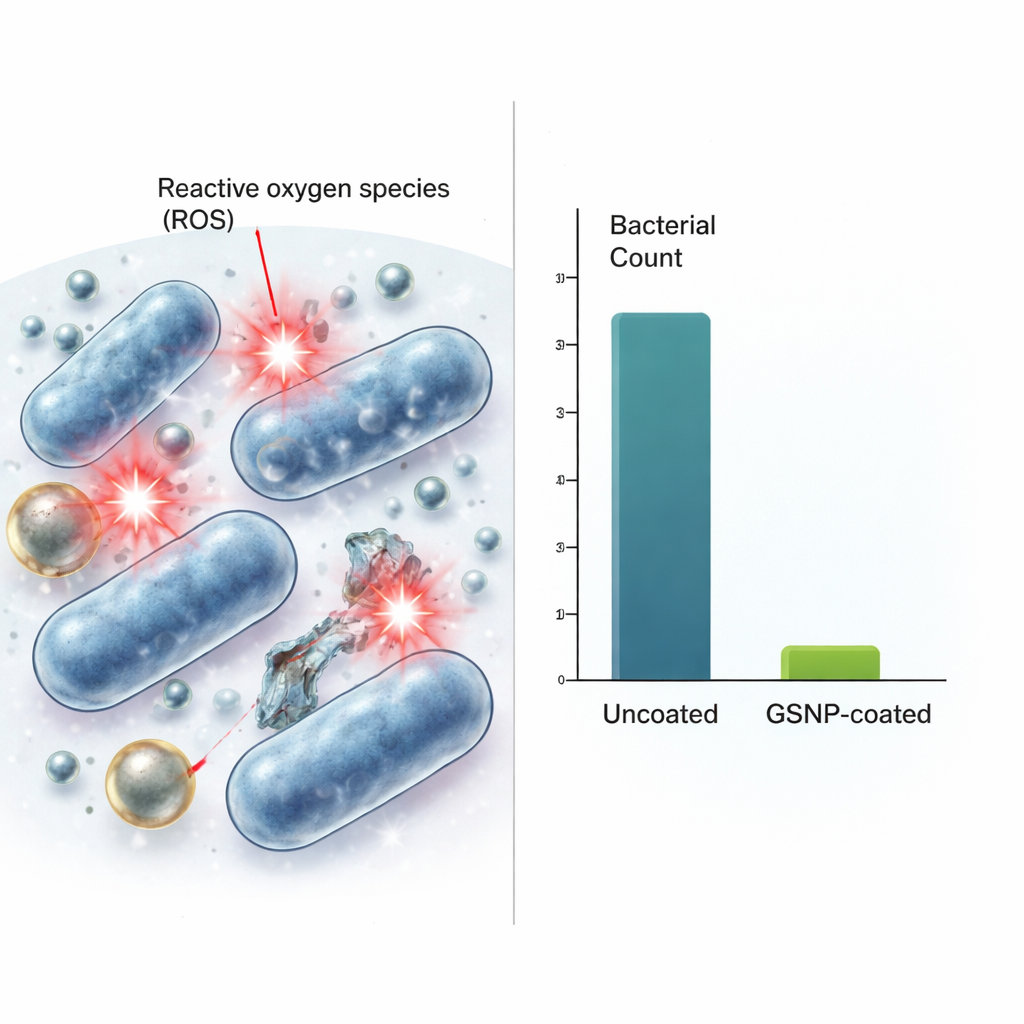
Wie sie wirken und wie sicher sie sind
Als Nächstes untersuchte das Team, wie diese Beschichtungen Bakterien abtöten und ob sie auch menschliche Zellen schädigen könnten. Ihre Daten deuten darauf hin, dass reaktive Sauerstoffspezies—chemisch reaktive Formen von Sauerstoff—ein zentraler Teil des Abtötungsmechanismus sind. Während die Nanopartikel allein diese reaktiven Moleküle nicht erzeugten, produzierten Bakterien, die GSNPs ausgesetzt waren, deutlich höhere Mengen als unbehandelte Bakterien, was darauf hindeutet, dass die Partikel schädliche Chemie innerhalb oder in der Nähe der Mikroben auslösen. Wenn Mausfibroblasten ähnlichen oder höheren GSNP-Konzentrationen ausgesetzt wurden, blieben mehr als 80% der Zellen bei der schlimmsten antibakteriellen Dosis am Leben. Mit anderen Worten: Die Konzentrationen, die Bakterien vernichteten, hatten nur einen moderaten Einfluss auf Säugerzellen. Die GSNPs waren zudem dramatisch wirksamer als ein kommerzielles Gold–Silber-Nanoprodukt, das parallel getestet wurde, und erreichten bei äquivalenten Dosen ungefähr eine Millionfach größere Bakterienreduktion.
Was das für Patienten bedeuten könnte
Obwohl diese Arbeit im Labor durchgeführt wurde und noch nicht an Tieren oder Menschen getestet ist, deuten die Ergebnisse auf eine vielversprechende neue Strategie für sicherere medizinische Implantate hin. Eine dünne Schicht GSNPs auf einem Katheter oder einer Prothese könnte breiten Schutz gegen viele verschiedene Bakterien bieten, den Bedarf an Geräteentfernungen reduzieren und dies ohne den Einsatz traditioneller Antibiotika erreichen. Die Beschichtung verwendet geringe Metallmengen, zeigt in ersten Tests eine relativ geringe Toxizität und ist einfach herzustellen. Mit weiterer Technik zur Verbesserung der Langzeitstabilität und sorgfältigen Tests in realistischen Modellen könnten diese Gold–Silber-Nanopartikel-Beschichtungen dazu beitragen, vitale urologische Geräte für Patienten funktionsfähig zu halten, statt ihnen als Brutstätte für Infektionen zu dienen.
Zitation: Rodriguez-Alvarez, J.S., Xu, Y., Gutierrez-Aceves, J. et al. Broad spectrum antimicrobial nanoparticles with low toxicity to prevent biofilm formation on urologic devices. Sci Rep 16, 7333 (2026). https://doi.org/10.1038/s41598-026-36969-2
Schlüsselwörter: Biofilm, urologische Geräte, antimikrobielle Beschichtung, Nanopartikel, Gold-Silber