Clear Sky Science · de
Quantitative proteomische Analyse des Plasmas nach Remote Ischemic Conditioning bei akutem ischämischem Schlaganfall
Warum das Zusammendrücken eines Arms das Gehirn schützen könnte
Bei einem Schlaganfall durch ein verlegtes Blutgefäß bedroht jeder verlorene Minute der Durchblutung Hirnzellen. Standardbehandlungen zielen darauf ab, die verstopfte Arterie wieder zu eröffnen, doch viele Patientinnen und Patienten kommen zu spät oder sind nicht dafür geeignet. Forschende untersuchen eine überraschend einfache Zusatztherapie: kurzzeitiges Unterbrechen der Durchblutung eines Arms oder Beins mit einer Blutdruckmanschette, eine Methode, die als Remote Ischemic Conditioning (RIC) bezeichnet wird. Diese Studie stellt eine zentrale Frage für die klinische Umsetzung: Was genau verändert RIC im Blut von Schlaganfallpatienten, und könnten diese Veränderungen Hinweise darauf geben, wer am meisten davon profitieren könnte?
Ein sanftes Stresssignal vom Gliedmaßensystem zum Gehirn
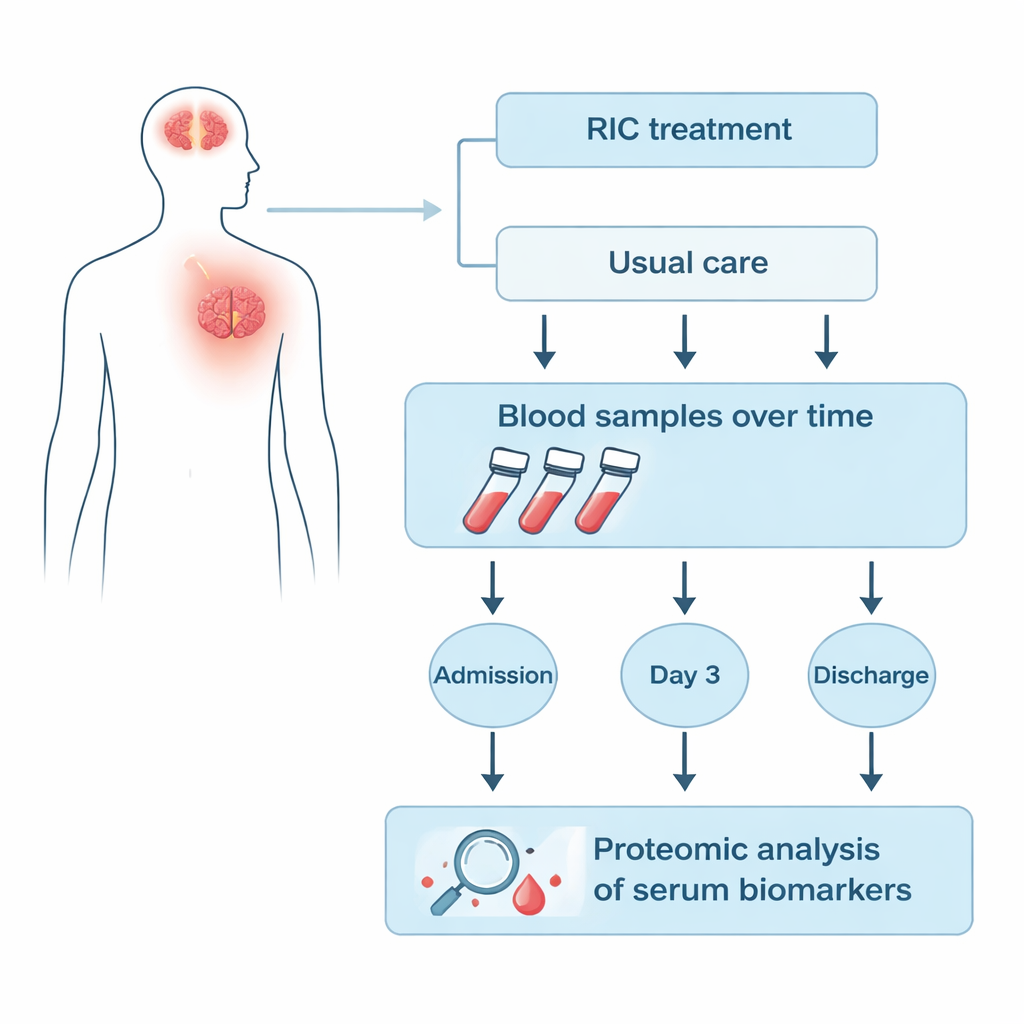
RIC besteht darin, eine Manschette an einer Gliedmaße für einige Minuten mehrmals aufzublasen und wieder zu entleeren, wodurch kurzzeitige, harmlose Phasen verringerter Durchblutung entstehen. Tierexperimente und frühe klinische Studien deuten darauf hin, dass dieses „kontrollierte Stressen“ entfernte Organe, einschließlich des Gehirns, dazu bringen kann, schützende Programme zu aktivieren. In einer großen klinischen Studie namens RICAMIS schnitten Patientinnen und Patienten mit mittelschwerem ischämischem Schlaganfall, die zusätzlich zur üblichen Versorgung RIC erhielten, nach 90 Tagen besser ab als jene mit alleiniger Standardbehandlung. Eine andere Studie (RESIST) zeigte jedoch keinen solchen Nutzen, sodass Ärztinnen und Ärzte unsicher sind, wann und für wen RIC wirklich wirkt. Die vorliegende Studie durchleuchtet das Blut der Patientinnen und Patienten auf molekulare Hinweise — messbare Proteine oder Biomarker, die sich im Zeitverlauf unter RIC verändern.
Den Verlauf des Blutes während des Krankenhausaufenthalts verfolgen
Die Forschenden konzentrierten sich auf 25 Patientinnen und Patienten aus der RICAMIS-Studie, bei denen Blutproben zu drei Zeitpunkten entnommen wurden: bei Aufnahme, drei Tage nach Zuteilung der Behandlung und bei Entlassung. Neun Patienten erhielten RIC plus Standardversorgung, sechzehn erhielten nur die Standardversorgung. Mit einer Methode namens quantitative Proteomik maß das Team Hunderte von Proteinen im Serumanteil des Bluts gleichzeitig, statt nur wenige vorgewählte Marker zu betrachten. Anschließend verglichen sie, wie die Konzentration jedes Proteins im Verlauf bei der RIC-Gruppe gegenüber der Kontrollgruppe anstieg oder sank, um Signaturen zu finden, die spezifisch mit RIC verknüpft sind.
Neun markante Signale im Blutkreislauf
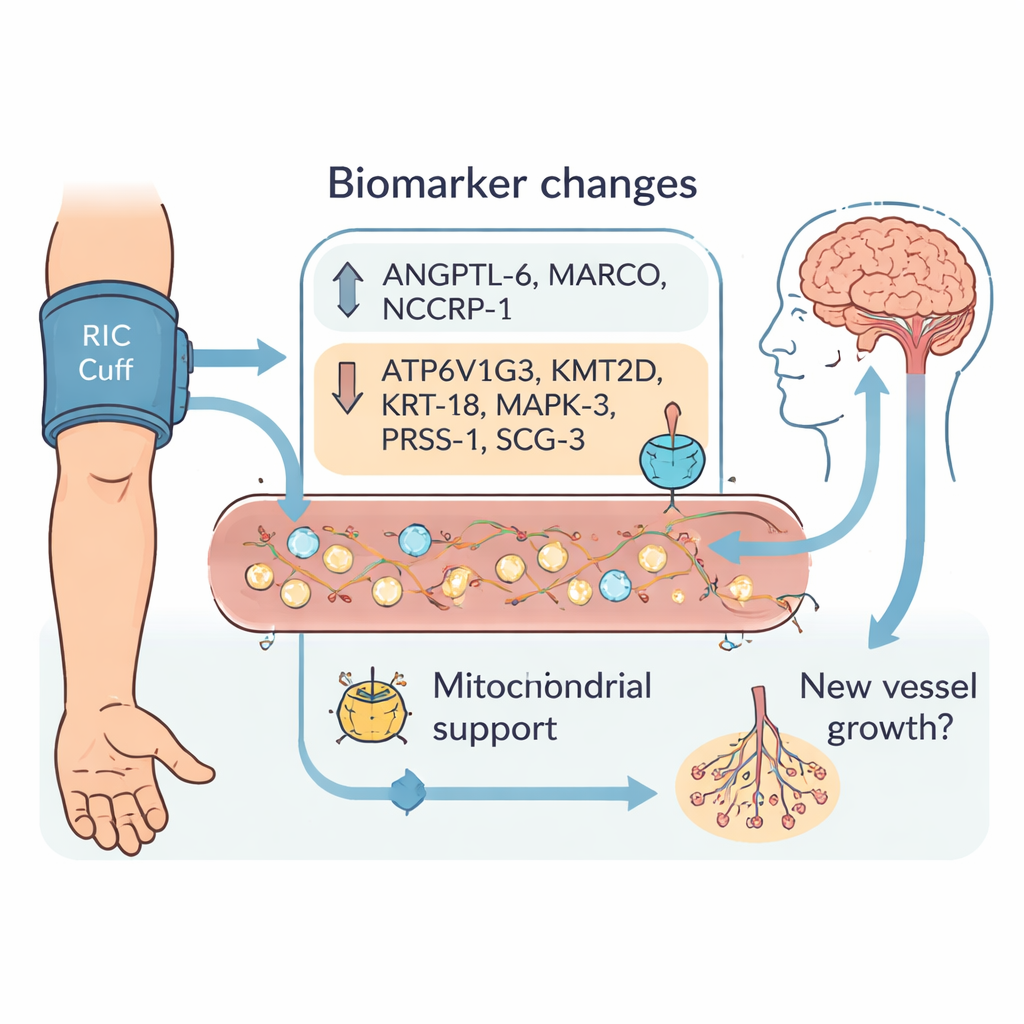
Im Verlauf des Krankenhausaufenthalts veränderten sich Dutzende Proteine unterschiedlich zwischen den beiden Gruppen. Nach sorgfältiger Filterung hob das Team neun Biomarker hervor, deren Veränderungen von der Aufnahme bis Tag 3 und bis zur Entlassung die RIC-behandelten Patientinnen und Patienten klar von den Kontrollen unterschieden. Drei Proteine — ANGPTL-6, MARCO und NCCRP-1 — erhöhten sich stärker unter RIC. Sechs weitere — ATP6V1G3, KMT2D, KRT-18, MAPK-3, PRSS-1 und SCG-3 — neigten dazu, abzunehmen. Viele dieser Moleküle sind an der Energieverwaltung in den zellulären Kraftwerken, den Mitochondrien, oder an der Bildung und Umgestaltung neuer Blutgefäße beteiligt. Das passt zu der Vorstellung, dass RIC nicht nur Neuronen vor Schaden schützt, sondern verletzten Hirnregionen bei der Reorganisation, der Wiederherstellung der Blutversorgung und der funktionellen Erholung über Tage bis Wochen helfen kann.
Hinweise auf Energieverbrauch und Gefäßneubildung
Um besser zu verstehen, welche Funktionen diese neun Proteine haben könnten, ordneten die Autorinnen und Autoren sie bekannten biologischen Signalwegen zu. Zwei davon, KMT2D und MAPK-3, stehen in Verbindung mit der Verpackung von DNA und der Ein-/Ausschaltung von Genprogrammen, insbesondere solchen, die mit Gefäßwachstum zusammenhängen. Andere, wie ATP6V1G3 und KRT-18, wurden in früheren Arbeiten mit der Aufrechterhaltung gesunder Mitochondrien und dem Schutz von Herzgewebe nach Verletzung in Verbindung gebracht. Zusammengenommen deuten diese Muster darauf hin, dass RIC den Körper in Richtung effizienterer Energienutzung lenkt und das Wachstum oder die Umgestaltung von Blutgefäßen fördert — was die Durchblutung im Bereich der durch den Schlaganfall geschädigten Areale verbessern könnte. Gleichzeitig spiegeln einige Marker, etwa NCCRP-1 und MARCO, möglicherweise die akuten Stress- und Immunantworten des Körpers auf das Aufblasen der Manschette wider und unterstreichen, dass RIC eine komplexe Reaktion des gesamten Organismus auslöst.
Was das für die zukünftige Schlaganfallversorgung bedeutet
Diese kleine explorative Studie kann nicht beweisen, wie RIC das Gehirn genau schützt, und sie umfasste nur 25 Patientinnen und Patienten aus einem einzigen Land, sodass die Befunde in deutlich größeren und vielfältigeren Gruppen bestätigt werden müssen. Dennoch ist die Identifizierung einer kurzen Liste von neun Proteinen, die sich mit und ohne RIC beständig in unterschiedliche Richtungen bewegen, ein wichtiger Schritt. Künftig könnten solche Biomarker Ärzten schnell anzeigen, ob RIC bei einer bestimmten Patientin oder einem bestimmten Patienten „wirkt“, die Auswahl der Empfänger steuern oder sogar zu Medikamenten führen, die seine positiven Effekte ohne Manschette nachahmen. Für den Moment stärkt die Arbeit eine einfache, aber kraftvolle Idee: Indem man einen Körperteil sicher stresst, lässt sich das Gehirn möglicherweise in einen widerstandsfähigeren Zustand bringen, der die Heilung nach einem Schlaganfall begünstigt.
Zitation: Cui, Y., Liu, F., Cai, JR. et al. Quantitative proteomic analysis of plasma after remote ischemic conditioning in acute ischemic stroke. Sci Rep 16, 6106 (2026). https://doi.org/10.1038/s41598-026-36968-3
Schlüsselwörter: akuter ischämischer Schlaganfall, remote ischemic conditioning, Serum-Biomarker, proteomische Analyse, Neuroprotektion