Clear Sky Science · de
Proteom- und Phosphoproteom-Analyse mit Orbitrap Astral identifiziert Kandidatenproteine, die mit der Phosphatidsäure-Phosphatase MoPah1 in Magnaporthe oryzae assoziiert sind
Warum ein Enzym bei einer Reiskrankheit wichtig ist
Reis ist Grundnahrungsmittel für Milliarden von Menschen, doch ein einziger mikroskopischer Pilz, Magnaporthe oryzae, verursacht die Reisblastkrankheit, die ganze Felder vernichten kann. Diese Studie untersucht die innere Chemie dieses Pilzes mit Fokus auf ein Enzym, MoPah1, das an der Steuerung von Zellfetten und Signalmolekülen beteiligt ist. Durch das Kartieren von Tausenden Proteinen und ihrer An-/Ausschalter enthüllen die Forschenden, wie dieses Enzym den Grundstoffwechsel mit der Infektionsfähigkeit des Pilzes verbindet.
Ein Pilz, der in Reisblätter eindringt
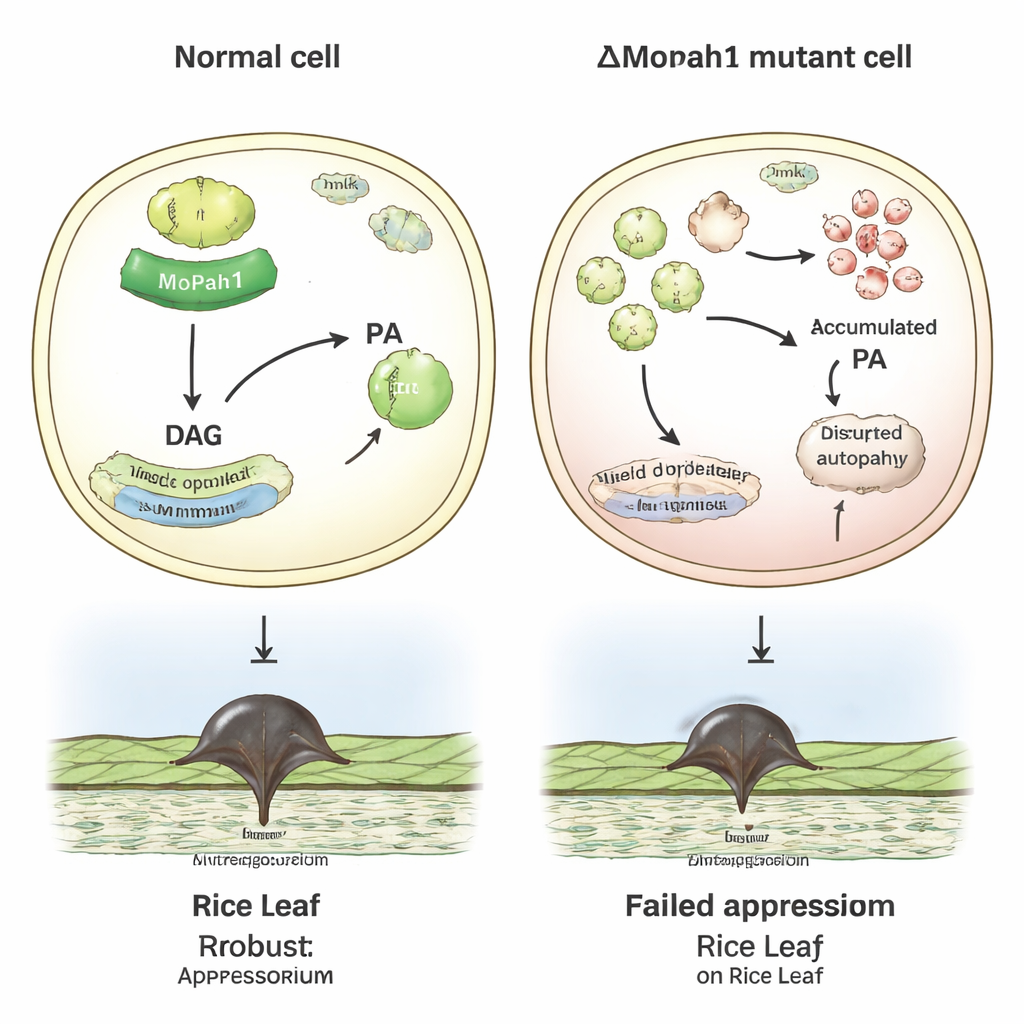
Magnaporthe oryzae infiziert Reisblätter mit einer spezialisierten Struktur, dem Appressorium, das enormen Innendruck aufbaut, um die Blattoberfläche zu durchbohren. Um diesen Vorgang zu ermöglichen, verbrennt der Pilz schnell gespeicherte Zucker und Fette. Frühere Arbeiten zeigten, dass MoPah1 — ein Enzym, das die Fettsäureverbindung Phosphatidsäure in Diacylglycerol umwandelt — für diese Lebensweise entscheidend ist: Entfernt man das MoPah1-Gen, wird der Pilz geschwächt und seine Fähigkeit, Krankheiten zu verursachen, verringert. Welche anderen Proteine jedoch mit MoPah1 verknüpft sind und wie dieses Enzym in breitere zelluläre Netzwerke eingebunden ist, blieb unklar.
Mit Next‑Generation-Proteinabbildung
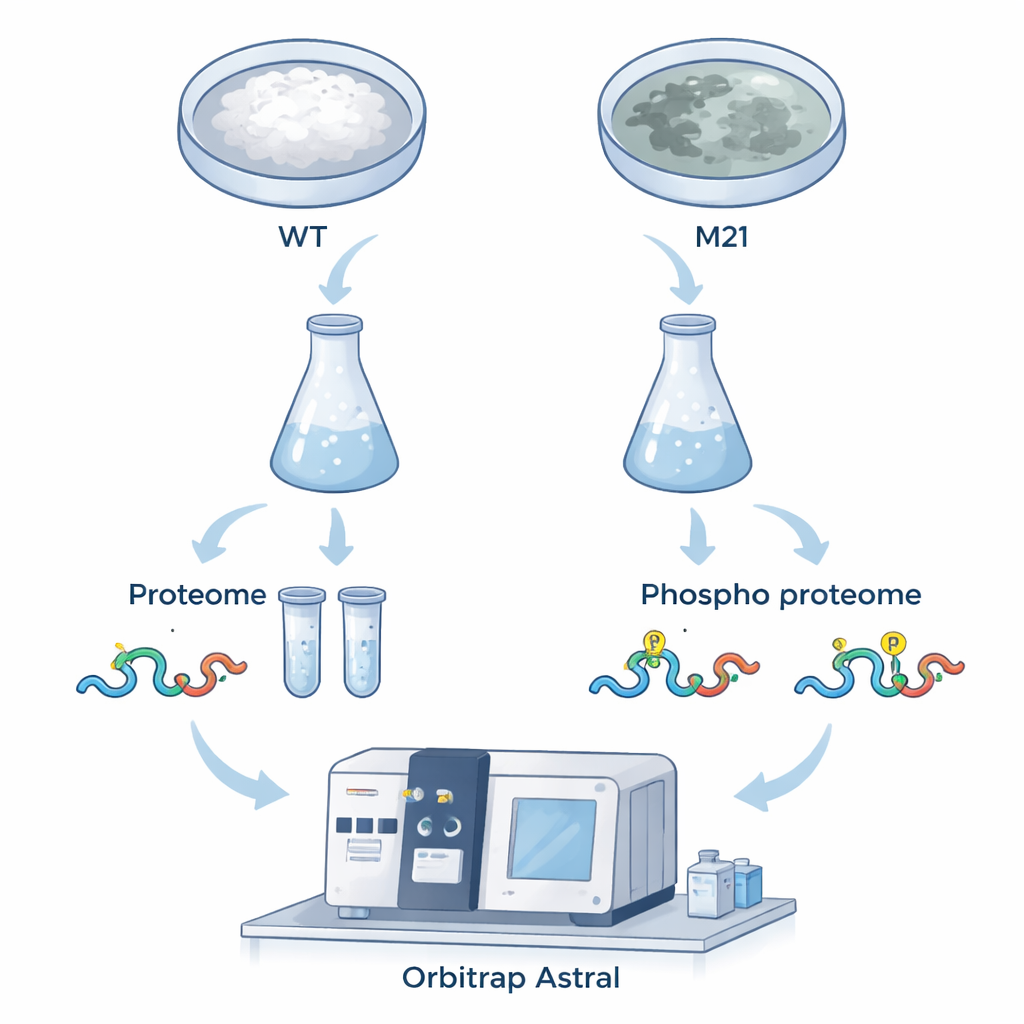
Um diese Fragen zu beantworten, verglich das Team Wildtyp-Pilze mit einem Mutanten ohne MoPah1. Sie konzentrierten sich auf fadenförmiges Wachstum (Myzel), weil der Mutant die normalerweise für Infektionsstudien genutzten Sporen nicht bilden kann. Mit einem hochentwickelten Massenspektrometer, dem Orbitrap Astral, und einer datenunabhängigen Erfassungsstrategie (DIA) maßen sie sowohl die Proteinmengen als auch das Vorkommen von Phosphatmarken, die wie molekulare Schalter wirken. Insgesamt identifizierten sie 6.799 Proteine und mehr als 15.000 Phosphorylierungsstellen, wobei Hunderte im Mutanten deutlich zu- oder abnahmen. Dieser umfangreiche, qualitativ hochwertige Datensatz liefert einen detaillierten Momentaufnahme davon, wie das Entfernen von MoPah1 die Pilzzelle umgestaltet.
Verschiebungen im Energieverbrauch und in der zellulären Wiederverwertung
Als die Forschenden untersuchten, welche Proteintypen sich veränderten, traten zwei Themen besonders hervor: der Stoffwechsel von Membranfetten und ein „Selbstverzehr“-Prozess namens Autophagie, mit dem Zellen Komponenten recyceln und Stress überstehen. Viele Proteine, die an Glycerophospholipiden — den Bausteinen von Zellmembranen — und an verwandten Energiewegen beteiligt sind, waren verändert. Proteine, die mit der Autophagie verbunden sind, zeigten besonders starke Veränderungen in ihren Phosphorylierungsmustern, was darauf hindeutet, dass MoPah1 nicht nur die Fettbildung und -abbau beeinflusst, sondern auch, wie der Pilz während Wachstum und Infektion eigenes Material recycelt. Eine Untergruppe von 72 Proteinen veränderte sich sowohl in der Menge als auch im Phosphorylierungszustand und markiert damit vielversprechende Kandidaten für direkte oder indirekte Regulation durch MoPah1.
MoPah1s Proteinpartner finden
Um über Korrelationen hinauszukommen, fragten die Forschenden, welche Proteine physisch an MoPah1 binden. Sie produzierten ein MoPah1-Protein, das mit einem „Griff“ (GST) in Bakterien fusioniert war, und nutzten es als Köder, um interagierende Proteine aus Pilzextrakten herauszufischen. Die Massenspektrometrie identifizierte 183 Kandidaten, von denen viele in große Proteinkomplexe gruppiert sind, was die Idee stützt, dass MoPah1 im Zentrum umfangreicher zellulärer Netzwerke sitzt. Unter diesen Partnern stach einer hervor: Pmk1, ein Schlüsselprotein der MAPK-Signalbahn, das die Bildung des Appressoriums, das Wachstum im Wirt und Stressantworten steuert. Zusätzliche Hefe-Zwei-Hybrid-Tests bestätigten, dass MoPah1 und Pmk1 direkt interagieren können.
Verknüpfung von Fettkontrolle und Infektionssignalen
Setzt man diese Befunde zusammen, schlagen die Autorinnen und Autoren vor, dass MoPah1 sowohl das Gleichgewicht der Membranfette als auch wichtige Signalwege in Magnaporthe oryzae mitprägt. Bei Pilzen ohne MoPah1 scheinen weitreichende Störungen im Lipidstoffwechsel, im Proteinrecycling und in der MAPK-Signalübertragung die Bildung und Wirksamkeit der für das Eindringen in Reisblätter benötigten Infektionsstrukturen zu untergraben. Obwohl die Studie auf myzeliale Proben beschränkt war — weil der Mutant keine Sporen bildet — liefert sie dennoch eine reichhaltige Ressource an Protein- und Phosphorylierungsdaten sowie eine Kurzliste von Proteinen, die am ehesten mit MoPah1 zusammenarbeiten. Für Nicht-Spezialisten lautet die wichtigste Erkenntnis: Die Kontrolle eines einzelnen Enzyms in einem Pflanzenpathogen kann viele zelluläre Systeme beeinflussen und bietet neue Ansatzpunkte, um den Pilz, der eine der weltweit wichtigsten Nahrungsquellen bedroht, besser zu verstehen und möglicherweise künftig zu bekämpfen.
Zitation: Zhao, J., Yang, L., Shi, X. et al. Orbitrap Astral–based proteome and phosphoproteome analysis identifies candidate proteins associated with the phosphatidate phosphatase MoPah1 in Magnaporthe oryzae. Sci Rep 16, 6901 (2026). https://doi.org/10.1038/s41598-026-36940-1
Schlüsselwörter: Reisblastpilz, Magnaporthe oryzae, Proteinnetzwerke, Lipidstoffwechsel, pilzliche Pathogenität