Clear Sky Science · de
Eine proinflammatorische Neutrophilen‑Subpopulation treibt die intestinale Ischämie‑Reperfusions‑Schädigung über den ATF4‑vermittelten Weg des endoplasmatischen Retikulums‑Stresses
Wenn Blutfluss dem Darm schadet
Chirurgen und Intensivmediziner rätseln seit langem über ein gefährliches Paradoxon: Wenn die Blutversorgung des Darms unterbrochen und anschließend wiederhergestellt wird, kann gerade das Wiederherstellen des Blutflusses die Darmbarriere massiv schädigen. Dieser Prozess, intestinales Ischämie‑Reperfusions‑Schaden genannt, kann zu lebensbedrohlichen Komplikationen wie Sepsis und Multiorganversagen führen. Die hier zusammengefasste Studie zeigt, dass nicht alle eintreffenden Immunzellen gleich sind — eine besonders aggressive Untergruppe von weißen Blutkörperchen spielt eine zentrale Rolle dabei, eine lebensrettende Reaktion in eine schädliche zu verwandeln.
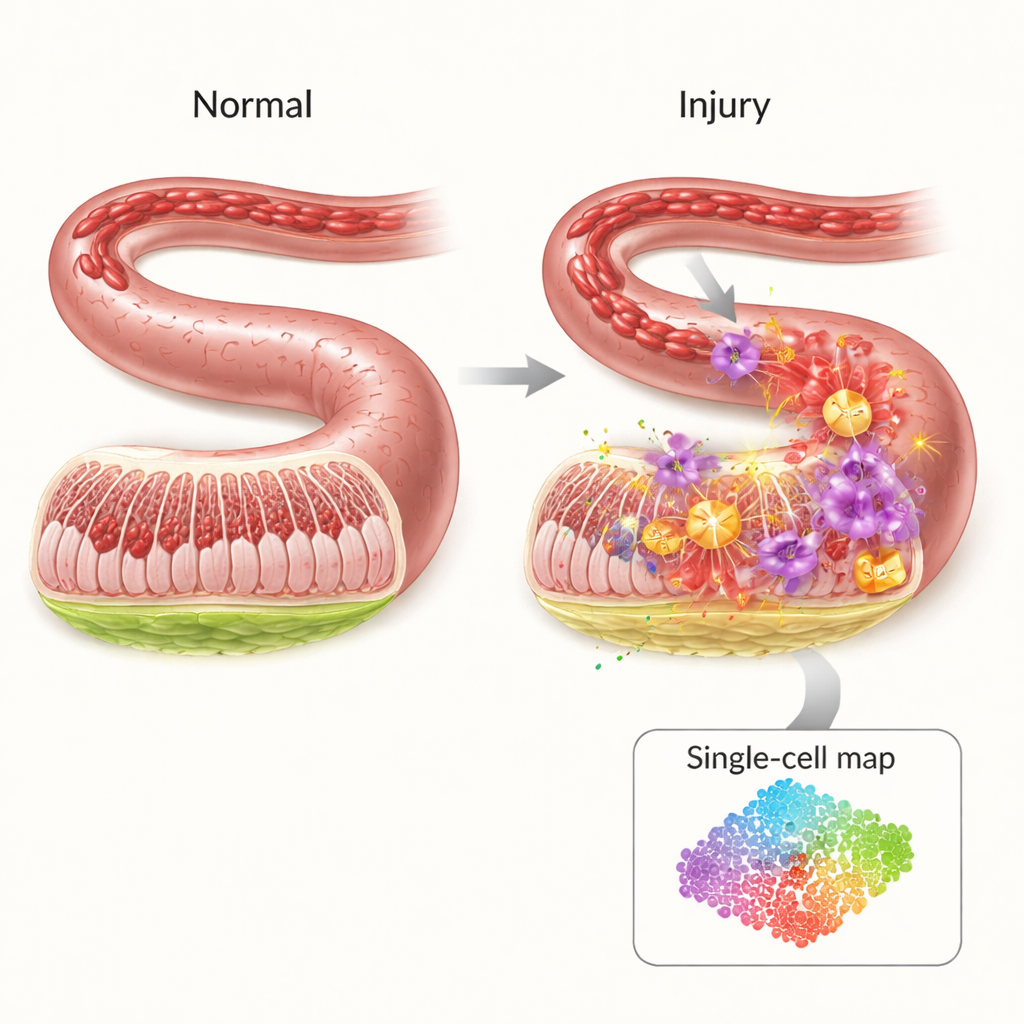
Die fragile Schutzwand des Darms
Die Innenseite des Darms ist von einer dünnen, aber hoch organisierten Barriere ausgekleidet, die Bakterien und Toxine im Darm hält und gleichzeitig den Durchtritt von Nährstoffen erlaubt. Wird die Durchblutung unterbrochen — etwa bei Schock, großen Operationen oder schweren Traumata — wird diese Barriere von Sauerstoff entzogen. Überraschenderweise tritt der größte Teil des Schadens nicht während der Minderdurchblutung selbst auf, sondern wenn die Durchblutung wieder einsetzt. Der plötzliche Zustrom von Sauerstoff und Immunzellen entfacht eine Sturmwelle entzündlicher Signale und reaktiver Moleküle, die Löcher in die Darmwand reißen können, sodass Keime in den Blutkreislauf gelangen. Trotz der klinischen Bedeutung gibt es bislang nur wenige gezielte Behandlungen, die diese Kaskade verhindern.
Einzelzellen unter der Lupe
Um herauszufinden, wer während dieser Krise welche Rolle spielt, nutzten die Forschenden Einzelzell‑RNA‑Sequenzierung, eine Methode, die erfasst, welche Gene in Tausenden einzelner Zellen aktiv sind. In einem Mausmodell der intestinalen Ischämie‑Reperfusion verglichen sie verletzte mit gesunden Darmproben und kartierten 19 große Zelltypen. Sie stellten fest, dass bestimmte Immunzellen — vor allem Neutrophile und inflammatorische Monozyten — nach der Verletzung stark zunahmen, während schützende Zellen wie T‑Zellen, B‑Zellen und natürliche Killerzellen abnahmen. Auch die Kommunikationsnetzwerke zwischen Zelltypen verschoben sich: Neutrophile traten als zentrale Knoten auf, die viele entzündliche Signale senden und empfangen, was sie als Schlüsseltreiber des Schadens ausweist.
Eine schädliche Untergruppe der Ersthelfer
Neutrophile gehören zu den schnellsten Ersthelfern des Körpers und gelangen zügig über den Blutkreislauf, um Infektionen zu bekämpfen und Zelltrümmer zu beseitigen. Diese Studie zeigt jedoch, dass innerhalb der Neutrophilenpopulation eine besonders aggressive Untergruppe für einen Großteil der Kollateralschäden im Darm verantwortlich ist. Wurde bei Mäusen vor Auslösung der Ischämie‑Reperfusion die Neutrophilenzahl reduziert, zeigten die Tiere weniger Darmverkürzung, niedrigere Blutwerte für Schadensmarker, ein besseres Gewebe‑Mikroskopbild und dichtere Versiegelungsproteine in der Darmbarriere. In Ko‑Kultur‑Experimenten schadeten Neutrophile aus verletzten Mäusen intestinalen Zellen direkt: Sie verringerten deren Überleben, erhöhten den Zelltod und störten Schlüssel‑„Reißverschluss“‑Proteine, die die Darmbarriere zusammenhalten.
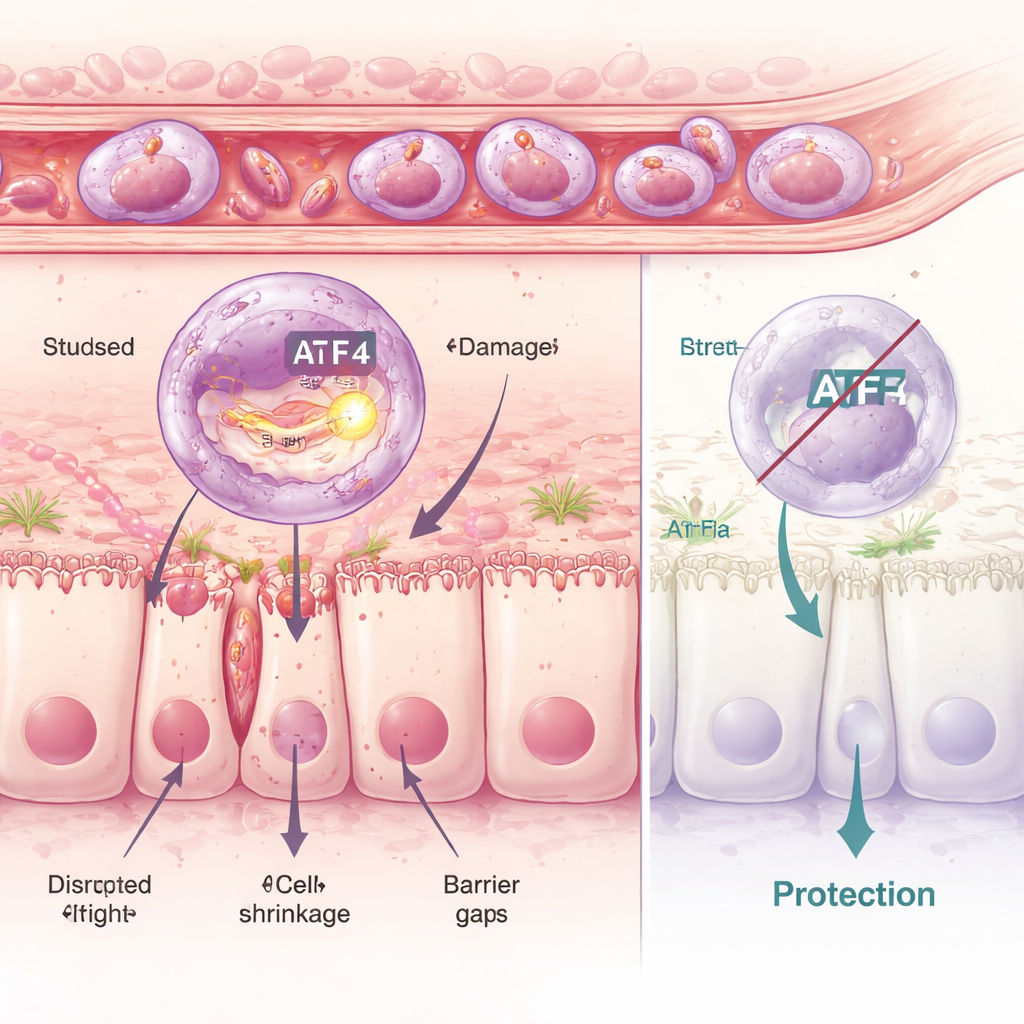
Stress in den Zellen: Wenn die Qualitätskontrolle versagt
Bei genauerer Untersuchung analysierten die Forschenden Neutrophile einzeln und identifizierten sechs unterschiedliche Untergruppen. Eine davon, das C5‑Cluster, zeichnete sich durch ein starkes entzündliches Profil und die Aktivierung eines molekularen Stressprogramms im endoplasmatischen Retikulum aus — der zellulären Werkstatt für Protein‑Faltung. Ein zentraler Regulator dieses Programms ist das Protein ATF4. In den schädlichen C5‑Zellen waren ATF4 und dessen Zielgene hochaktiv. Durch Medikamente, die diese interne Stressantwort entweder verstärken oder dämpfen, zeigten die Forschenden, dass mehr Stress zu mehr Darmschaden führt, während das Blockieren dieses Weges die Darmbarriere schützt. Mäuse, denen ATF4 genetisch fehlte, waren weitgehend geschützt: Selbst wenn stressauslösende Medikamente verabreicht wurden, konnten ihre Neutrophilen das schädliche Programm nicht vollständig ausführen, und die Darmwand blieb deutlich intakter.
Was das für künftige Behandlungen bedeutet
Zusammen ergeben diese Befunde ein klares Bild für ein allgemeines Publikum: Unter den Immunzellen‑Schwärmen, die den Darm nach Wiederherstellung der Durchblutung überschwemmen, agiert eine spezifische, stressbereite Neutrophilen‑Untergruppe wie eine übermotivierte Aufräumtruppe, die das Gebäude zusammen mit den Trümmern niederreißt. Ihre zerstörerische Kraft beruht auf einem intrazellulären Stressweg, der von ATF4 gesteuert wird. Dieses Signal gezielt herunterzufahren — ohne alle Neutrophilen zu eliminieren — könnte eine Möglichkeit bieten, den Darm bei Hochrisikoereignissen wie großen Operationen, schweren Infektionen oder Traumata zu schützen. Zwar sind weitere Studien erforderlich, um diese Ergebnisse beim Menschen zu bestätigen und sichere, präzise Medikamente zu finden, doch die Studie eröffnet einen vielversprechenden Weg zu Therapien, die die Darmbarriere dann bewahren, wenn Patienten sie am meisten brauchen.
Zitation: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Schlüsselwörter: intestinaler Schutzwall, Ischämie‑Reperfusion, Neutrophile, Stress des endoplasmatischen Retikulums, ATF4