Clear Sky Science · de
CKAAKN-Peptid-konjugierte, langzirkulierende Nanoliposomen zur gezielten Verabreichung von Oridonin an Bauchspeicheldrüsenkrebs
Warum diese Forschung wichtig ist
Bauchspeicheldrüsenkrebs gehört zu den tödlichsten Krebsarten, teilweise weil er meist spät entdeckt wird und häufig gegen Standardchemotherapie resistent ist. Diese Studie untersucht eine schlauere Methode, eine pflanzenbasierte, krebshemmende Verbindung — Oridonin — direkt an Bauchspeicheldrüsentumoren zu bringen, indem winzige fettbasierte Bläschen, sogenannte Nanoliposomen, verwendet werden. Indem mehr Wirkstoff das Tumorareal erreicht und gesundes Gewebe geschont wird, weist diese Arbeit auf schonendere und effektivere Behandlungsoptionen für eine Krebsart hin, die dringend neue Ansätze benötigt.
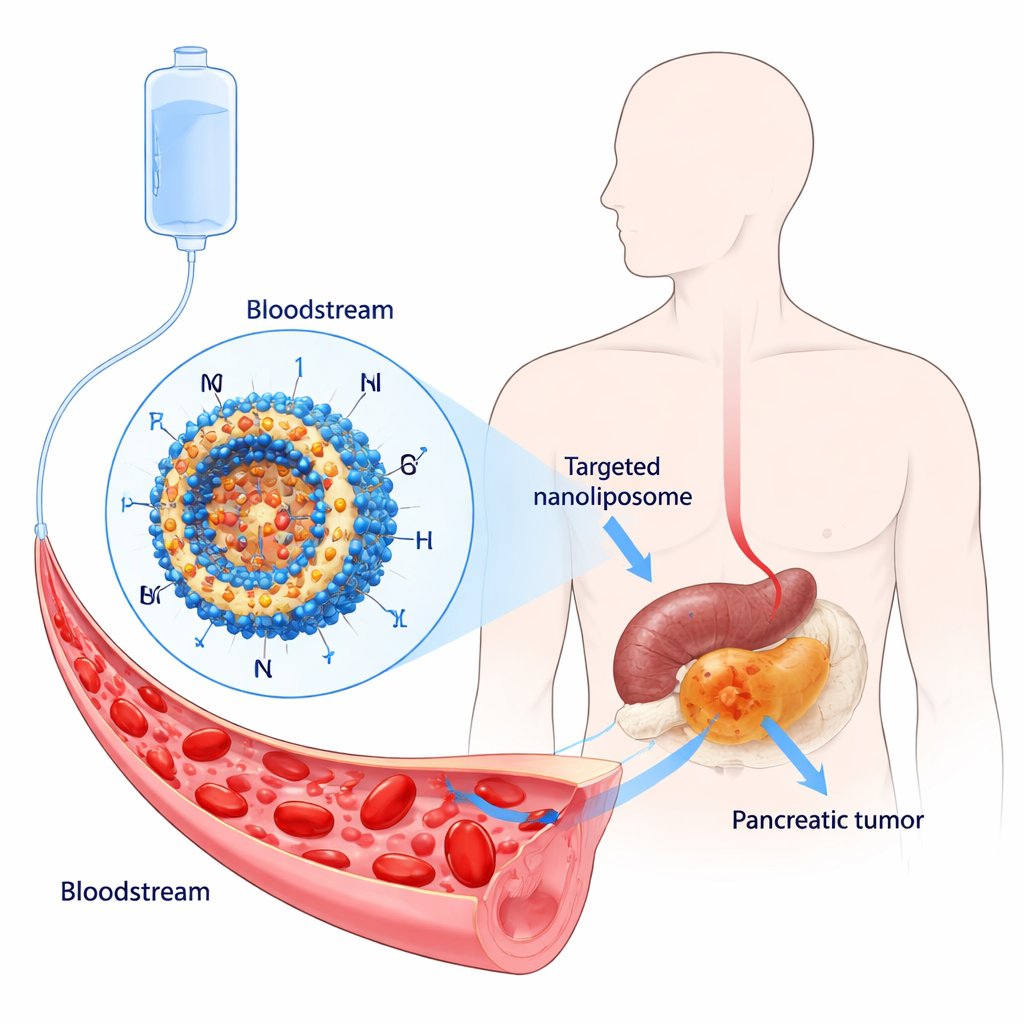
Eine tödliche Krankheit, die schwer zu behandeln ist
Bauchspeicheldrüsenkrebs hat den düsteren Spitznamen „König der Krebse“ erhalten, weil die Überlebensraten bei den meisten Patientinnen und Patienten einstellig bleiben. Nur ein kleiner Teil der Betroffenen kommt für eine Operation in Frage, und selbst dann treten bei vielen Tumoren Rückfälle auf. Chemotherapeutika wie Paclitaxel und Cisplatin können das Fortschreiten bremsen, verursachen aber starke Nebenwirkungen, und Tumoren werden häufig resistent. Forscher suchen deshalb nach Wirkstoffen, die präziser und weniger toxisch sind, sowie nach Verabreichungssystemen, die das Medikament im Tumor konzentrieren, statt den ganzen Körper zu belasten.
Aus einem pflanzlichen Molekül eine moderne Medizin machen
Oridonin ist eine natürliche Verbindung, die aus der traditionellen chinesischen Heilpflanze Rabdosia rubescens gewonnen wird. Laborstudien zeigen, dass sie viele Krebszelltypen, einschließlich pankreatischer Zellen, abtöten oder deren Wachstum verlangsamen kann, indem sie die Zellteilung stört und den programmierten Zelltod auslöst. Allein ist Oridonin jedoch schwer als Arzneimittel nutzbar: Es löst sich schlecht in Wasser, wird schlecht aufgenommen und kann in höheren Dosen toxisch sein. Um sein Potenzial nutzbar zu machen, verpackten die Autorinnen und Autoren Oridonin in Nanoliposomen — winzige Kugeln aus Lipiden, ähnlich denen von Zellmembranen —, die den Wirkstoff sicher durch den Blutkreislauf transportieren und am Tumor langsam freisetzen sollen.
Entwurf einer „stealth“-Homing-Verpackung für den Wirkstoff
Das Team entwickelte ein zweischichtiges Liefersystem. Zuerst erzeugten sie langzirkulierende Liposomen, indem sie die Oberfläche mit Polyethylenglykol (PEG) beschichteten, einem flexiblen, wasserliebenden Polymer, das die Partikel vor Immunzellen verbirgt und ihre Verweildauer im Blut verlängert. Dann fügten sie ein kurzes Peptid, CKAAKN, hinzu, das als Zielmarke für Bauchspeicheldrüsenkrebs wirkt. Dieses Peptid ahmt einen Teil des Wnt-Signalwegs nach, der in vielen Pankreastumoren fehlreguliert ist, sodass die modifizierten Liposomen (genannt ORI@CPD-Lipo) an Krebszellen mit passenden Rezeptoren andocken können. Die fertigen Partikel hatten einen Durchmesser von etwa 100 Nanometern, führten hohe Mengen Oridonin und setzten den Wirkstoff über viele Stunden langsam frei statt auf einmal.
Wie sich die zielgerichteten Partikel in Zellen und Tieren verhalten
In Zellkulturtests wurden die mit CKAAKN markierten Liposomen von menschlichen Bauchspeicheldrüsenkrebszellen deutlich effizienter aufgenommen als von normalen Pankreaszellen, insbesondere in den ersten Stunden der Interaktion. Wurde überschüssiges freies CKAAKN-Peptid als Köder zugegeben, nahmen die Krebszellen weniger Partikel auf, was die Annahme eines spezifischen Bindungsschritts stützt. Leere Liposomen zeigten geringe Toxizität und schädigten keine roten Blutkörperchen, was auf eine gute Verträglichkeit hindeutet. Mit Oridonin beladene, zielgerichtete Liposomen töteten Krebszellen wirksamer als freies Oridonin oder nicht zielgerichtete Liposomen und hemmten die Migration von Krebszellen über eine Kratz‑„Wunde“ in der Kulturschale stärker. Bei Mäusen mit Bauchspeicheldrüsentumoren reichern sich fluoreszenzmarkierte, zielgerichtete Liposomen bis zu 48 Stunden im Tumor an und sammeln sich dort stärker an als nicht zielgerichtete Liposomen, während sie wie erwartet größtenteils über Leber und Milz eliminiert wurden.
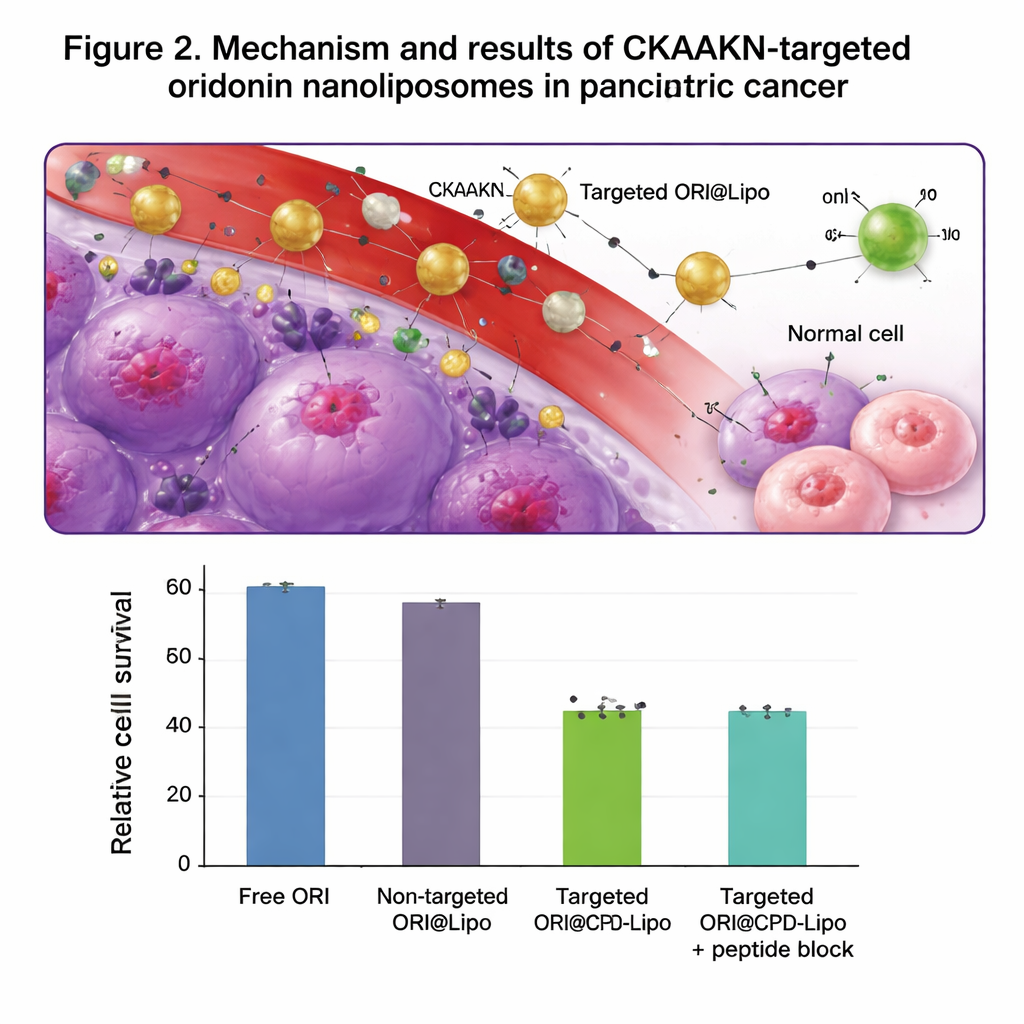
Was das für künftige Behandlungen bedeuten könnte
Insgesamt zeigen die Ergebnisse, dass die Kombination einer traditionellen Pflanzenverbindung mit einem modernen, präzisen Transportvehikel ihre antitumorale Wirkung in Laborversuchen deutlich verstärken kann. Die mit CKAAKN dekorierten, langzirkulierenden Nanoliposomen bringen mehr Oridonin in Bauchspeicheldrüsenkrebszellen, während die Exposition von normalem Gewebe begrenzt bleibt, wodurch Krebszellsterben verstärkt und die Bewegung, die zu Metastasierung führen könnte, reduziert wird. Obwohl diese Befunde noch präklinisch sind und die Autorinnen und Autoren darauf hinweisen, dass umfassende Tierstudien und klinische Prüfungen erforderlich sind, legt die Arbeit eine solide Grundlage für zielgerichtete Nanomedizinansätze beim Bauchspeicheldrüsenkrebs und zeigt eine allgemeine Strategie auf, vielversprechende natürliche Moleküle in praxisnahe, tumoranvisierende Medikamente zu verwandeln.
Zitation: Zhang, F., Luo, K., Xuan, S. et al. CKAAKN peptide-conjugated long-circulating nanoliposomes for the targeted delivery of oridonin to pancreatic cancers. Sci Rep 16, 6065 (2026). https://doi.org/10.1038/s41598-026-36920-5
Schlüsselwörter: Bauchspeicheldrüsenkrebs, Nanoliposomen, gezielte Wirkstofffreisetzung, Oridonin, tumororientiertes Peptid