Clear Sky Science · de
Metadynamik enthüllt luteolin-vermittelte konformationelle Stabilisierung gegen avapritinib-resistente PDGFRα D842V/G680R GIST
Warum das für die Krebstherapie wichtig ist
Zielgerichtete Krebsmedikamente können bemerkenswert wirksam sein – bis Tumoren Wege entwickeln, ihnen zu entkommen. Dieser Artikel untersucht, wie eine weit verbreitete Pflanzenverbindung, Luteolin, dazu beitragen könnte, die Wirksamkeit eines wichtigen Medikaments gegen bestimmte gastrointestinale Stromatumoren (GIST), eine Krebsart im Verdauungstrakt, wiederherzustellen. Mithilfe moderner Computersimulationen zeigen die Forschenden, wie Luteolin ein verformtes Protein in Krebszellen stabilisieren könnte, sodass das bestehende Medikament wieder andocken kann. Das deutet auf einen neuen Ansatz hin, Resistenzen zu bekämpfen, ohne die Behandlung von Grund auf neu erfinden zu müssen. 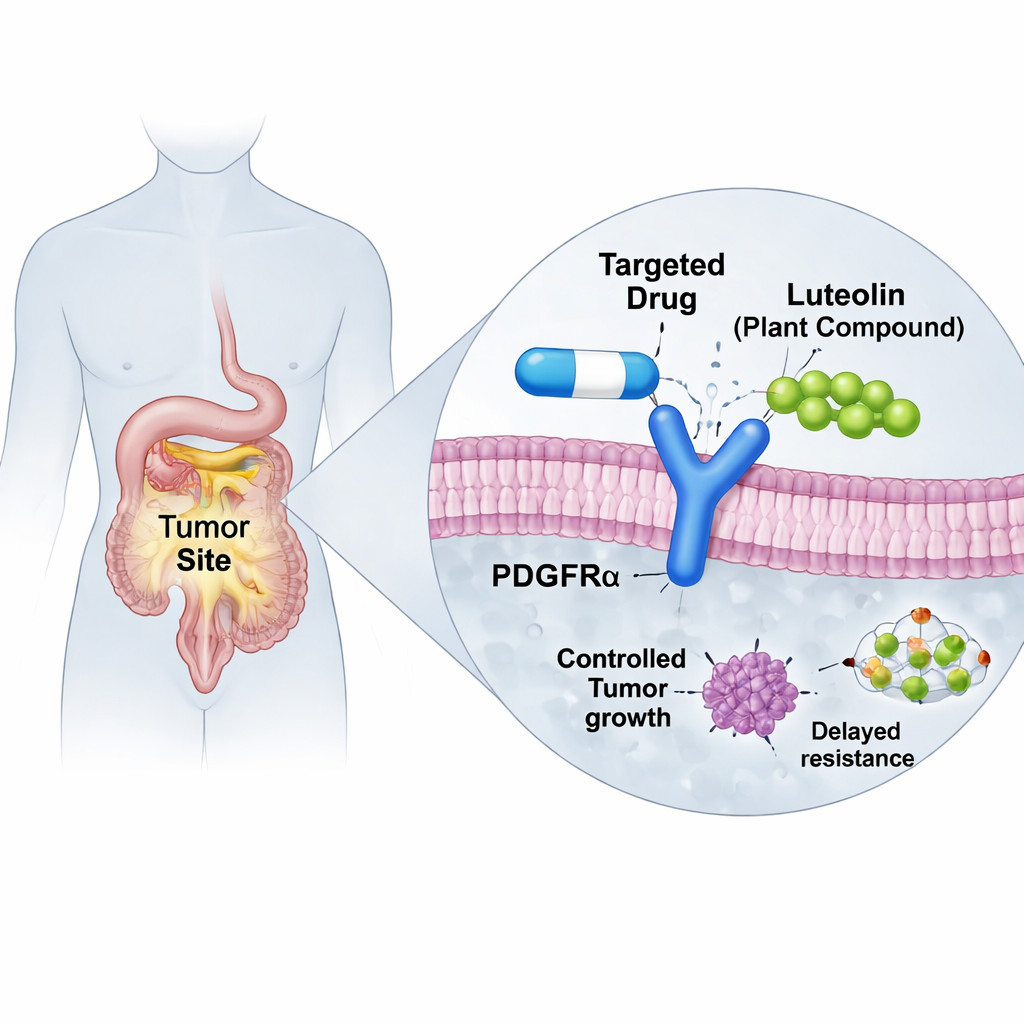
Das Problem: Tumoren, die lernen, Drogen auszuweichen
GISTs wachsen häufig wegen defekter „Anschaltmechanismen“ in zelloberflächenständigen Proteinen wie KIT oder PDGFRα, die dauerhaft Wachstumssignale auslösen. Moderne Präparate, sogenannte Tyrosinkinaseinhibitoren, wurden entwickelt, um diese Schalter auszuschalten, und haben die Prognose vieler Patient*innen stark verbessert. Eine häufige Mutation in PDGFRα, D842V, macht das ältere Medikament Imatinib jedoch weitgehend wirkungslos. Ein neueres Medikament, Avapritinib, wurde speziell entwickelt, um diese hartnäckige Mutation zu bekämpfen, und zeigte in klinischen Studien beeindruckende Erfolge. Leider können Tumoren weiterhin adaptieren. Manche Patient*innen entwickeln zusätzliche Veränderungen in PDGFRα, etwa die sekundäre G680R-Mutation, die physisch verhindert, dass Avapritinib bequem in seine Bindungstasche passt, wodurch das Medikament herausfällt und Resistenzen zunehmen.
Ein Pflanzenmolekül mit faszinierender Form
Naturstoffe sind eine reiche Quelle für Arzneimittelideen, und Flavonoide – farbige Verbindungen, die in vielen Früchten, Gemüsen und Heilpflanzen vorkommen – interagieren oft mit wachstumsregulierenden Proteinen in Zellen. Luteolin, ein solches Flavonoid, das in dem im Mittelmeerraum vorkommenden Strauch Retama monosperma enthalten ist, wurde bereits hinsichtlich seiner antikanzerogenen und entzündungshemmenden Eigenschaften untersucht und scheint in oral erreichbaren Dosen sicher zu sein. Auf der Grundlage früherer Screenings vermuteten die Autor*innen, dass Luteolin an PDGFRα an einer Stelle anhaften könnte, die nahe, aber nicht überlappend mit der üblichen Wirkstoffbindungsstelle liegt. Wenn das stimmt, könnte Luteolin wie eine subtile Schiene wirken und das Protein in eine Form bringen, die Avapritinib wieder aufnimmt.
Simulation einer molekularen Partnerschaft
Um diese Idee in silico zu testen, bauten die Forschenden detaillierte dreidimensionale Computermodelle des resistenten PDGFRα-Proteins mit den Mutationen D842V und G680R. Sie simulierten, wie sich Avapritinib allein verhält und wie es sich verhält, wenn Luteolin in der Nähe gebunden ist, und verfolgten atomare Bewegungen über Hunderte von Nanosekunden – Milliardenstel einer Sekunde in Echtzeit. Wenn nur Avapritinib gebunden war, driftete das Medikament allmählich aus seiner Tasche, da die sperrige G680R-Veränderung es wegdrückte, bis es vollständig vom Protein gelöst war. Im Gegensatz dazu blieb Avapritinib weitgehend an Ort und Stelle, wenn Luteolin zusätzlich an einer separaten „allosterischen“ Stelle neben einer Schlüsselhelix gebunden war. Das Protein als Ganzes bewegte sich weniger, wichtige Struktursegmente behielten ihre Form, und bedeutsame Kontakte zwischen dem Medikament und dem Protein hielten deutlich länger an. 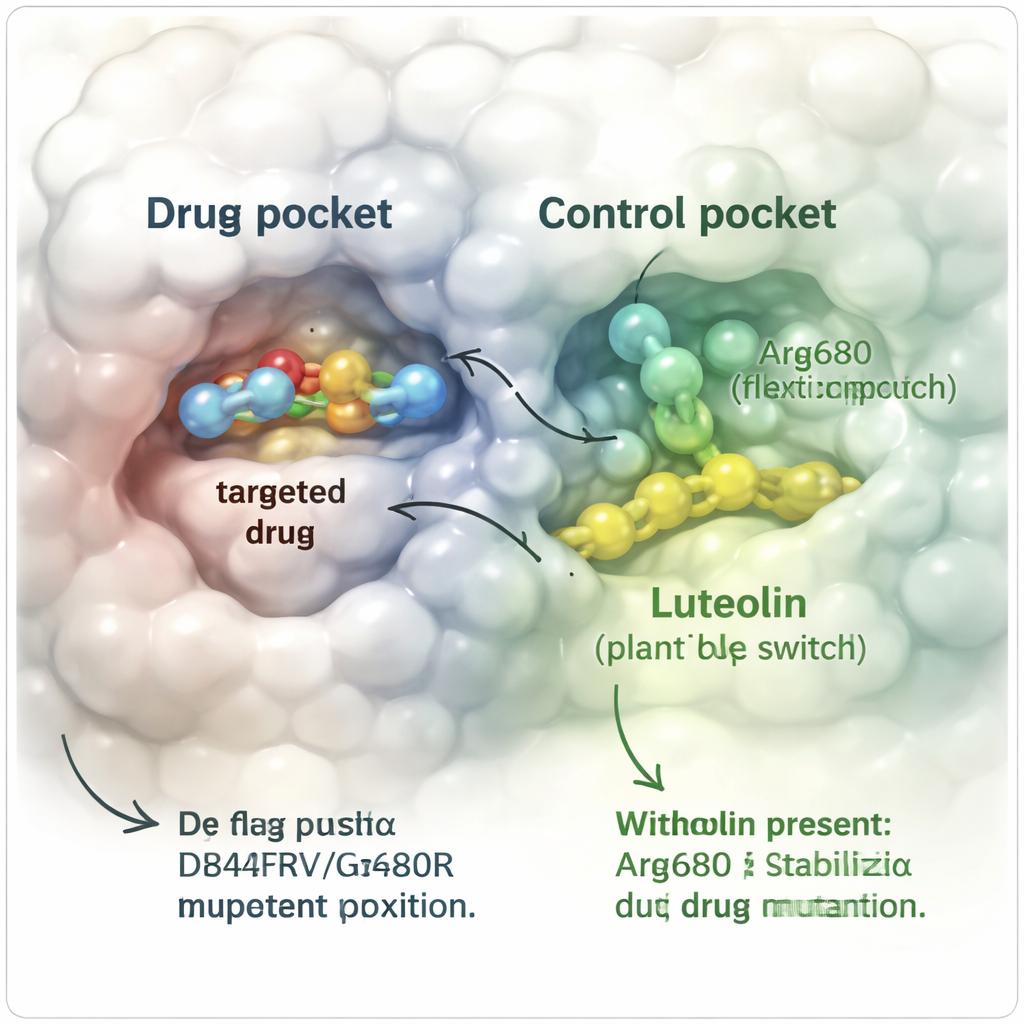
Ein widerspenstigen molekularen Schalter fixieren
Standardmäßige Simulationen übersehen seltene, aber wichtige Formänderungen, daher nutzten die Forschenden einen erweiterten Ansatz, die Metadynamik, um vollständiger zu erkunden, wie sich das Protein verdrehen und biegen könnte. Sie konzentrierten sich auf das Verhalten der veränderten Aminosäure Arg680, die wie ein kleiner flexibler Arm nahe der Wirkstofftasche wirkt. Ohne Luteolin nahm dieser Arm viele Positionen ein und das Medikament rutschte leicht weg, mit relativ niedrigen Energiebarrieren für das Entkommen. Mit Luteolin an Ort und Stelle wurde Arg680 in einer bestimmten Orientierung gehalten, die nicht mehr mit dem Medikament kollidierte. Die Energielandschaft verschob sich: Das System bevorzugte nun Konformationen, in denen Avapritinib gebunden blieb, und der energetische „Berg“, den das Medikament erklimmen müsste, um zu entkommen, wuchs um mehrere Kilokalorien, wodurch die Dissoziation deutlich unwahrscheinlicher wurde.
Was das für Patient*innen bedeuten könnte
Einfach ausgedrückt legt die Studie nahe, dass Luteolin wie eine molekulare Schiene wirken könnte, die ein verzogenes Krebsprotein stabilisiert, sodass eine vorhandene zielgerichtete Tablette wieder greifen kann. Statt für jede Resistenzmutation ein völlig neues Medikament zu entwickeln, könnte die Kombination des aktuellen Mittels mit einer sorgfältig ausgewählten Hilfssubstanz seine Wirksamkeit wiederherstellen. Die Arbeit basiert auf leistungsfähigen, aber rein rechnerischen Methoden, daher sind Labor- und Tierversuche nötig, um zu bestätigen, ob Luteolin oder ein verwandtes, für Arzneimittelzwecke optimiertes Molekül Avapritinib in lebenden Systemen tatsächlich verstärkt. Dennoch könnte das Konzept, kleine allosterische Helfer zu nutzen, um resistente Krebsziele neu zu stabilisieren, einen vielversprechenden Weg eröffnen, die Lebensdauer heutiger Präzisionstherapien zu verlängern.
Zitation: El Khattabi, K., Akachar, J., Lemriss, S. et al. Metadynamics reveals luteolin-mediated conformational stabilization against avapritinib-resistant PDGFRα D842V/G680R GIST. Sci Rep 16, 6534 (2026). https://doi.org/10.1038/s41598-026-36898-0
Schlüsselwörter: Arzneimittelresistenz, gastrointestinales Stromatumor, Tyrosinkinaseinhibitoren, Luteolin, allosterische Modulation