Clear Sky Science · de
Synthese und antitumorale Bewertung neuartiger Thioimidazol‑Derivate mit Trimethoxyphenyl‑Fragment
Neue chemische Werkzeuge im Kampf gegen Krebs
Chemotherapeutika schädigen oft gesunde Zellen neben Tumoren, was zu starken Nebenwirkungen führt. Diese Studie untersucht eine neue Familie im Labor hergestellter Moleküle, die Krebszellen deutlich stärker angreifen sollen als normales Gewebe. Durch das clevere Zusammenfügen zweier chemischer Bausteine, die bereits in Arzneimitteln erfolgreich sind, erzeugten die Forschenden Verbindungen, die in Reagenzglas‑ und 3D‑Tumormodellen eine starke, zielgerichtete Abtötung von Krebszellen zeigen, während gesunde Zellen weitgehend verschont bleiben.
Intelligentere krebstötende Moleküle entwickeln
Das Team konzentrierte sich auf zwei „bevorzugte“ chemische Gerüste, die immer wieder in erfolgreichen Medikamenten vorkommen. Das eine ist Imidazol, ein kleiner Ring, der gut in viele biologische Zielstrukturen passt. Das andere ist eine Trimethoxyphenyl‑(TMP)‑Gruppe, ein Muster aus drei sauerstoffhaltigen Seitenketten an einem aromatischen Ring, das in mehreren Antikrebswirkstoffen vorkommt, die die Zellteilung stören. Indem sie dem Imidazolkern ein Schwefelatom zusetzten (ein Thioimidazol erzeugend) und es mit einer TMP‑Gruppe verbanden, wollten die Chemiker die Verteilung der Moleküle im Körper und ihre Bindungsstärke an krebsrelevanten Proteinen feinjustieren. Mittels einer schrittweisen Syntheseroute bauten sie eine Bibliothek verwandter Verbindungen auf, die jeweils subtil variiert wurden, um herauszufinden, welche Merkmale für die antitumorale Aktivität am wichtigsten sind. 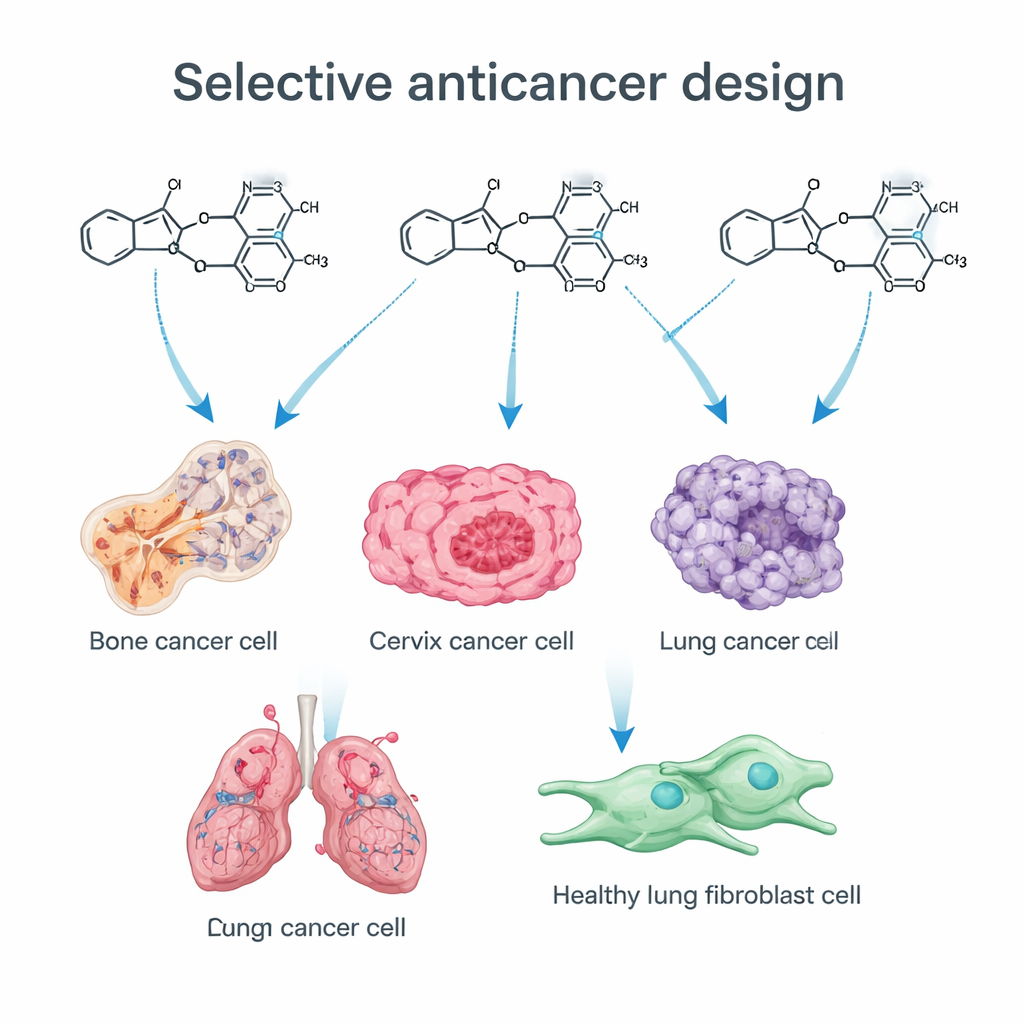
Krebszellen testen und dabei gesundes Gewebe schonen
Die neuen Moleküle wurden an vier humanen Krebszelllinien getestet — Osteosarkom (Knochen), Gebärmutterhalskrebs, Darm- und Lungenkrebs — sowie an nicht‑tumorösen Lungenfibroblasten. Viele der Verbindungen verlangsamten oder stoppten das Wachstum der Krebszellen, doch eine Verbindung, bezeichnet als 13b, fiel besonders auf. Sie tötete Knochen‑ und Gebärmutterhalskrebszellen in sehr niedrigen Konzentrationen, zeigte jedoch auch bei mehr als 60‑fach höheren Dosen keine nachweisbare Toxizität gegenüber normalen Fibroblasten. Mehrere andere Verbindungen waren mäßig wirksam, aber weniger selektiv, was unterstreicht, wie kleine strukturelle Änderungen — etwa das Einfügen eines Chloratoms oder einer Nitrogruppe an bestimmten Positionen — das Gleichgewicht zwischen breiter Toxizität und krebsfokussierter Wirkung verschieben können.
Wie die Leitverbindung Krebszellen zur Selbstzerstörung bringt
Um zu verstehen, was 13b innerhalb der Zellen bewirkt, suchten die Forschenden nach Kennzeichen des programmierten Zelltods, der Apoptose. Mit 13b behandelte Krebszellen wurden Annexin‑V‑positiv und zeigten aktivierte Enzyme Caspase‑3 und ‑7, klassische Marker dafür, dass eine Zelle in ein geordnetes Suizidprogramm gedrängt wurde statt einfach zu platzen. Die Mikroskopie zeigte helle Flecke von γH2AX, ein Signal für gebrochene DNA‑Stränge, in den Zellkernen der behandelten Zellen. Im Laufe der Zeit begann das innere Gerüst der Zellen sich umzuorganisieren und zu zerfallen, besonders in den Gebärmutterhalskrebszellen, die sich aufrollten und ablösten — visuelle Hinweise darauf, dass die Apoptose in vollem Gange war. Zusammengenommen zeigen diese Befunde, dass 13b die DNA von Krebszellen schädigt und die Zellen anschließend auf einen kontrollierten Todesweg treibt.
Von flachen Zellschichten zu 3D‑Mini‑Tumoren
Die meisten Labortests züchten Krebszellen in dünnen Schichten, die die dichte, geschichtete Struktur echter Tumoren nicht vollständig nachbilden. Um dem Rechnung zu tragen, züchtete das Team die Krebszellen zu dreidimensionalen Spheroiden — winzigen, kugelförmigen Clustern, die der Architektur eines Tumors und den Herausforderungen der Wirkstoffpenetrierung näher kommen. Wurden diese Spheroide mit 13b behandelt, schrumpften sie konzentrationsabhängig. Besonders empfindlich waren die Spheroide des Knochentumors; bei höheren Wirkstoffkonzentrationen wurden sie klein, locker und fragmentiert. Fluoreszenzfärbungen zeigten Wellen der Apoptose, die bei steigender Konzentration von außen nach innen durch die Sphäroide liefen, was beweist, dass 13b in der Lage ist, diese kompakten Strukturen zu durchdringen und Zellen im gesamten Volumen abzutöten. 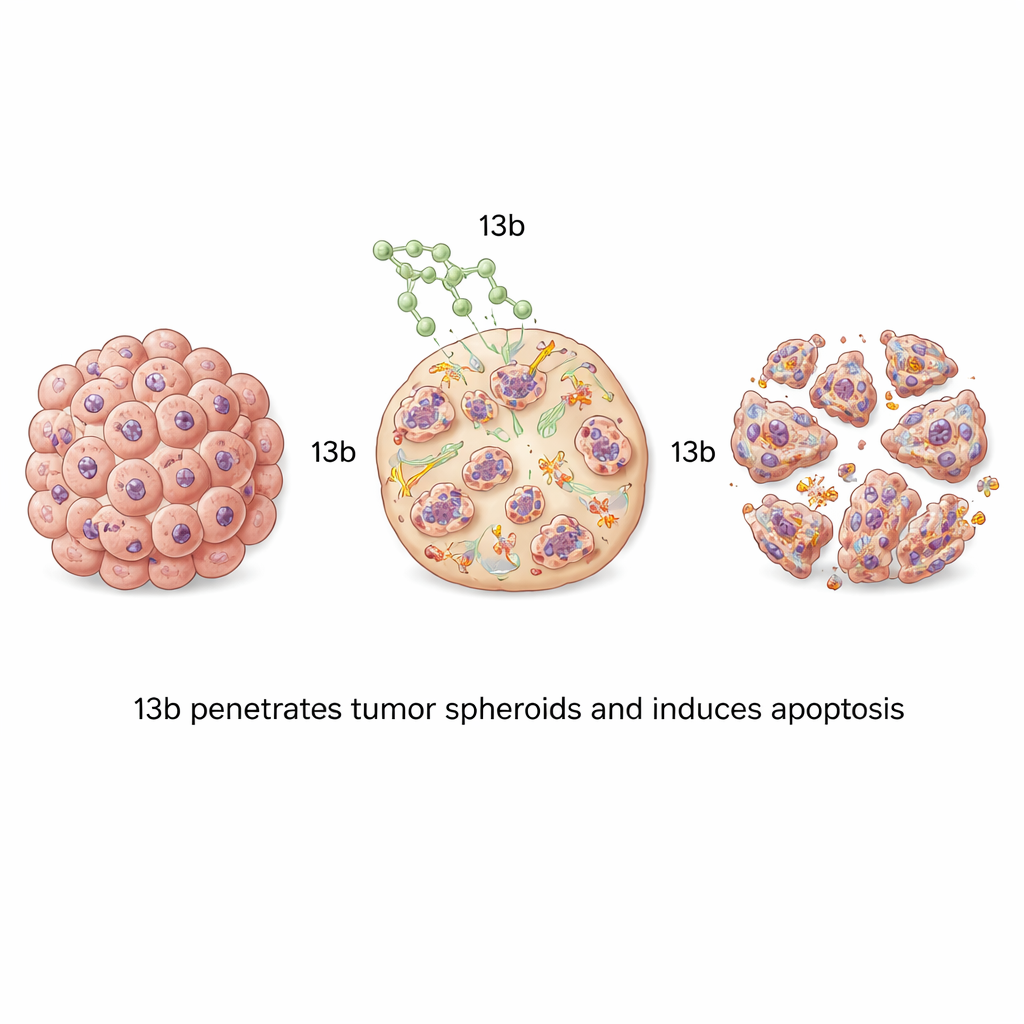
Warum diese Arbeit für zukünftige Krebstherapien wichtig ist
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass die Forschenden eine neue Klasse kleiner Moleküle geschaffen haben, die die besten Eigenschaften zweier bewährter Wirkstoffkomponenten in einem hybriden Design vereinen. Ihre Leitverbindung 13b erkennt und zerstört Krebszellen effizient und schont in Labortests weitgehend gesunde Zellen; sie bleibt auch in realistischeren 3D‑Tumormodellen wirksam. Zwar steht noch viel Arbeit aus — etwa die genaue Identifizierung der molekularen Ziele, die Verbesserung der Löslichkeit und Tierversuche — doch zeigt diese Studie, dass die Kombination von Thioimidazol‑ und TMP‑Gerüsten eine vielversprechende Strategie zur Entwicklung selektiverer und wirksamerer Antikrebsmittel ist.
Zitation: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Schlüsselwörter: Antikrebsmittel, Imidazol‑Derivate, Trimethoxyphenyl, Apoptose, 3D‑Tumor‑Spheroide