Clear Sky Science · de
4-Nonylphenol reguliert Zellproliferation und Apoptose im Zervixkarzinom über den MEG3/PI3K/AKT-Signalweg
Alltägliche Chemikalien und das Krebsrisiko bei Frauen
Wir sind umgeben von Chemikalien aus Kunststoffen, Reinigungsmitteln und Pestiziden, die im Körper wie Hormone wirken können. Diese Studie untersucht, ob eine solche Verbindung, 4‑Nonylphenol (4‑NP), die Entstehung von Zervixkarzinom fördern könnte und wie ein natürlicher Schutzfaktor in unseren Zellen, genannt MEG3, dem entgegentreten kann. Das Verständnis dieser Wechselwirkung könnte neue Wege aufzeigen, das Risiko durch Umweltverschmutzung zu reduzieren und gezieltere Therapien für Gebärmutterhalskrebs zu entwickeln.
Ein verbreiteter Schadstoff unter dem Mikroskop
4‑NP wird in vielen Industrieprodukten verwendet und kann in Wasser, Boden und schließlich in den menschlichen Körper gelangen. Es verhält sich ähnlich wie Östrogen, ein wichtiges weibliches Hormon, und wurde mit Problemen des Fortpflanzungssystems in Verbindung gebracht. Die Forschenden stellten zunächst eine einfache Frage: Tragen Frauen mit Zervixkarzinom höhere Mengen dieser Chemikalie im Körper? Durch die Messung von 4‑NP im Urin von 35 Frauen mit Zervixkarzinom und 35 gesunden Frauen fanden sie heraus, dass Patientinnen im Mittel fast sechsmal höhere 4‑NP-Werte hatten. Das beweist nicht, dass die Chemikalie Krebs verursacht, zeigt aber, dass Frauen mit Zervixkarzinom tendenziell deutlich höher exponiert sind.
Die eingebaute Bremse des Körpers: MEG3
In unseren Zellen können lange RNA-Stränge, die keine Proteine codieren, dennoch steuern, wie Zellen wachsen und sterben. Eine davon, MEG3 genannt, wirkt normalerweise als Bremse für Tumorwachstum. Das Team verglich Tumorgewebe des Gebärmutterhalses mit benachbartem gesundem Gewebe von 31 Patientinnen und fand, dass die MEG3-Spiegel in Tumoren deutlich niedriger waren. Dasselbe Muster zeigte sich in Zellversuchen: Zervixkarzinomzellen (HeLa) wiesen weniger MEG3 auf als normale Zervixzellen, und bei Exposition gegenüber 4‑NP sank MEG3 mit der Zeit noch weiter. Das deutet darauf hin, dass sowohl der Krebs selbst als auch die Umweltbelastung durch 4‑NP zusammenwirken können, um ein natürliches tumorsuppressives Signal zu unterdrücken.
Wenn die Bremse wiederhergestellt wird
Als Nächstes testeten die Wissenschaftler, was passiert, wenn sie Krebszellen dazu bringen, mehr MEG3 zu produzieren. Mithilfe eines viralen Vektors, um MEG3 in HeLa-Zellen zu erhöhen, beobachteten sie eine Verlangsamung der Zellen. Die Krebszellen teilten sich seltener, bewegten sich langsamer über die Kulturplatte (ein Hinweis auf geringere Invasionsfähigkeit) und gingen eher in programmierte Zellsterbeformen über. Zellzyklustests zeigten, dass MEG3 die Zellen dazu brachte, vor der DNA-Replikation eine Pause einzulegen, eine weitere Möglichkeit, das Wachstum zu begrenzen. In Mäusen waren Tumoren, die aus MEG3-aufgepeppten HeLa-Zellen entstanden, deutlich kleiner und leichter als solche aus gewöhnlichen Krebszellen, was bestätigt, dass MEG3 das Tumorwachstum in einem lebenden Organismus hemmen kann.
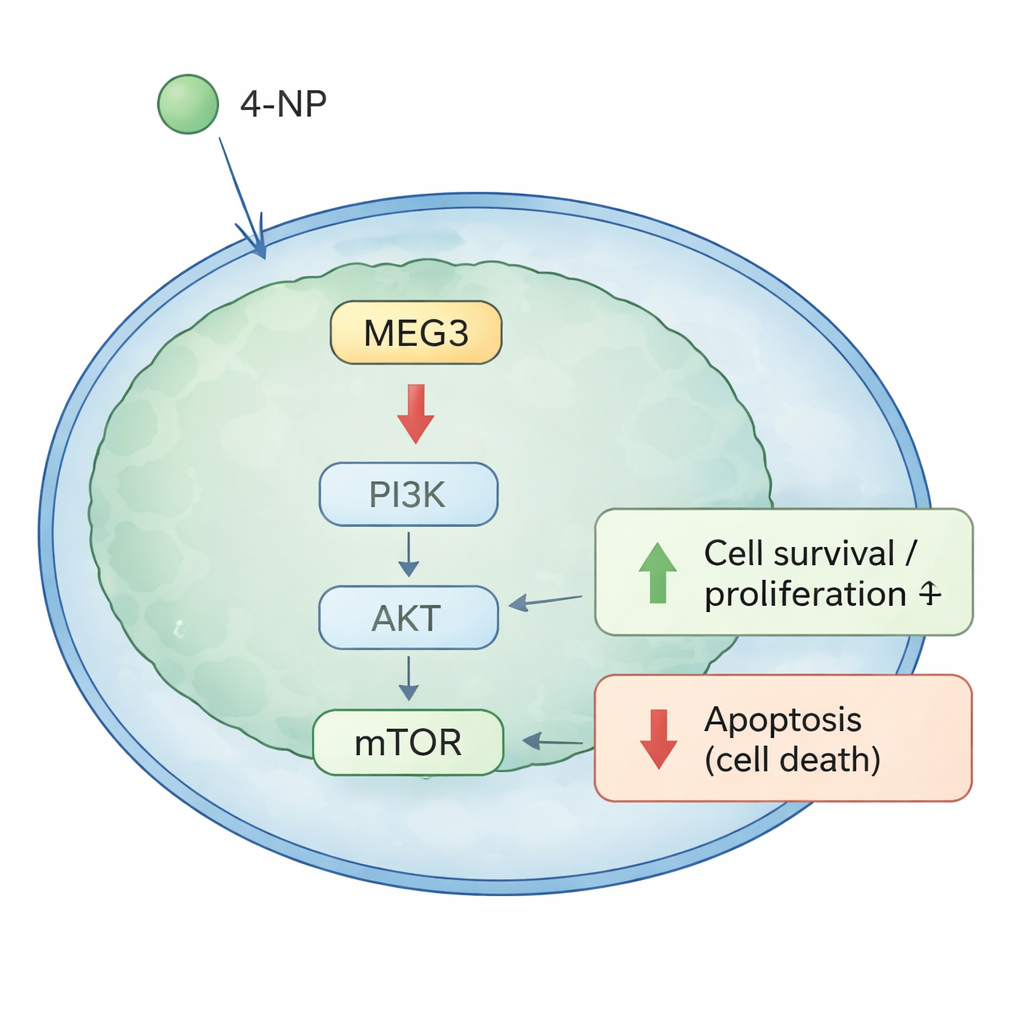
Ein Wachstumsschalter innerhalb der Krebszellen
Um zu verstehen, wie MEG3 diese Kontrolle ausübt, konzentrierten sich die Forschenden auf einen bekannten Wachstumsschalter in Zellen: den PI3K/AKT-Signalweg. Wenn dieser Weg aktiv ist, neigen Zellen dazu zu wachsen und zu überleben; ist er gedämpft, sind Zellen eher dem Tod geweiht. Sowohl in Zellkulturen als auch in Mäusetumoren reduzierte die Erhöhung von MEG3 die aktiven (phosphorylierten) Formen von PI3K, AKT und mTOR sowie BCL‑2, ein Protein, das Zellen vor dem Zelltod schützt, während pro‑apoptotische Signale begünstigt wurden. Im Gegensatz dazu hatte die Exposition gegenüber 4‑NP die gegenteilige Wirkung: Sie verstärkte Signale für Wachstum und Überleben und verringerte den Zelltod. Wichtig ist, dass die Wiederherstellung von MEG3 die pro‑Wachstums- und anti‑Zelltod-Effekte von 4‑NP weitgehend umkehrte, was darauf hindeutet, dass diese RNA als Schlüsselvermittler zwischen Umweltexposition und dem Verhalten von Krebszellen fungiert.
Was das für Patientinnen und Prävention bedeutet
Für Nicht‑Spezialistinnen und Nicht‑Spezialisten lautet die Botschaft: Eine verbreitete Umweltchemikalie steht offenbar in Zusammenhang mit höheren Körperbelastungen bei Frauen mit Zervixkarzinom und kann im Labor Krebszellen dazu bringen, schneller zu wachsen und seltener zu sterben. MEG3, ein natürliches Molekül in unseren Zellen, wirkt als Schutzmechanismus, indem es einen starken Wachstumsweg drosselt. Zwar kann die Studie noch nicht beweisen, dass 4‑NP Gebärmutterhalskrebs verursacht, und sie war in Größe und Modellen begrenzt, doch sie hebt eine neue Ereigniskette hervor: 4‑NP senkt MEG3, wodurch ein Wachstumsschalter freigelegt wird, der Tumoren begünstigt. Künftig könnten die Überwachung von 4‑NP-Werten und MEG3-Aktivität helfen, das Umweltrisiko besser einzuschätzen, und Therapien, die MEG3 wiederherstellen oder denselben Wachstumsweg blockieren, könnten neue Optionen für Frauen mit Zervixkarzinom bieten.
Zitation: Wu, W., Ren, X., Chen, Y. et al. 4-Nonylphenol regulates cell proliferation and apoptosis in cervical carcinoma through the MEG3/PI3K/AKT signaling pathway. Sci Rep 16, 6067 (2026). https://doi.org/10.1038/s41598-026-36863-x
Schlüsselwörter: Zervixkarzinom, Umweltgifte, 4-Nonylphenol, lange nicht-kodierende RNA MEG3, PI3K-AKT-Signalweg