Clear Sky Science · de
Differenzielle Mechanismen der SARS-CoV-2-Inaktivierung durch anionische Tenside: eine vergleichende Studie von Fettsäuresalzen und synthetischen Tensiden
Warum die Wahl der Seife noch immer wichtig ist
Die COVID‑19-Pandemie machte Händewaschen zur täglichen Devise, doch nicht alle Seifen wirken gleich gegen das Virus, das die Krankheit verursacht. Diese Studie blickt mikroskopisch auf gängige Seifenbestandteile, um zu ermitteln, welche am besten SARS‑CoV‑2 entwaffnen und wie sie das tun. Die Ergebnisse können helfen, bessere Entscheidungen für alltägliche Seifen und Desinfektionsmittel zu treffen und damit eine Routine wie Händewaschen zu einem noch wirksameren Mittel für die Gesundheit zu machen.
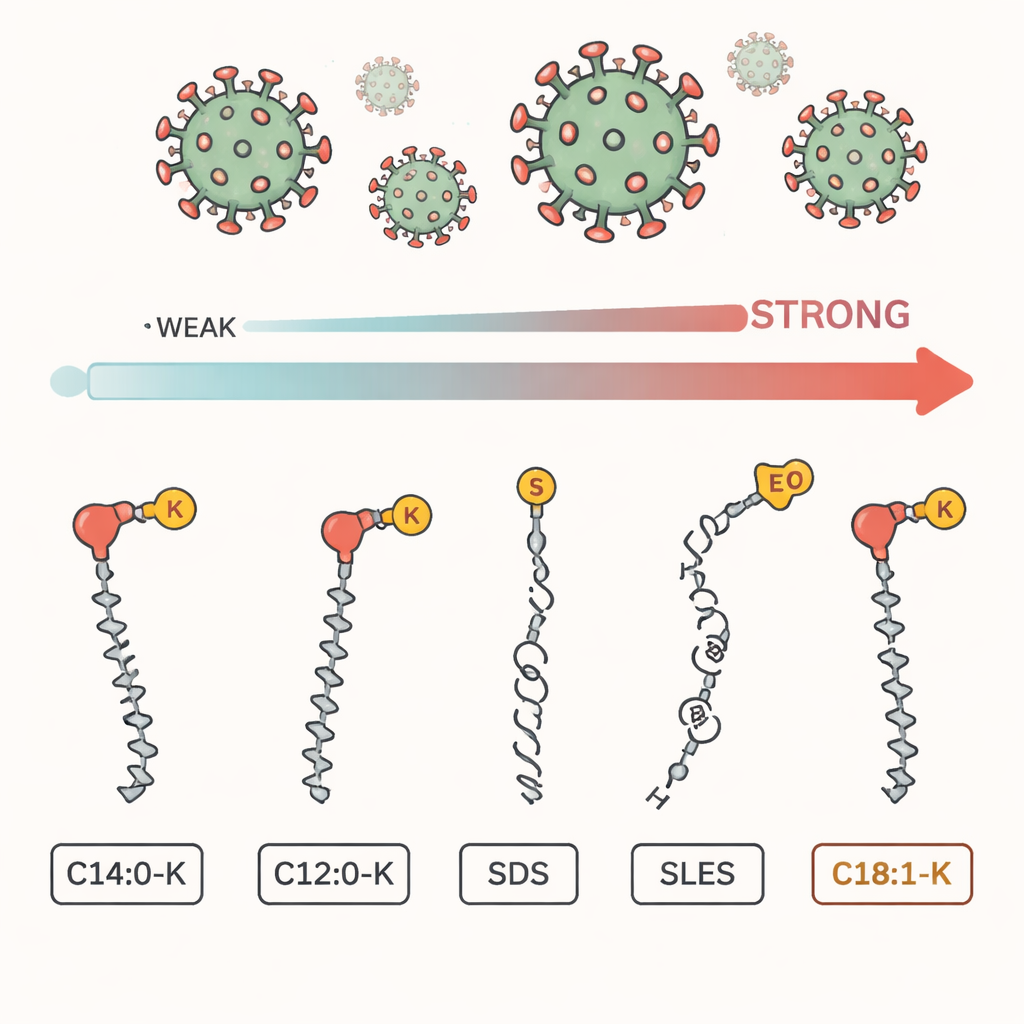
Wie Seife eine fettige Schutzschicht bekämpft
SARS‑CoV‑2 ist wie viele gefährliche Viren von einer fragilen, fettigen Hülle aus Lipiden umgeben. Seifenmoleküle haben zwei Gesichter: eine hydrophile (wasserliebende) Seite und eine lipophile (ölfreundliche) Seite. Beim Händewaschen schieben sich diese Moleküle in diese fettige Hülle und können sie aufreißen, wodurch das Virus unfähig wird, Zellen zu infizieren. Seifen bestehen jedoch aus unterschiedlichen Inhaltsstoffen; in dieser Studie verglichen die Autoren fünf weit verbreitete: drei natürliche Fettsäuresalze (darunter Kaliumoleat, bezeichnet als C18:1‑K) und zwei häufige synthetische Tenside, SDS und SLES, die oft in Flüssigseifen und Shampoos vorkommen.
Welche Seifenbestandteile das Virus am stärksten treffen
Als die Forschenden das Virus im Labor mit diesen Tensiden vermischten, stach ein Inhaltsstoff besonders hervor. C18:1‑K, ein natürlicher Seifenbestandteil mit einem langen, leicht geknickten Schwanz, verringerte die Infektiosität des Virus bei sehr niedriger Konzentration um mehr als den Faktor 100.000. SDS, ein stärker wirkender synthetischer Inhaltsstoff, erreichte bei derselben Konzentration nur etwa eine zehnfache Reduktion, und SLES sowie ein kurzschwänziges Seifenmolekül, C12:0‑K, inaktivierten das Virus kaum. Insgesamt ergab sich eine klare Rangfolge: C18:1‑K war am wirksamsten, gefolgt von SDS, dann SLES, während die kürzeren Fettsäuren zurückblieben. Längere, stärker lipophile Ketten führten zu deutlich stärkerer Virusinaktivierung.
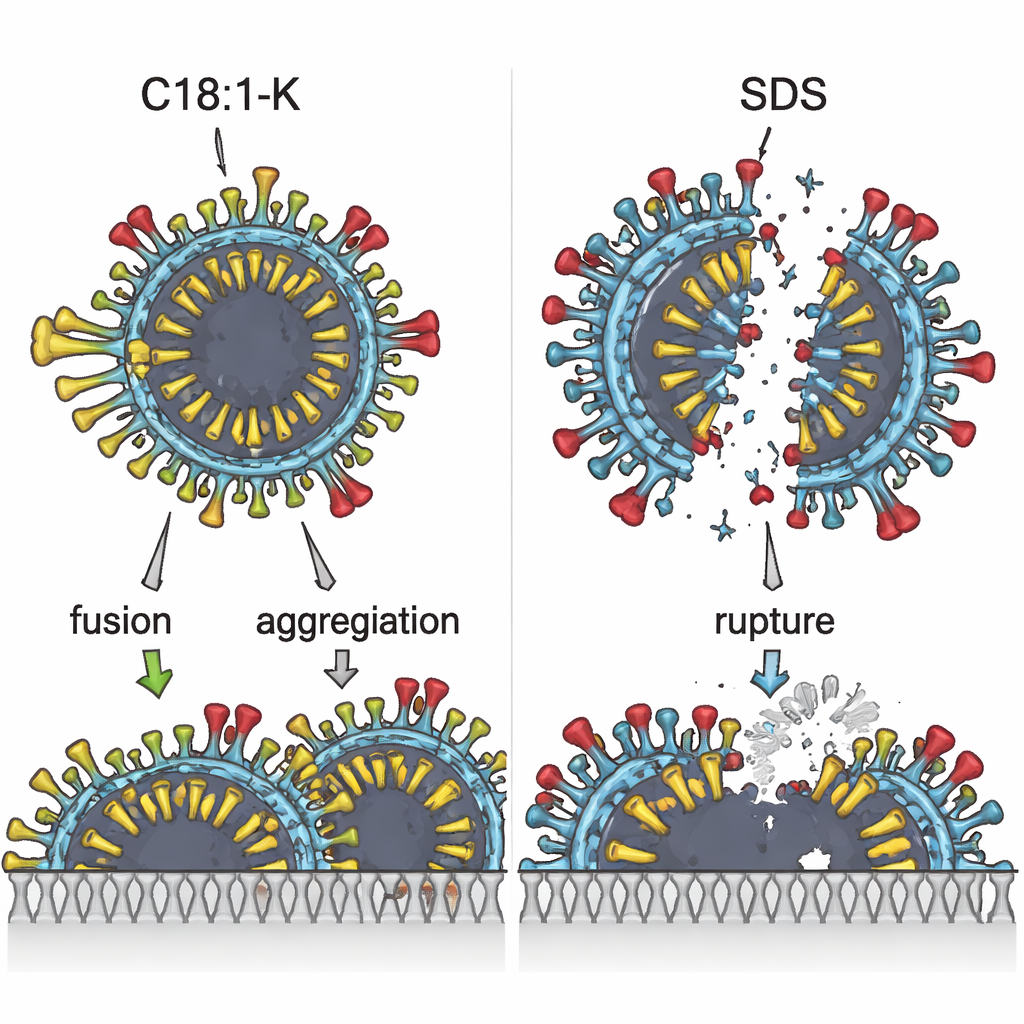
Einen Blick auf unsichtbare Gefechte
Um zu verstehen, warum diese Unterschiede so groß waren, nutzte das Team eine wärmemessende Methode, um nachzuverfolgen, wie Tenside mit dem Virus interagieren. C18:1‑K erzeugte ein Wärmeprofil, das zeigte, dass es vornehmlich mit seinem öligen Schwanz in die Lipidhülle des Virus eindringt — ein Vorgang, der von hydrophoben (ölfreundlichen) Kräften angetrieben wird. SDS und C12:0‑K hingegen zeigten entgegengesetzte Wärmeänderungen, was darauf hindeutet, dass sie stärker an geladene Proteinanteile auf der Virusoberfläche binden, anstatt die Fetthülle tiefgreifend zu stören. SLES lag dazwischen und offenbarten ein Gleichgewicht zwischen öl‑ und wasserliebenden Eigenschaften. Diese energetischen Fingerabdrücke zeigten, dass sich nicht nur die Stärke, sondern auch der Angriffsmodus der Inhaltsstoffe unterschied.
Was das Mikroskop zeigte
Die Elektronenmikroskopie lieferte ein visuelles Gegenstück zu diesen unsichtbaren Energieänderungen. Wurde das Virus mit Tensiden behandelt, die hauptsächlich über elektrische Anziehung an Proteine wirken, wie SDS oder C12:0‑K, wirkten viele Partikel aufgerissen oder rupturiert. Bei C18:1‑K hingegen erschienen die Viruspartikel häufiger verschmolzen oder verklumpt, ohne deutliches Aufplatzten. Alle Tenside führten bei höheren Konzentrationen zu einem gewissen Grad an Virusaggregation, doch nur C18:1‑K erzeugte ausgedehnte „membranverschmolzene“ Cluster, die wahrscheinlich nicht infektiös bleiben. Der Inhaltsstoff, der das Virus am besten inaktivierte, C18:1‑K, wies außerdem die niedrigste kritische Mizellenkonzentration auf — ein Hinweis darauf, dass seine öligen Schwänze leicht zusammenpacken und die virale Membran nach Überschreiten einer Schwelle stark stören können.
Was das für den Alltagschutz bedeutet
Für Nichtfachleute ist die Kernaussage einfach: Handseife beschädigt SARS‑CoV‑2 chemisch, und einige natürlich gewonnene Inhaltsstoffe sind darin ungewöhnlich wirksam. Seifen, die reich an langkettigen Fettsäuresalzen wie Kaliumoleat sind, können die fettige Hülle des Virus durch starke hydrophobe Wechselwirkungen angreifen und Viruspartikel zum Verschmelzen und Verklumpen bringen, wodurch sie harmlos werden. Während alle getesteten Tenside zur Inaktivierung beitragen können, bieten solche, die für starke hydrophobe Wirkung ausgelegt oder ausgewählt sind, möglicherweise einen überlegenen Schutz. Diese Erkenntnisse können Chemikerinnen und Chemikern helfen, effektivere und hautverträglichere Seifen und Desinfektionsmittel zu entwickeln — nicht nur gegen SARS‑CoV‑2, sondern auch gegen andere von einer Hülle umgebene Viren, die auf dieselbe fragile Lipidschicht angewiesen sind.
Zitation: Yamamoto, A., Iseki, Y., Elsayed, A.M.A. et al. Differential mechanisms of SARS-CoV-2 inactivation by anionic surfactants: a comparative study of fatty acid salts and synthetic surfactants. Sci Rep 16, 6394 (2026). https://doi.org/10.1038/s41598-026-36858-8
Schlüsselwörter: Händewaschen, SARS-CoV-2, Seifentenside, virale Hülle, Desinfektionsmittel