Clear Sky Science · de
Pharmakokinetik, Pathologie und Wirksamkeit des SARS‑CoV‑2‑Hauptproteaseinhibitors VPC285785 in einem murinen Modell der Coronavirusinfektion
Warum wir immer noch bessere COVID‑Pillen brauchen
Die ersten antiviralen Tabletten gegen COVID‑19, etwa Paxlovid, stellten einen Wendepunkt in der Pandemie dar. Doch sie sind nicht ideal: Sie müssen sehr früh eingenommen werden, erfordern mehrere Tabletten pro Tag und können gefährlich mit anderen Medikamenten wechselwirken. Diese Studie untersucht neue Wirkstoffkandidaten, die das Coronavirus auf mehr als eine Weise blockieren, sich als einzeldosige orale Tabletten eignen und weniger Arzneimittel‑Wechselwirkungen verursachen sollen, anhand eines Mausmodells der Coronavirusinfektion.
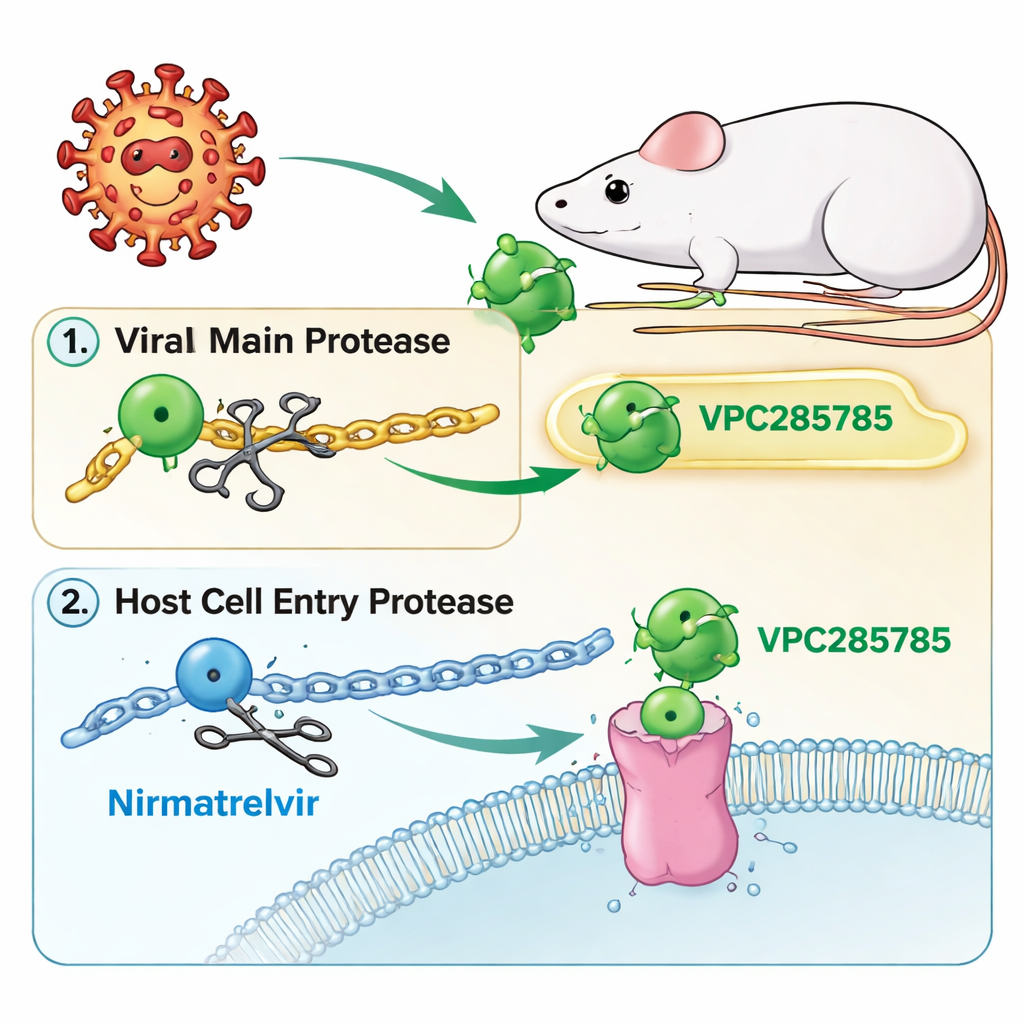
Eine neue Variante des Protease‑Ziels bei COVID‑19
Wie Paxlovid richten sich die neuen Verbindungen — VPC285785 und VPC285786 — gegen die virale „Hauptprotease“, eine molekulare Schere, die lange virale Proteine in funktionelle Teile zerschneidet. Sind diese Scheren blockiert, kann das Virus seine Reifung nicht abschließen und bleibt stehen. Die Forschenden gestalteten die Moleküle außerdem so, dass sie ein zweites Protein in unseren Zellen, Cathepsin L, hemmen, das manchen Coronaviren beim Eindringen hilft. Durch die kombinierte Zielausrichtung auf die virale Schere und einen Wirts‑Eintrittshelfer hoffte das Team, eine Doppelwirkungs‑Pille zu entwickeln, der das Virus schwerer entkommen kann und die keinen Booster benötigt.
Für Beständigkeit gebaut, nicht für einen Booster
Paxlovid kombiniert Nirmatrelvir mit Ritonavir, dessen Aufgabe nicht die antivirale Wirkung ist, sondern den Abbau von Nirmatrelvir in der Leber zu verlangsamen. Ritonavir beeinträchtigt jedoch viele Enzyme, die gängige Medikamente verstoffwechseln, und führt so zu komplexen und teils gefährlichen Wechselwirkungen. VPC285785 und VPC285786 wurden chemisch so optimiert, dass sie von vornherein weniger anfällig für den Abbau sind, etwa durch Fluoratome und Ringversteifung, die sie für Leberenzyme weniger attraktiv machen. In Labortests mit menschlichen und murinen Leberpräparaten erwiesen sich beide neuen Verbindungen als mindestens ebenso stabil wie Nirmatrelvir; VPC285786 war in mancher Hinsicht sogar noch robuster, ganz ohne Ritonavir.
Wie sich die Wirkstoffe bei Mäusen verhalten und verteilen
Das Team untersuchte dann, wie sich die Verbindungen im Körper von Mäusen verhalten, indem es misst, wie schnell sie aus dem Blut verschwinden und wie gut sie oral aufgenommen werden. Nach Injektion blieben VPC285785 und VPC285786 etwa so lange im Blut wie Nirmatrelvir und erzielten insgesamt sogar eine höhere Exposition. Bei oraler Gabe jedoch gingen ihre Wege auseinander: VPC285785 erzielte eine mäßige, aber brauchbare Resorption (etwa 15 % der geschluckten Dosis gelangen in den Kreislauf), während VPC285786 kaum ins Blut gelangte (rund 3 %). Da Tabletten die Darmwand passieren müssen, um praktisch einsetzbar zu sein, wurde nur VPC285785 in die Infektionsversuche weitergeführt.
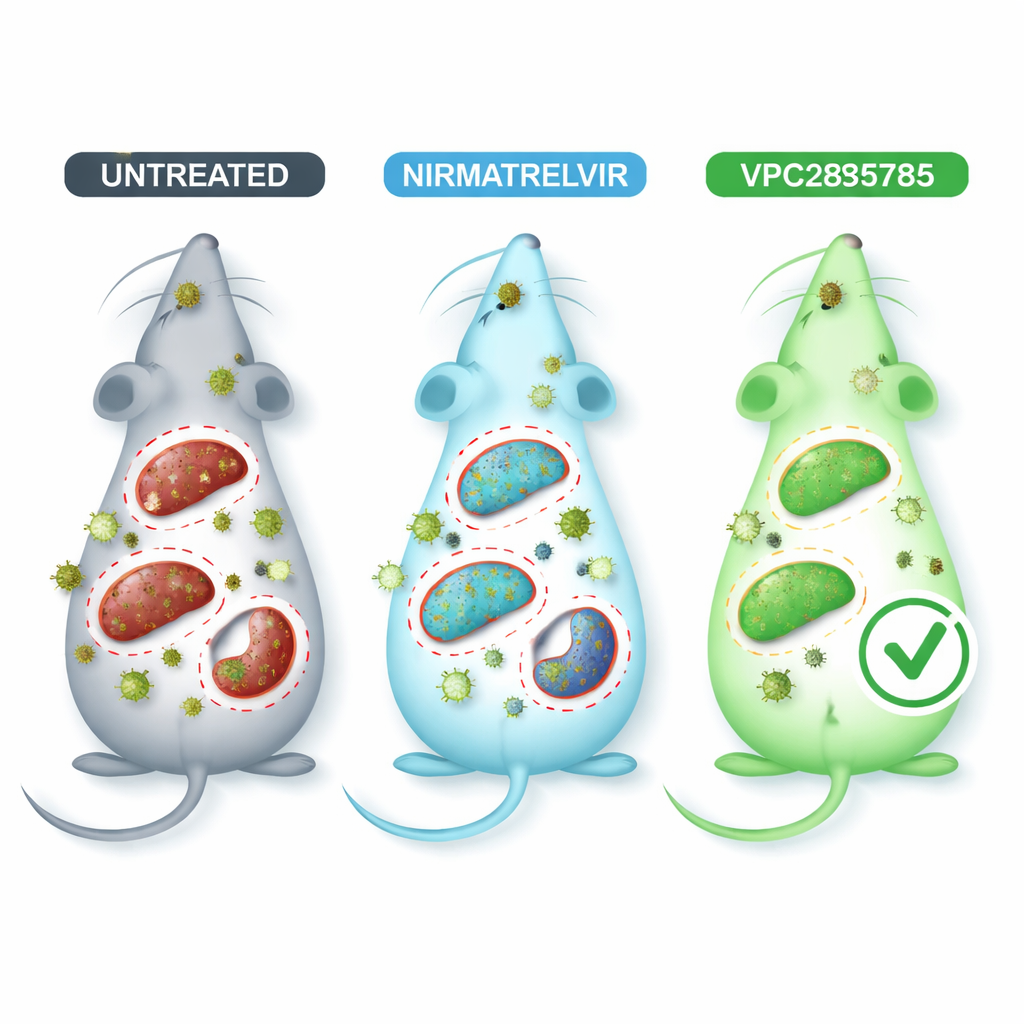
Die neue Pille im Test bei infizierten Mäusen
Um Coronavirerkrankungen in einem sichereren Rahmen nachzuahmen, verwendeten die Forschenden ein Mauscoronavirus namens MHV‑A59, das mehrere Organe befällt und Lungen‑ und Leberschäden verursacht, die in vielerlei Hinsicht der menschlichen Infektion ähneln. Infizierte Mäuse wurden oral mit VPC285785 behandelt, mit Nirmatrelvir zum Vergleich oder mit einem inaktiven Vehikel. Bluttests zeigten, dass die Infektion Leber und Nieren belastete, doch Tiere, die VPC285785 oder Nirmatrelvir erhielten, wiesen tendenziell gesündere Leberenzym‑ und Nierenmarker auf als unbehandelte Mäuse. Am auffälligsten senkte VPC285785 die Menge viraler genetischer Materiale in Leber, Gehirn und Milz deutlich, während Nirmatrelvir einen klaren Rückgang nur im Gehirn bewirkte. In Lunge, Herz und Nieren zeigte unter den getesteten Bedingungen keine der Behandlungen einen starken Effekt.
Was das für künftige COVID‑Behandlungen bedeuten könnte
Obwohl VPC285785 im Reagenzglas weniger potent gegen die virale Protease ist als Nirmatrelvir, zeigt es in lebenden Tieren eine gute Wirksamkeit: Es reduziert die Viruslast in mehreren wichtigen Organen deutlich und erhält die Organfunktionen, alles ohne Ritonavir‑Booster. Die Schwesterverbindung VPC285786 demonstriert, dass eine noch stärkere Doppelzielsetzung von viraler Protease und Cathepsin L möglich ist, ihr mangelhafte Absorption muss jedoch behoben werden. Zusammengenommen deuten diese Ergebnisse darauf hin, dass nächste Generationen von COVID‑Pillen als einzelne, oral verfügbare Wirkstoffe entwickelt werden könnten, die sowohl virale als auch Wirtsziele angreifen, weniger gefährliche Wechselwirkungen mit anderen Medikamenten bieten und dennoch starken Schutz in lebenswichtigen Geweben liefern.
Zitation: Smith, J.R., Toro, A., Sabater, A. et al. Pharmacokinetics, pathology and efficacy of SARS-CoV-2 main protease inhibitor VPC285785 in a murine model of coronavirus infection. Sci Rep 16, 6905 (2026). https://doi.org/10.1038/s41598-026-36842-2
Schlüsselwörter: SARS‑CoV‑2‑Antiviralia, Hauptproteasehemmer, Paxlovid‑Alternativen, murines Coronavirusmodell, orale COVID‑Behandlung