Clear Sky Science · de
YTHDC1 moduliert das maligne Phänotyp des Retinoblastoms über SQSTM1-vermittelte Autophagie
Warum das für kindlichen Augenkrebs wichtig ist
Retinoblastom ist der häufigste Augenkrebs bei Kleinkindern. Wird die Erkrankung früh entdeckt, können Ärzte sie oft heilen; sobald der Tumor jedoch in umliegendes Gewebe einbricht oder in Richtung Gehirn ausbreitet, wird es deutlich schwieriger, sowohl das Leben als auch das Sehvermögen des Kindes zu erhalten. Diese Studie untersucht eine molekulare "Bremse" in Tumorzellen — zwei Moleküle namens YTHDC1 und SQSTM1 — die offenbar dazu beitragen, dass Retinoblastome weniger aggressiv bleiben. Zu verstehen, wie diese Bremse funktioniert, könnte neue Wege für schonendere, gezieltere Therapien eröffnen.
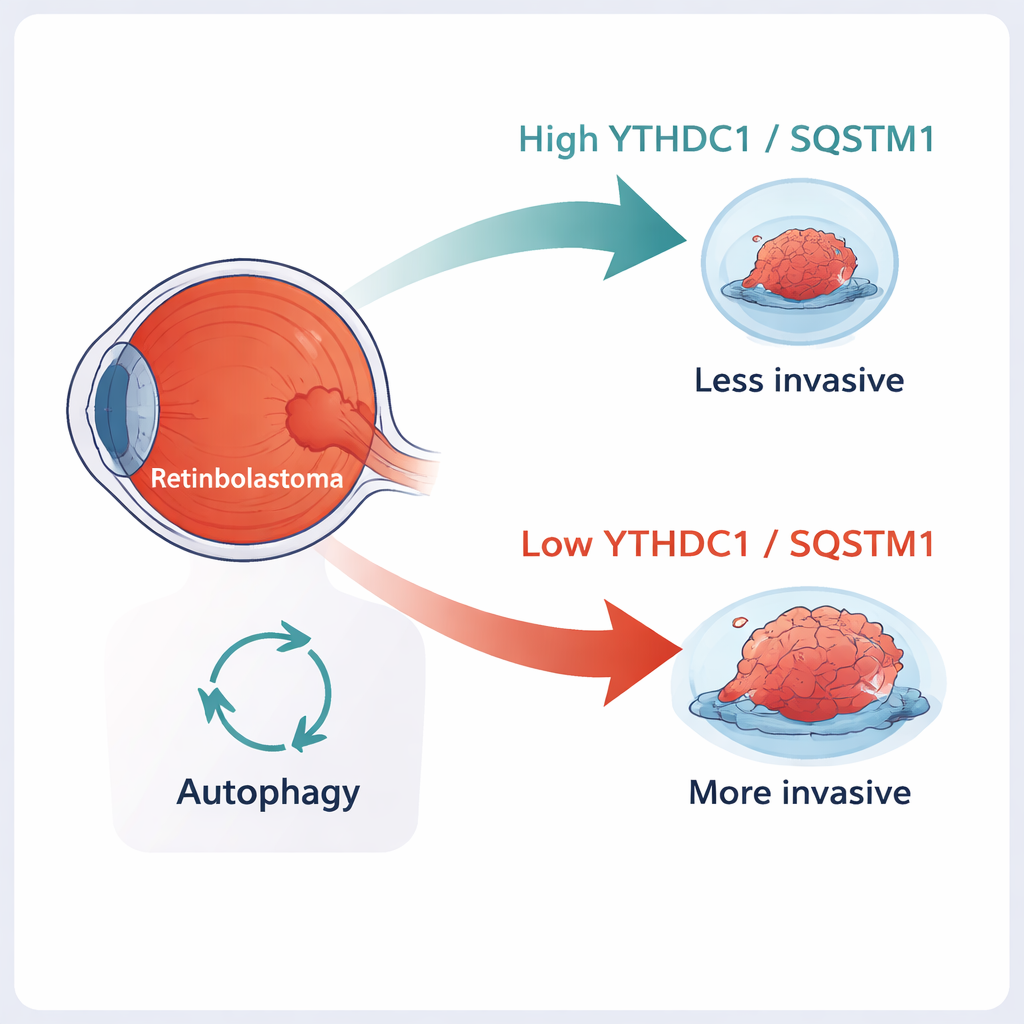
Ein genauerer Blick auf kindliche Augentumoren
Retinoblastom entsteht aus der lichtempfindlichen Schicht des Auges, der Netzhaut, meist bei Kindern unter fünf Jahren. Klassischerweise beginnt die Krankheit, wenn beide Kopien eines Schutz-Gens, RB1, verloren gehen. Aber der Verlust von RB1 erklärt nicht vollständig, warum sich einige Tumoren auf das Auge beschränken, während andere in benachbartes Gewebe eindringen oder dem Sehnerv entlang wandern. Forscher erkennen zunehmend, dass chemische Markierungen auf RNA — die vorübergehenden Botschaften, die Zellen sagen, welche Proteine sie herstellen sollen — stark beeinflussen können, wie sich Krebserkrankungen verhalten. Eine der häufigsten Markierungen, genannt m6A, kann die Stabilität dieser Botschaften und ihre Lebensdauer in der Zelle verändern.
Entdeckung einer fehlenden molekularen Bremse
Die Autoren begannen damit, die Genaktivität in Tumoren zu vergleichen, die im Auge blieben, mit solchen, die bereits invasiv waren. Mithilfe eines öffentlichen RNA-Sequenzierungs-Datensatzes von Retinoblastom-Proben identifizierten sie Tausende von Genen mit unterschiedlicher Aktivität zwischen den Gruppen und konzentrierten sich dann auf wichtige m6A-"Regulatoren". Dazu gehören Enzyme, die m6A hinzufügen oder entfernen, und "Reader"-Proteine, die die Markierung interpretieren. Unter zehn wichtigen Regulatoren stellten sie fest, dass ein Reader, YTHDC1, in invasiven Tumoren durchgehend niedriger war. Als sie Proben von 50 Kindern untersuchten und Labortests an Tumorgewebe durchführten, bestätigten sie, dass die YTHDC1-Spiegel — sowohl RNA als auch Protein — in aggressiveren Tumoren reduziert waren.
YTHDC1 auf dem Prüfstand
Um zu klären, was YTHDC1 tatsächlich bewirkt, manipulierte das Team dessen Spiegel in zwei menschlichen Retinoblastom-Zelllinien. Wenn sie YTHDC1 mittels genetischer Werkzeuge verminderten, teilten sich die Zellen schneller und gelangten leichter durch künstliche Membranen, die Gewebe-Barrieren nachahmen — Anzeichen für einen invasiveren Tumor. In Mäusen bildeten Zellen ohne YTHDC1 größere und schwerere Tumoren. Das Gegenteil war ebenfalls der Fall: Zwingen die Forscher die Zellen, mehr YTHDC1 zu produzieren, verlangsamte sich ihr Wachstum und ihre Wanderungs- und Invasionsfähigkeit nahm ab. Diese Experimente deuten darauf hin, dass YTHDC1 als Tumorsuppressor wirkt und hilft, die gefährlichsten Eigenschaften des Retinoblastoms zu bremsen.
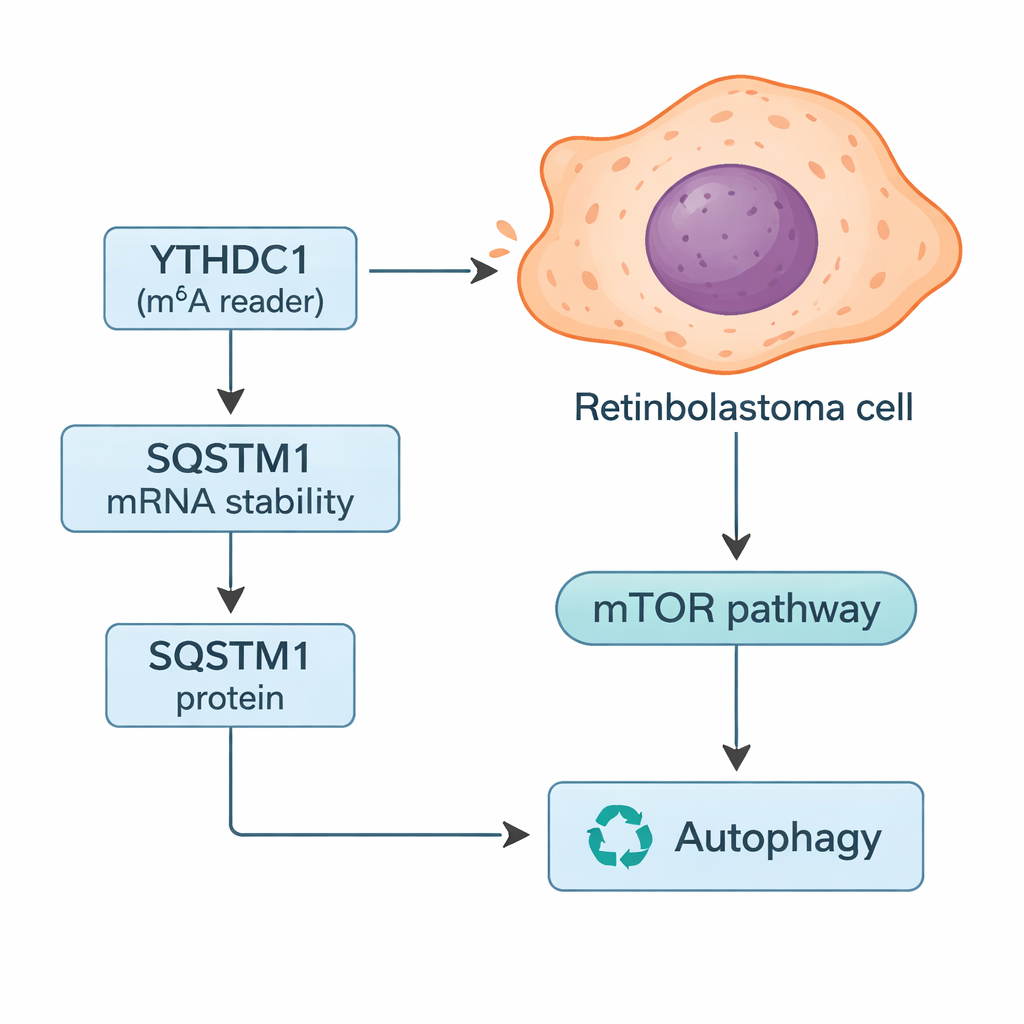
Wie YTHDC1 das Recycling-System der Zelle steuert
Bei tiefergehenden Untersuchungen suchten die Forscher nach spezifischen Genen, deren Botschaften von YTHDC1 kontrolliert werden könnten. Durch die Kombination von Datenbankrecherchen mit ihren Tumordaten konzentrierten sie sich auf SQSTM1, ein Protein, das besser als p62 bekannt ist. SQSTM1 steuert die Autophagie, das Recycling-System der Zelle, das beschädigte Komponenten abbaut und bei knappen Ressourcen als Energiequelle dienen kann. Die Studie zeigte, dass YTHDC1 physisch an die RNA von SQSTM1 bindet und sie stabilisiert, sodass mehr SQSTM1-Protein entsteht. Wenn YTHDC1 reduziert war, sanken die SQSTM1-Spiegel und deren RNA zerfiel schneller. Das alleinige Stummschalten von SQSTM1 ließ Retinoblastom-Zellen stärker wachsen und invasiver werden und hob teilweise die schützenden Effekte auf, die durch YTHDC1-Überexpression beobachtet wurden — SQSTM1 steht damit als zentraler Vermittler in diesem Signalweg.
Autophagie, Energie und Tumoraggressivität
Da SQSTM1 zentral für die Autophagie ist, prüfte das Team, wie sich Änderungen von YTHDC1 und SQSTM1 auf diesen Recycling-Prozess auswirkten. Mithilfe fluoreszenzbasierter Marker und Proteinmessungen fanden sie heraus, dass die Reduktion von entweder YTHDC1 oder SQSTM1 den autophagischen "Fluss" erhöhte — es wurde mehr zelluläres Material in das Recycling-System geleitet und dort verarbeitet. Sie beobachteten außerdem Veränderungen im mTOR-Signalweg, einem wichtigen Nährstoff-Sensor, der normalerweise die Autophagie dämpft. Bei geringerem SQSTM1 nahm die mTOR-Aktivität ab, was einer erhöhten Autophagie entspricht. Bei invasivem Retinoblastom schlagen die Autoren vor, dass reduzierte YTHDC1-Werte zu schwächeren SQSTM1-Signalen, gedämpfter mTOR-Aktivität und verstärkter Autophagie führen, die den Tumorzellen hilft, Stress zu überstehen und sich auszubreiten.
Was das für künftige Behandlungen bedeutet
Für Nicht-Spezialisten lautet die Kernaussage: Diese Studie identifiziert eine Abfolge von Ereignissen in Retinoblastom-Zellen — YTHDC1 steuert SQSTM1, das wiederum das Recycling der Zelle prägt — die beeinflusst, wie aggressiv der Krebs wird. Wird diese Kette geschwächt, wachsen Tumoren schneller und dringen stärker ein. Zwar ist noch viel Arbeit nötig, bevor diese Erkenntnisse klinisch verwertbar sind, doch bietet der Signalweg neue therapeutische Ansatzpunkte: Die Wiederherstellung der YTHDC1-Funktion, die Stabilisierung von SQSTM1 oder das gezielte Einstellen von Autophagie und mTOR-Aktivität könnten eines Tages bestehende Chemotherapien ergänzen. Für betroffene Kinder könnten solche gezielten Strategien helfen, die Tumorausbreitung zu begrenzen, mehr Sehvermögen zu erhalten und Nebenwirkungen der Behandlung zu verringern.
Zitation: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Schlüsselwörter: Retinoblastom, YTHDC1, SQSTM1, Autophagie, mTOR-Signalweg