Clear Sky Science · de
Irisin reguliert den Lipidstoffwechsel und Ferroptose in Eierstockkrebszellen durch Modulation der ALOX5‑5‑HETE‑PD‑L1‑Achse
Warum dieses Pflanzenmolekül für Eierstockkrebs wichtig ist
Eierstockkrebs gehört zu den tödlichsten Krebserkrankungen bei Frauen, weil er meist spät entdeckt wird und nach einer Behandlung häufig zurückkehrt. Diese Studie untersucht, ob eine natürliche Verbindung namens Tectorigenin, die in der Pflanze Belamcanda chinensis vorkommt, das Wachstum von Eierstocktumoren verlangsamen kann, indem sie den Tumorzellen bestimmte Fette entzieht und sie in eine spezielle Form des eisenabhängigen Zelltods zwingt. Außerdem wird geprüft, ob diese Verbindung die „Unsichtbarkeitsglocke“ der Tumoren schwächt, mit der sie sich vor dem Immunsystem verbergen.
Eine verborgene Treibstoffquelle in Tumorzellen
Wie viele andere Krebsarten verändern Eierstocktumoren ihre Fettverarbeitung. Anstatt Fette nur als Energiequelle zu nutzen, legen Krebszellen sie als Bausteine für neue Membranen und als Puffer gegen Schäden an. In im Labor gezüchteten Eierstockkrebszellen führte die Zugabe zusätzlicher einfach ungesättigter Fettsäuren zu einer Anhäufung freier Fettsäuren, Triglyceride und Cholesterin — wichtigen Formen gespeicherter Fette. Dieser Fettüberschuss förderte das Zellwachstum und die Invasionsfähigkeit und half den Zellen, einem zerstörerischen Prozess namens Ferroptose zu widerstehen, bei dem Eisen und oxidierte Fette zur Zerstörung von Zellmembranen führen. Mit anderen Worten: ein gestörter Fettstoffwechsel verlieh dem Krebs einen Wachstums‑ und Überlebensvorteil.
Krebszellen in Richtung Selbstzerstörung drängen
Die Forschenden testeten daraufhin Tectorigenin an normalen Eierstockzellen und mehreren Eierstockkrebszelllinien. Bei Dosen bis zu 200 Mikrogramm pro Liter schadete die Verbindung normalen Zellen nicht, verlangsamte jedoch deutlich das Wachstum der Krebszellen, verringerte ihre Fähigkeit, durch eine Membran zu dringen, und erhöhte ihre Rate programmierter Zellteilung bzw. des Zelltods. Wenn Krebszellen zuvor mit einem Ferroptose‑blocker behandelt wurden, wurden sie aggressiver. Die Zugabe von Tectorigenin kehrte diese Effekte um: Fettdepots sanken, Marker für eisen‑ und oxidationsbedingte Schäden stiegen und mehr Zellen starben. In Mausmodellen mit humanen Eierstocktumoren verkleinerten Injektionen von Tectorigenin die Tumoren, reduzierten den Fettgehalt in Tumorgeweben und verstärkten chemische Hinweise auf Ferroptose, was erneut darauf hindeutet, dass die Verbindung Krebszellen in Richtung dieses eisenabhängigen Todeswegs treibt.
Ein zentraler molekularer Schalter, der Fett und Immunflucht verbindet
Um zu verstehen, wie Tectorigenin auf molekularer Ebene wirkt, kombinierten die Forschenden Big‑Data‑Analysen mit computerbasiertem Modellieren von Wirkstoff‑Protein‑Interaktionen. Sie konzentrierten sich auf ein Enzym namens ALOX5, das eine häufige Fettsäure in das Signalmolekül 5‑HETE umwandelt. In Eierstockkrebszellen und Tumorproben lagen die ALOX5‑Spiegel deutlich höher als im normalen Gewebe. Computer‑Docking und molekulardynamische Simulationen zeigten, dass Tectorigenin stabil an ALOX5 binden kann und so wie eine innere Bremse wirkt. Als die Forschenden ALOX5 künstlich in Krebszellen erhöhten, stiegen die Fettdepots, die Ferroptose‑Marker sanken und die Zellen wurden invasiver. Die Behandlung mit Tectorigenin kehrte diese Veränderungen um. Das Herunterregulieren von ALOX5 führte zum gegenteiligen Effekt — weniger Fett, mehr Ferroptose und geringeres Wachstum — und positioniert dieses Enzym damit klar in der Mitte der Wirkungsweise der Verbindung.
Wie Tumoren ihren Schutz gegen das Immunsystem verlieren
Die Studie verknüpfte diesen Fettstoffwechselweg auch mit einem wichtigen Immun‑Checkpoint‑Molekül namens PD‑L1, das Tumoren nutzen, um angreifende Immunzellen auszuschalten. Das ALOX5‑Produkt 5‑HETE erhöhte die PD‑L1‑Spiegel und stärkte diesen Schutz. Wurde ALOX5 stillgelegt, sanken sowohl 5‑HETE als auch PD‑L1; bei Wiederzufuhr von 5‑HETE stieg PD‑L1 wieder an und die Krebszellen gewannen einen Teil ihres Schutzes vor Ferroptose zurück. Tectorigenin reduzierte ALOX5, senkte 5‑HETE und verringerte folglich PD‑L1 in Zellkulturen und in Maus‑Tumoren. Das legt nahe, dass die gezielte Hemmung eines einzelnen Stoffwechselenzyms sowohl die fettbasierten Abwehrmechanismen des Tumors stören als auch seine Fähigkeit schwächen kann, sich vor Immunangriffen zu verbergen.
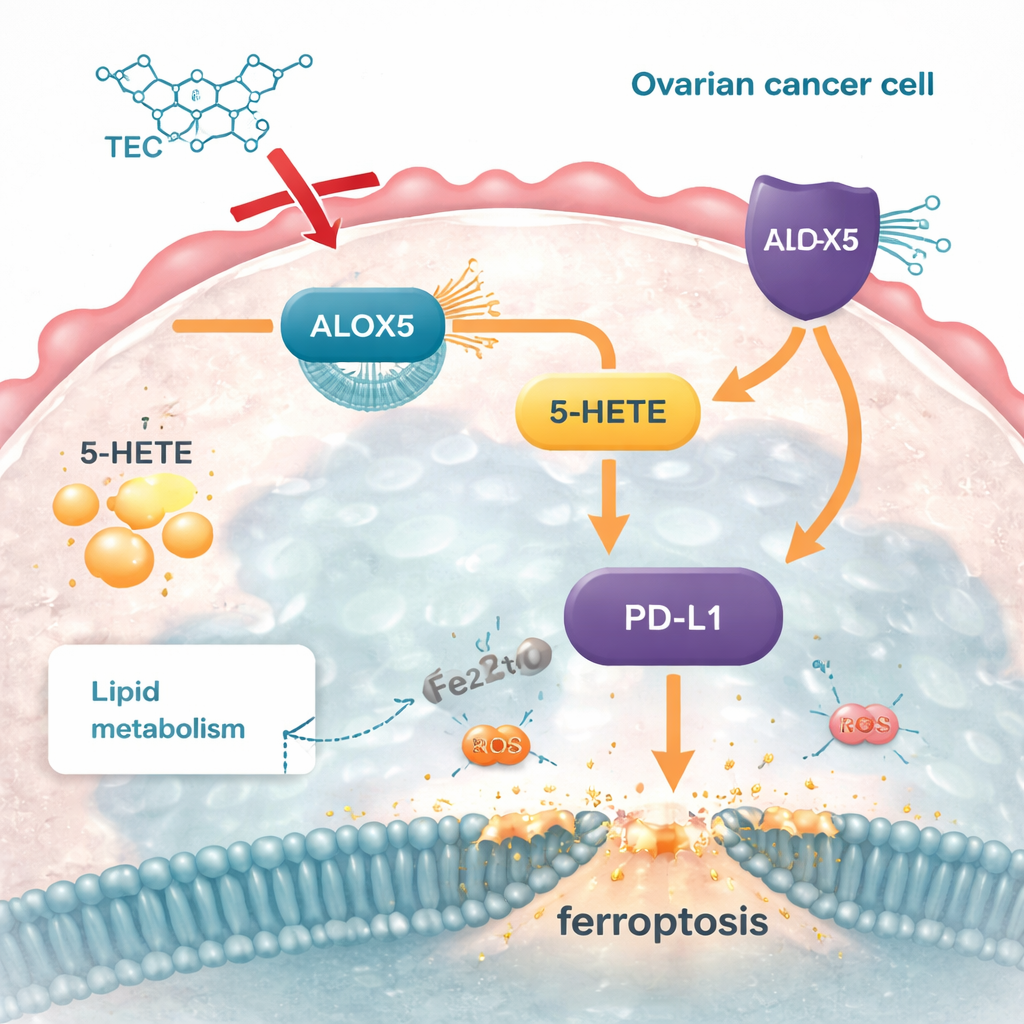
Was das für künftige Therapien bedeuten könnte
Kurz gesagt zeigt diese Arbeit, dass Tectorigenin wie ein präziser Schraubenschlüssel in die Fett‑Verarbeitungsmaschinerie von Krebszellen greift. Durch die Blockade von ALOX5 wird die Produktion von 5‑HETE unterbunden, überschüssige Fettdepots werden abgebaut, die Zellen werden anfällig für eisengetriebene Schäden und ein Teil ihrer immunologischen Tarnung fällt weg. Obwohl diese Befunde aus Zell‑ und Tierstudien stammen und bei Menschen noch viel geprüft werden muss, deuten sie auf eine vielversprechende Strategie hin: Die ALOX5–5‑HETE–PD‑L1‑Achse anzugreifen, um Eierstocktumoren zu schwächen und sie für die körpereigenen Abwehrmechanismen oder zukünftige Immuntherapien besser angreifbar zu machen.
Zitation: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
Schlüsselwörter: Eierstockkrebs, Lipidstoffwechsel, Ferroptose, ALOX5, natürliche Wirkstofftherapie