Clear Sky Science · de
Prophagen‑kodiertes RexAB‑Typ Phagen‑Verteidigungssystem in Pseudomonas putida
Verborgene Leibwächter im Inneren von Bakterien
Bakterien werden ständig von Viren, sogenannten Phagen, bedroht, die ganze mikrobielle Populationen auslöschen können. Diese Studie untersucht, wie „schlafende“ Viren, die bereits in der DNA eines Bakteriums verborgen sind, heimlich als Leibwächter fungieren können, indem sie infizierte Zellen opfern, um den Rest zu retten. Das Verständnis dieser natürlichen Abwehrtricks ist wichtig für Phagentherapien, Biotechnologie und dafür, industrielle Mikroben zuverlässig am Laufen zu halten.
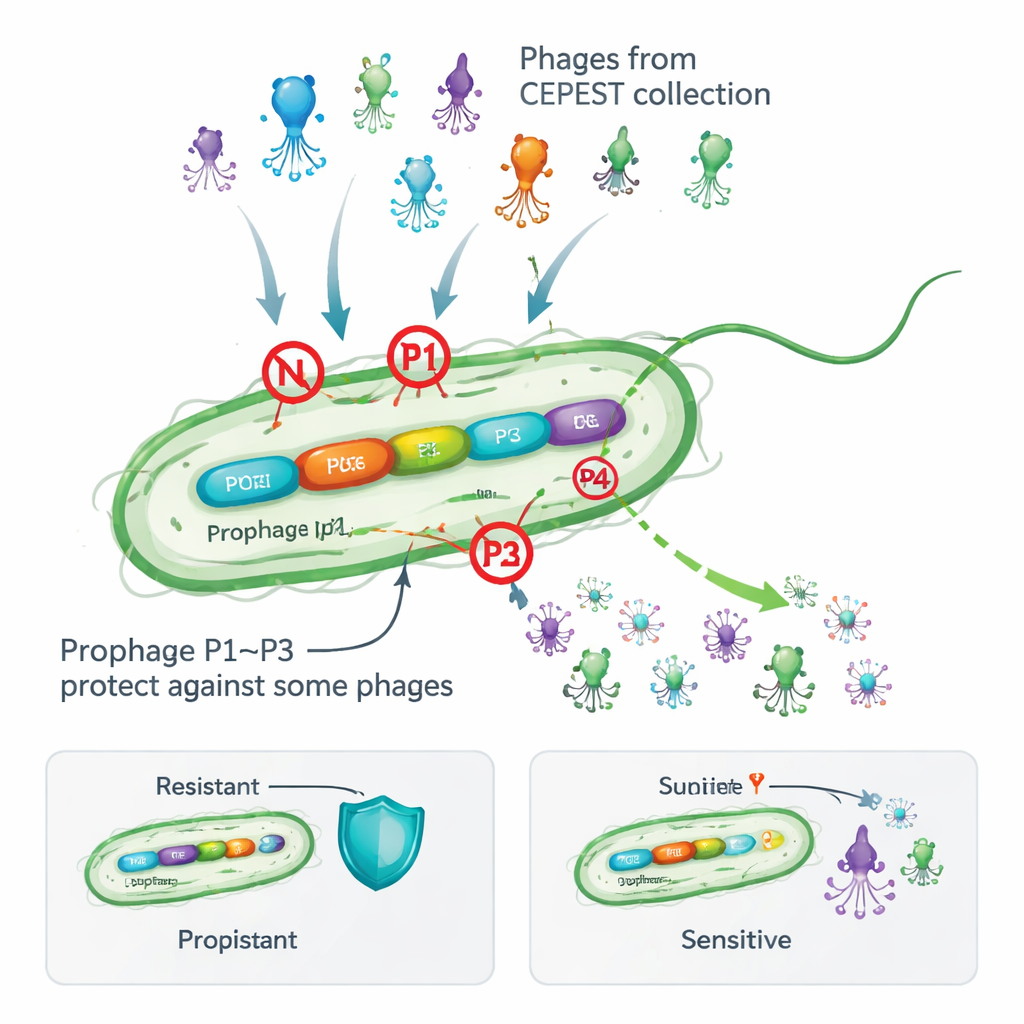
Viren, die sich vom Feind zum Verbündeten wandeln
Viele Bakterien tragen temperente Phagen in einer ruhenden Form, genannt Prophagen, die in ihre Chromosomen eingebettet sind. Auf den ersten Blick wirkt das riskant: diese viralen Mitreisenden können aufwachen und die Wirtszelle schädigen, zudem machen sie das Genom voluminöser. Doch Untersuchungen an Tausenden bakterieller Genome zeigen, dass die meisten Arten solche Prophagen behalten, was dafür spricht, dass sie Vorteile bringen. Frühere Arbeiten am Bodenbakterium Pseudomonas putida zeigten, dass das Entfernen seiner vier kryptischen (nicht produktiven) Prophagen die Zellen anfälliger für Angriffe einer experimentellen Phagensammlung namens CEPEST machte. Das deutete darauf hin, dass die Prophagen Anti‑Phagen‑Waffen tragen, aber die genauen Gene und Mechanismen waren unbekannt.
Drei residente Viren liefern gezielten Schutz
Die Autoren untersuchten den Beitrag jedes Prophagen einzeln, indem sie sie nacheinander löschten und testeten, wie gut 26 verschiedene CEPEST‑Phagen Plaques auf Bakterienteppichen bilden konnten. Sie fanden heraus, dass die Prophagen P1, P2 und P3 jeweils Schutz bieten, aber nur gegen bestimmte Phagengruppen, während P4 neutral zu sein scheint. P1 allein kann die Infektion durch einige Phagen um etwa das Tausendfache reduzieren, P2 bietet einen moderateren Schutz, und P3 ist spektakulär wirksam — jedoch nur gegen bestimmte riesige „Jumbo“‑Phagen. In den meisten Fällen erklärt ein einzelner Prophage das beobachtete Resistenzmuster, obwohl bei einigen Phagen mehrere Prophagen zusammenzuarbeiten scheinen. Diese Ergebnisse zeigen, dass selbst „stille“ Prophagen als maßgeschneiderter Schild gegenüber spezifischen viralen Bedrohungen wirken können.
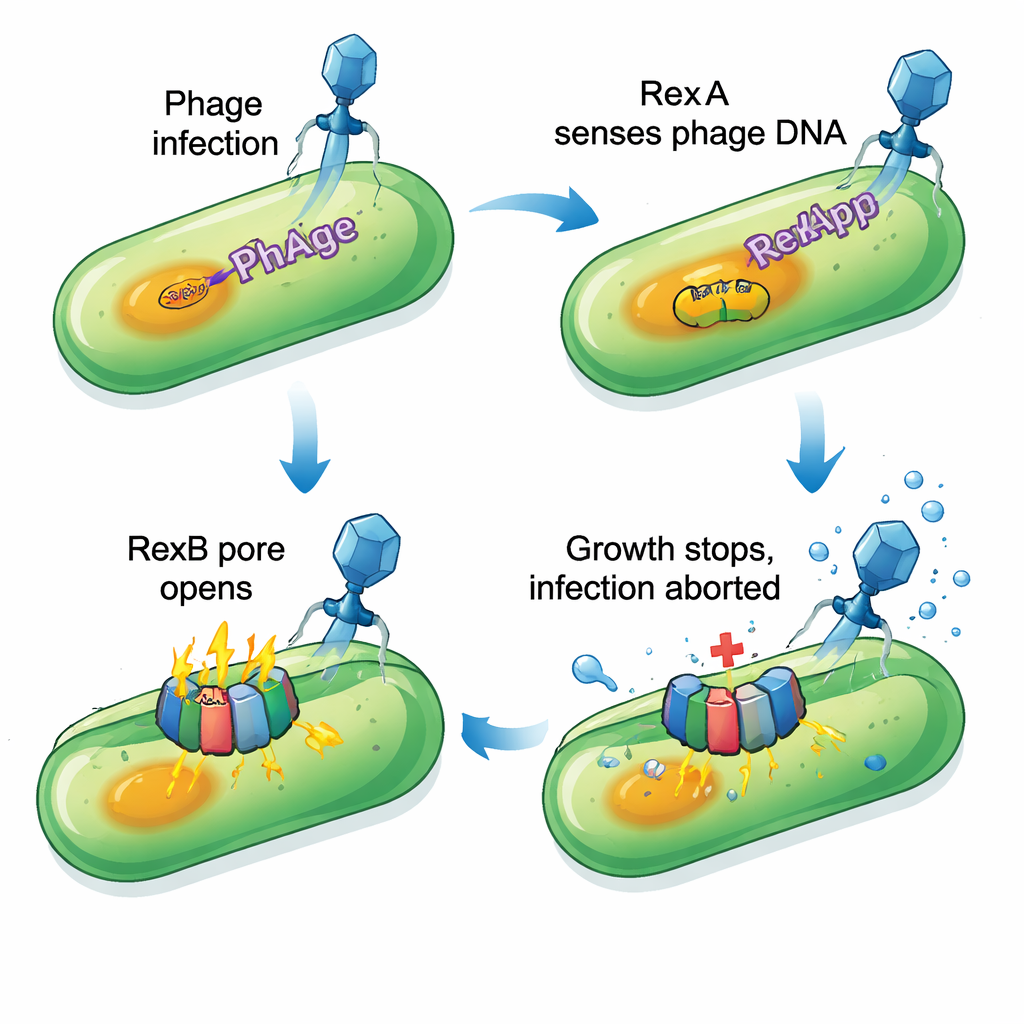
Auf der Spur eines zweiteiligen molekularen Alarms
Mit Fokus auf den starken und relativ breiten Schutz durch P1 löschte das Team systematisch Blöcke von P1‑Genen, bis die Abwehr verschwand. Durch weitere Eingrenzung entdeckten sie, dass schon der Verlust von nur zwei benachbarten Genen, PP_5643 und PP_5644, die Zellen so empfindlich machte wie beim Entfernen des gesamten P1‑Prophagens. Bioinformatische Werkzeuge zeigten, dass PP_5643 RexA ähnelt, einem DNA‑bindenden Protein aus klassischen Lambda‑Phagen‑Studien, während PP_5644 wie ein Membranprotein mit mehreren Helices aussieht, das eine Pore bilden könnte, ähnlich RexB. Zusammen passt dieses Paar zu einem bekannten Typ von „abortive infection“‑System: Wird ein spezifischer Phage erkannt, stoppt die infizierte Zelle absichtlich ihr eigenes Wachstum, sodass sich der Virus nicht vermehren und auf Nachbarzellen ausbreiten kann.
Wie die Abwehr infizierte Zellen sabotiert
Experimente bestätigten, dass die P1‑Variante von RexA (genannt RexApp) DNA bindet, ohne stark auf eine bestimmte Sequenz angewiesen zu sein, was sie geeignet macht, ungewöhnliche DNA‑Strukturen zu erkennen, die während der viralen Replikation entstehen. Das Partnerprotein RexBpp ist in der Zellmembran verankert. Wenn RexApp künstlich überproduziert wird, zeigen Zellen, die noch das rexBpp‑Gen tragen, starke Wachstumshemmung und Anzeichen von Membranschäden: Farbstoffe, die normalerweise intakte Membranen nicht passieren, dringen plötzlich ein, und kleine Mengen eines zytoplasmatischen Enzyms treten aus. Fehlt rexBpp oder ist es mutiert, schadet die Überproduktion von RexApp den Zellen nicht mehr. Das deutet darauf hin, dass RexApp als Auslöser wirkt, während RexBpp der Effektor ist, der die Zellhülle schädigt. Interessanterweise platzen die meisten betroffenen Zellen nicht vollständig; stattdessen treten sie in einen stark verlangsamten, nahezu stationären Zustand ein, der offenbar mit der Vermehrung von Phagen unvereinbar ist.
Warum das Aufgeben weniger Zellen die Population retten kann
Das entstehende Bild ist das einer altruistischen Abwehr: Wenn ein sensibler Phage P. putida infiziert, erkennt RexApp vermutlich virale DNA‑Protein‑Komplexe und schaltet RexBpp ein, das die Membran kompromittiert und das Wachstum abrupt stoppt. Die infizierte Zelle zahlt den Preis, aber der Phagenlebenszyklus wird abgebrochen und die breitere bakterielle Gemeinschaft geschützt. Systeme dieses RexAB‑Typs wurden bisher nur in einer Handvoll verschiedener Phagen gefunden, teilen jedoch die gleiche Grundlogik — einen intrazellulären Sensor, gekoppelt mit einem Membran‑Effektor, der schnell eine produktive Zelle in eine Sackgasse für das Virus verwandeln kann. Für Bakterien kann das Behalten kryptischer Prophagen, die solche Abwehrmodule tragen, die Kosten des Tragens viraler DNA ausgleichen und ihnen helfen, in einer von Phagen dominierten Welt zu überleben.
Zitation: Rosendahl, S., Kängsep, A., Ainelo, A. et al. Prophage-encoded RexAB-type phage defense system in Pseudomonas putida. Sci Rep 16, 5898 (2026). https://doi.org/10.1038/s41598-026-36734-5
Schlüsselwörter: Abwehr gegen Bakteriophagen, Prophage, Pseudomonas putida, abortive Infektion, RexAB‑System