Clear Sky Science · de
Entwicklung und Validierung eines PSMA-positiven Triple-negativen Mammakarzinom-Mausmodells für präklinische zielgerichtete Radionuklidtherapien
Warum diese Forschung wichtig ist
Triple-negativer Brustkrebs ist eine der schwersten Formen von Brustkrebs zu behandeln. Er neigt dazu, sich schnell auszubreiten, bietet den Patienten weniger gezielte Behandlungsoptionen und kommt nach Standardtherapien häufig zurück. Gleichzeitig hat eine neue Klasse von „intelligenten“ Strahlenmedikamenten, die an ein spezifisches Molekül namens PSMA andocken, die Behandlung fortgeschrittener Prostatakrebserkrankungen revolutioniert. Diese Studie stellt eine einfache, aber entscheidende Frage: Können wir ein realistisches Labor-Modell des triple-negativen Brustkrebses entwickeln, das dasselbe PSMA-Ziel trägt, damit wir verlässlich prüfen können, ob diese intelligenten Strahlenmedikamente auch bei dieser aggressiven Form von Brustkrebs helfen könnten?
Vom Prostataziel zur Herausforderung des Brustkrebses
PSMA, kurz für prostataspezifisches Membranantigen, ist eine kleine Struktur an der Oberfläche bestimmter Zellen. Es ist in vielen Prostatakrebserkrankungen reichlich vorhanden und kann von radioaktiven Wirkstoffen erkannt werden, die Tumore sowohl in Scanbildern sichtbar machen als auch gezielt bestrahlen. Forscher haben kürzlich entdeckt, dass PSMA auch in unterschiedlichem Maße in den Blutgefäßen und Zellen mehrerer anderer Tumoren vorkommt, darunter beim triple-negativen Brustkrebs. In diesen nicht-prostatischen Tumoren ist PSMA jedoch oft ungleichmäßig und schwächer ausgeprägt, was es schwer macht einzuschätzen, ob PSMA-gerichtete Therapien wirksam sein werden. Bevor neue Behandlungen am Menschen erprobt werden, benötigen Wissenschaftler Tiermodelle, die dieses PSMA-Muster in Brusttumoren treu nachbilden — etwas, das sich überraschend schwer realisieren ließ.
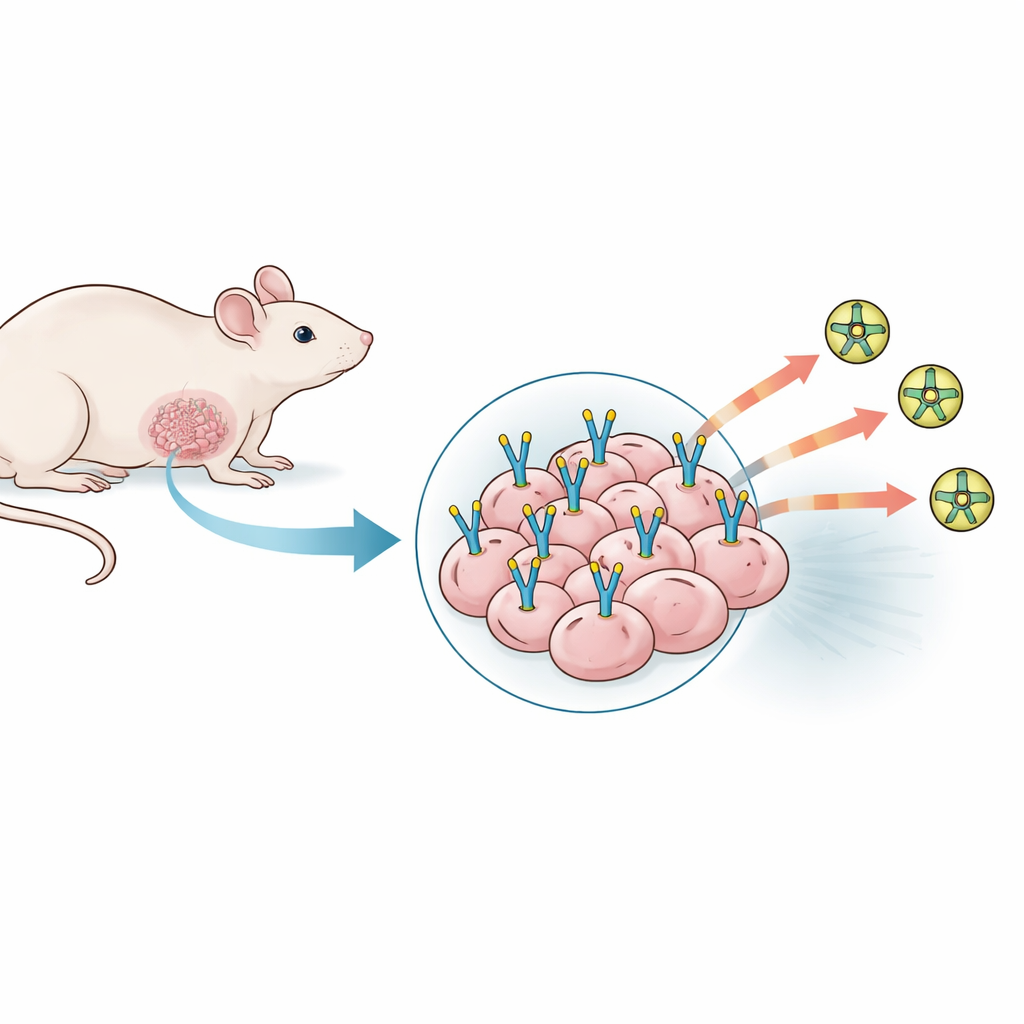
Viele Tumormodelle getestet, die nicht kooperieren wollten
Das Team untersuchte zunächst eine breite Palette vorhandener Mausmodelle für triple-negativen Brustkrebs, indem sowohl Maus- als auch menschliche Krebszelllinien an verschiedenen Stellen und unter unterschiedlichen Bedingungen implantiert wurden. Sie variierten die Anzahl der injizierten Krebszellen, fügten unterstützende Gele zur Förderung der Gefäßbildung hinzu und mischten sogar menschliche Blutgefäßzellen bei, um PSMA-Spiegel zu erhöhen. Für jedes Modell maßen sie, wie zuverlässig Tumore angelegt wurden und wuchsen, untersuchten Tumorschnitte mikroskopisch und nutzten einen PSMA-suchenden PET-Tracer, um zu sehen, ob die Tumore im Ganzkörper-Scan aufleuchteten. Trotz kräftigen Tumorwachstums und gut ausgebauter Gefäßnetze zeigte keines dieser 23 Modelle eine nennenswerte PSMA-Präsenz, weder in der Gewebeanfärbung noch in der PET-Bildgebung. Die Tumore wirkten aktiv und gut durchblutet, aber die spezifische PSMA-„Andockstelle“, die die Forscher benötigten, war im Wesentlichen nicht vorhanden.
Ein Tumor, der das richtige Ziel zeigt, wird gezielt erzeugt
Angesichts dieser Blockade gingen die Forscher einen direkteren Weg. Sie modifizierten genetisch eine weit verbreitete menschliche Triple-negativ-Zelllinie, MDA-MB-231, sodass sie gezwungen wurde, PSMA an ihrer Oberfläche zu produzieren. Diese veränderten Zellen wurden dann in das Fettpolster der Mamma immunsupprimierter Mäuse implantiert, ein Ort, der die natürliche Brustumgebung besser nachahmt. Die Wissenschaftler schufen zwei Varianten des Modells: eine, in der alle Tumorzellen PSMA exprimierten, und ein „gemischtes“ Tumormodell mit gleichen Anteilen PSMA-positiver und gewöhnlicher Krebszellen, um die fleckigen Muster zu imitieren, die bei Patienten beobachtet werden. Beide Modelle bildeten Tumore ebenso zuverlässig und wuchsen mit ähnlichen Geschwindigkeiten wie Tumore aus unveränderten Zellen, was zeigte, dass die Zufuhr von PSMA das Verhalten des Krebses selbst nicht ungewöhnlich veränderte.
Den neuen Zielmarker in Scans und unter dem Mikroskop sehen
Als der PSMA-gerichtete PET-Tracer in diese Mäuse injiziert wurde, leuchteten die konstruierten Tumore im Scan deutlich auf, mit einer Tumoraufnahme, die grob zehnmal höher war als in Leber oder Muskel. Dieses starke und selektive Signal bestätigte, dass PSMA nun reichlich auf den Krebszellen vorhanden war und von einem zirkulierenden Wirkstoff erreicht werden konnte. Mikroskopische Analysen des Tumorgewebes stimmten überein: Die PSMA-Färbung war hoch, aber ungleichmäßig, mit Flecken stärkerer und schwächerer Expression, die dem heterogenen Muster ähnelten, das bei menschlichen triple-negativen Brustkrebserkrankungen beobachtet wird. Wichtig war, dass das zugefügte PSMA auf Tumorzellen beschränkt blieb und nicht auf die umliegenden Blutgefäße überging, wodurch das Modell auf zellgerichtete Therapien fokussiert blieb. Bereiche abgestorbenen Gewebes in größeren Tumoren nahmen den Tracer nicht auf, was den klinisch beobachteten Befunden entspricht.
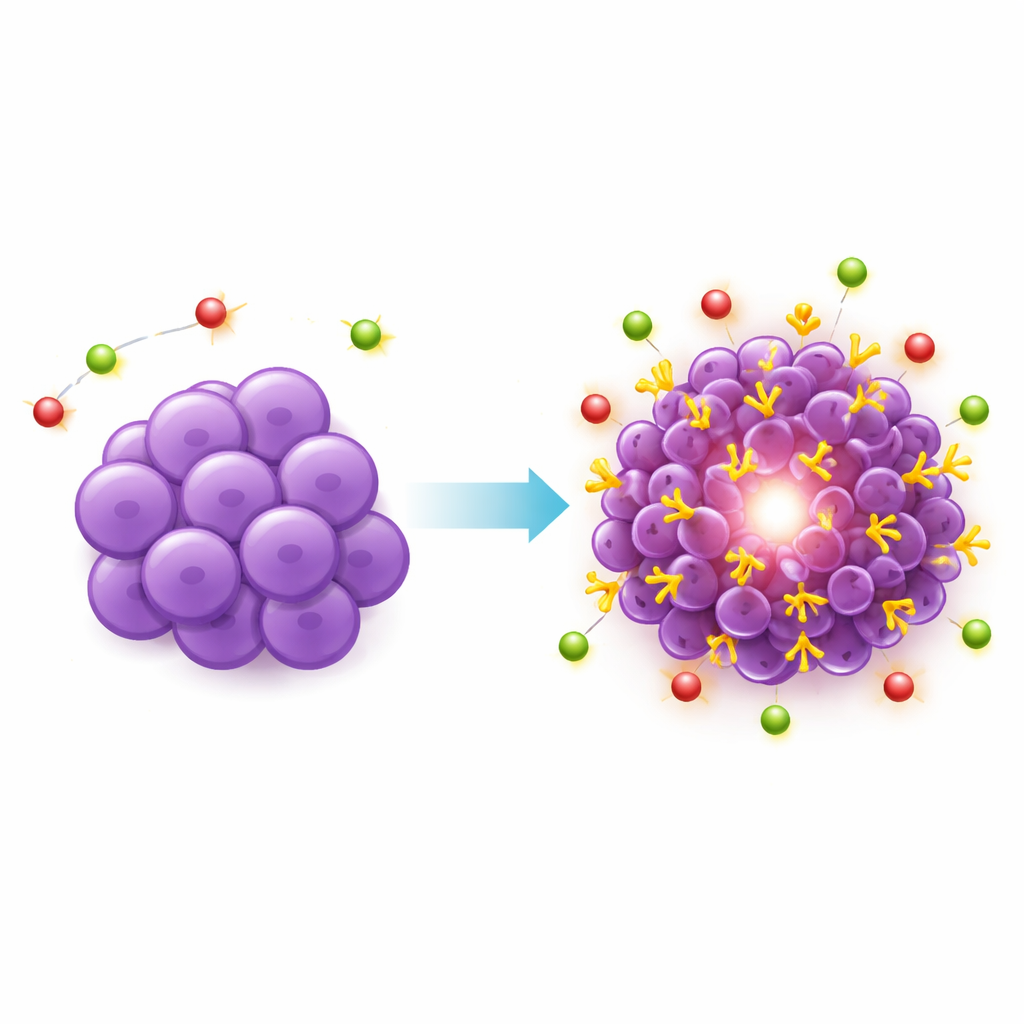
Was das für künftige Behandlungen bedeutet
Indem sie systematisch zeigen, dass Standard-Mausmodelle für Brustkrebs PSMA nicht zuverlässig exprimieren, und anschließend ein neues Modell entwickeln, das dies tut, liefern die Autoren eine entscheidende Testumgebung für die nächste Generation zielgerichteter Strahlenbehandlungen. Das PSMA-positive Triple-negativ-Mammakarzinom-Modell ist stabil, wächst vorhersehbar und weist eine realistische Mischung aus Bereichen mit hoher und niedriger PSMA-Expression auf, wodurch es sich gut eignet, das Verhalten PSMA-gerichteter Wirkstoffe zu beurteilen, bevor diese am Menschen erprobt werden. Obwohl dieses Modell nicht jeden Aspekt der menschlichen Erkrankung abbilden kann — etwa den Einfluss eines vollständig funktionierenden Immunsystems — bietet es ein kraftvolles Werkzeug, um zu untersuchen, ob der Erfolg PSMA-basierter Therapien beim Prostatakrebs eines Tages auch auf Menschen mit dieser besonders aggressiven Form von Brustkrebs übertragbar sein könnte.
Zitation: Chaussin, B., Sanchez, L., Levesque, S. et al. Development and validation of a PSMA-positive triple-negative breast cancer mouse model for preclinical targeted radionuclide therapies. Sci Rep 16, 9348 (2026). https://doi.org/10.1038/s41598-026-36724-7
Schlüsselwörter: triple-negativer Brustkrebs, PSMA, zielgerichtete Radionuklidtherapie, präklinisches Mausmodell, PET-Bildgebung