Clear Sky Science · de
Herunterregulierung der langen Isoform der WNK1-Kinase mildert die anti-glomeruläre Basalmembran-Glomerulonephritis bei Mäusen
Warum das für die Nierengesundheit wichtig ist
Schnell verlaufende Nierenerkrankungen können die winzigen Filter des Organs innerhalb weniger Wochen zerstören und führen oft zu Dialyse oder Transplantation. Diese Studie untersucht, ob die Herunterregulierung eines einzelnen Proteins, genannt L‑WNK1, diese Zerstörung bei Mäusen verlangsamen kann. Da Wirkstoffe gegen dieses Protein bereits zur Behandlung von Blutdruckproblemen entwickelt werden, deuten die Ergebnisse auf einen möglichen neuen Ansatz hin, die Niere bei Angriffen zu schützen.
Ein Verkehrsregler in den Nierenfiltern
Jede Niere enthält Hunderttausende mikroskopischer Filter, die Glomeruli, die das Blut reinigen. Innerhalb dieser Filter arbeiten zwei wichtige Zelltypen zusammen: Podocyten, die sich wie ineinandergreifende Finger um Blutgefäße legen, und parietale Epithelzellen (PECs), die die äußere Hülle auskleiden. In einer gefährlichen Erkrankung, der schnell progredienten Glomerulonephritis (RPGN), werden Podocyten geschädigt und PECs überaktiv, sodass sie sich zu "Halbmond"-Formationen anhäufen, die die Filtration blockieren. Das Protein L‑WNK1, ein Signalschalter, der vor allem für seine Rolle bei Salz‑ und Blutdruckregulation bekannt ist, wird tatsächlich in hohen Mengen in diesen glomerulären Zellen gebildet. Die Autoren fragten, ob zu viel L‑WNK1 RPGN verschlimmert und ob seine Reduktion die Erkrankung abschwächen könnte.
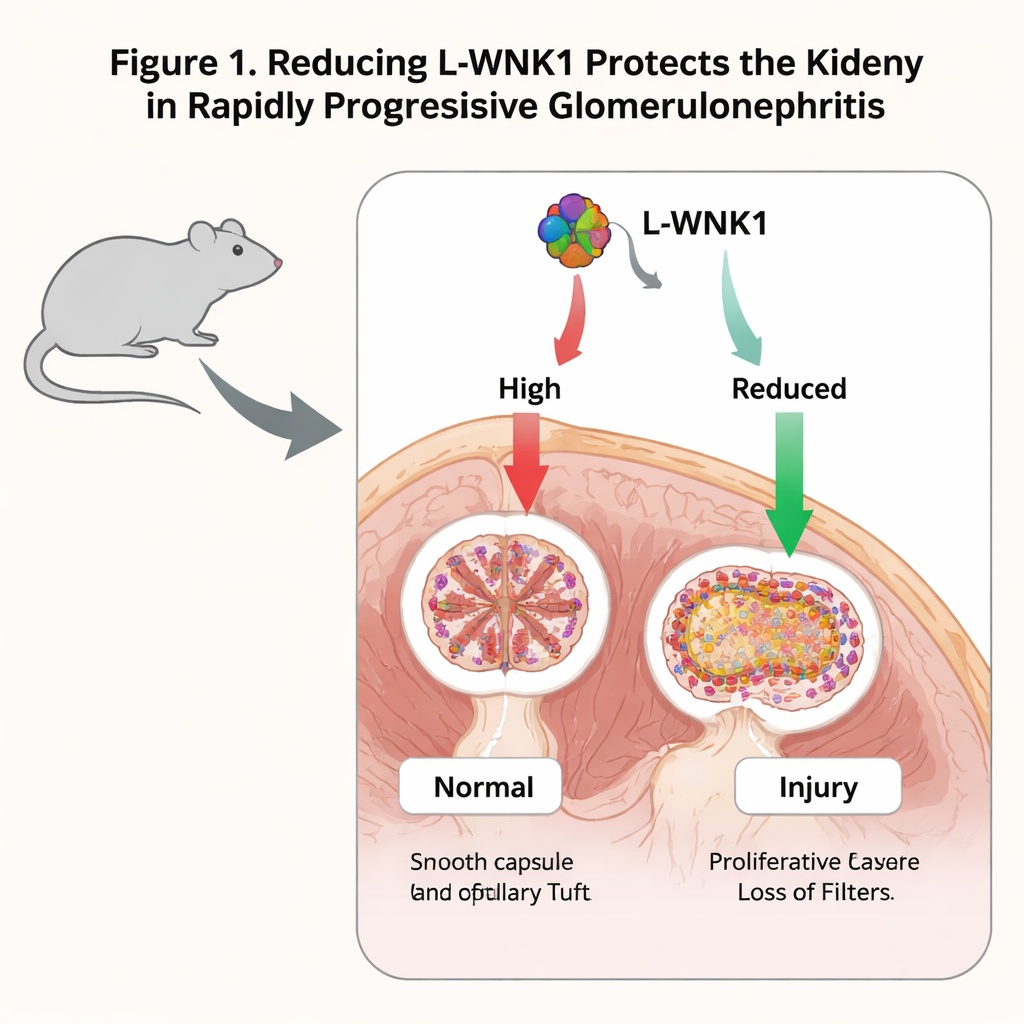
Herunterdrehen von L‑WNK1 lindert Nierenschäden bei Mäusen
Die Forschenden verwendeten zunächst ein klassisches Mausmodell der RPGN, ausgelöst durch Antikörper, die die glomeruläre Basalmembran, einen wichtigen Filterbestandteil, angreifen. Sie fanden, dass die L‑WNK1-Spiegel in den Glomeruli nach der Schädigung anstiegen — nicht nur bei Mäusen, sondern auch in Nierenbiopsien von Patientinnen und Patienten mit verwandten Erkrankungen. Um Ursache und Wirkung zu prüfen, untersuchten sie Mäuse, die nur mit einer funktionierenden Kopie des L‑WNK1-Gens geboren wurden. Diese Tiere entwickelten nach Antikörperverletzung Nierenversagen, aber ihre Blutwerte waren weniger stark erhöht und ihr Nierengewebe zeigte weniger Halbmonde und weniger Vernarbung als bei normalen Mäusen. Entzündungs‑ und Fibrosemarker, wie die Signalmoleküle MCP‑1, TGF‑β1 und Kollagen‑Gene, waren ebenfalls reduziert. Zusammengenommen deutet dies darauf hin, dass ein teilweiser Verlust von L‑WNK1 die Erkrankung abschwächt, statt sie zu verschlechtern.
Zoom auf Podocyten und ihre Nachbarn
Da Podocyten zentral für die Glomerulusfunktion sind und L‑WNK1 stark exprimieren, entferzte das Team als Nächstes WNK1 gezielt aus diesen Zellen mittels eines genetischen Tricks. Unter normalen Bedingungen hatten diese Mäuse gesunde Nieren, was zeigt, dass Podocyten L‑WNK1 für Entwicklung und alltägliche Funktion nicht benötigen. Nach Induktion der RPGN schnitten die podocyten‑spezifischen Knockout‑Mäuse wieder besser ab als Kontrollen: Ihre Blutwerte verbesserten sich und sie zeigten tendenziell weniger Halbmonde und weniger PECs, die CD44 exprimieren — ein Aktivierungsmarker. Der Schutz war jedoch schwächer als bei Mäusen mit der breiteren, körpereigenen Reduktion von L‑WNK1, und die Spiegel einiger Entzündungsmarker fielen nicht. Das deutet darauf hin, dass L‑WNK1 nicht nur in Podocyten, sondern auch in anderen glomerulären oder immunologischen Zellen eine Rolle spielt, die an der Erkrankung beteiligt sind.
Verlangsamung schädlicher Zellbewegung
Um zu erforschen, wie L‑WNK1 die Halbmondbildung fördern könnte, gingen die Wissenschaftler zu Zellkulturen über. Mit einem niedermolekularen Wirkstoff, der WNK‑Kinasen blockiert, behandelten sie in vitro gezüchtete menschliche Podocyten und beobachteten, wie schnell diese in eine künstliche "Wund"‑Lücke einwanderten. Das Blockieren der L‑WNK1‑Aktivität verlangsamte ihre Bewegung deutlich. Einen ähnlichen Effekt sahen sie in kultivierten PECs: Normalerweise breiten sich PECs nach Zugabe eines Wachstumsfaktors aus, um die Lücke zu schließen, doch diese Reaktion war abgeschwächt, wenn der WNK‑Inhibitor vorhanden war. Interessanterweise störte das Medikament in ihrem System das innere Gerüst der Podocyten nicht auffällig, obwohl frühere Arbeiten an Maus‑Zellen größere strukturelle Probleme nahegelegt hatten. Das stützt die Idee, dass L‑WNK1 in lebenden Organismen vor allem die Bewegung und Reaktion glomerulärer und immunologischer Zellen während der Schädigung steuert, statt die grundlegende Filterarchitektur zu erhalten.
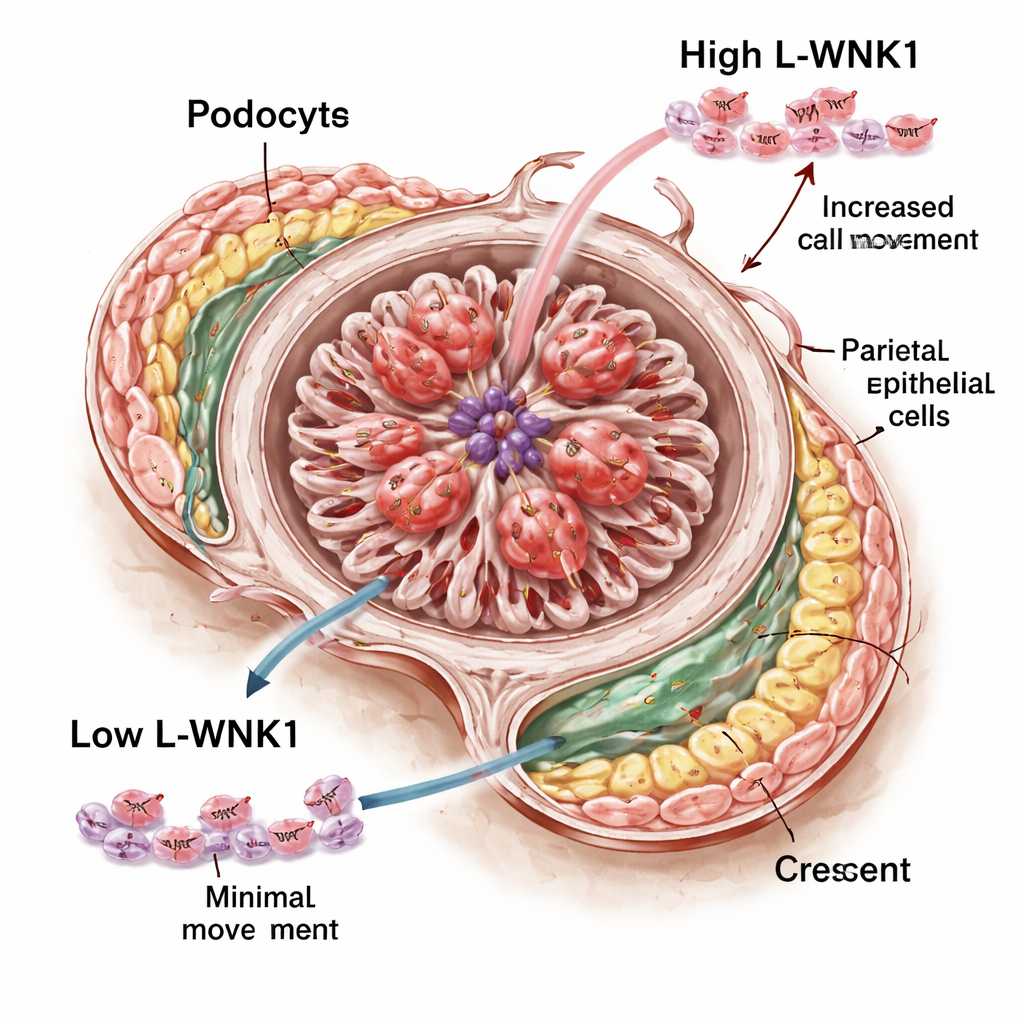
Was das für künftige Therapien bedeutet
Insgesamt zeigt die Studie L‑WNK1 als schädlichen Beschleuniger einer heftigen Form der Nierenentzündung: Wenn dieses Protein erhöht ist, bewegen und vermehren sich Schlüsselzellen im Glomerulus so, dass Filter verstopfen und vernarben; ist seine Aktivität reduziert, wird der Schaden gemildert. Da L‑WNK1 bereits als Arzneimittelziel für den Blutdruck untersucht wird, eröffnen diese Befunde die Möglichkeit, dass sorgfältig abgestimmte Inhibitoren eines Tages Patientinnen und Patienten mit schnell verlaufenden Nierenerkrankungen schützen könnten. Es bedarf noch erheblicher Arbeit, um Maus‑ und Zellkulturbefunde in sichere Therapien zu übersetzen, doch L‑WNK1 fällt nun als vielversprechender neuer Ansatzpunkt bei einer sonst verheerenden Erkrankung auf.
Zitation: Mousseaux, C., Migeon, T., Frère, P. et al. Knock-down of the long isoform of the WNK1 kinase mitigates the anti-glomerular basement membrane glomerulonephritis in mice. Sci Rep 16, 7335 (2026). https://doi.org/10.1038/s41598-026-36715-8
Schlüsselwörter: schnell progrediente Glomerulonephritis, Nierenentzündung, Podocyten, glomeruläre Halbmonde, WNK1-Hemmung