Clear Sky Science · de
Identifizierung und Verifikation von SPP1 bei Anoikis als prognostischer Biomarker für intestinale Metaplasie und Magenkrebs
Warum das für die Magengesundheit wichtig ist
Magenkrebs gehört zu den tödlichsten Krebsarten weltweit, vor allem weil er meist spät entdeckt wird. Bevor ein ausgewachsener Tumor entsteht, durchläuft die Magenschleimhaut häufig eine Warnstufe, die als intestinale Metaplasie bezeichnet wird, bei der normale Magenzellen beginnen, Darmschleimhautzellen zu ähneln. Diese Studie verfolgt den gesamten Verlauf — von gesundem Gewebe über intestinale Metaplasie bis hin zu Magenkrebs — um ein einzelnes messbares Signal im Gewebe zu finden, das frühzeitig ein hohes Risiko anzeigen könnte und Ärzten helfen würde, vorherzusagen, welche Patienten voraussichtlich schlechtere Prognosen haben und von engerer Nachsorge oder neuen Therapien profitieren könnten.
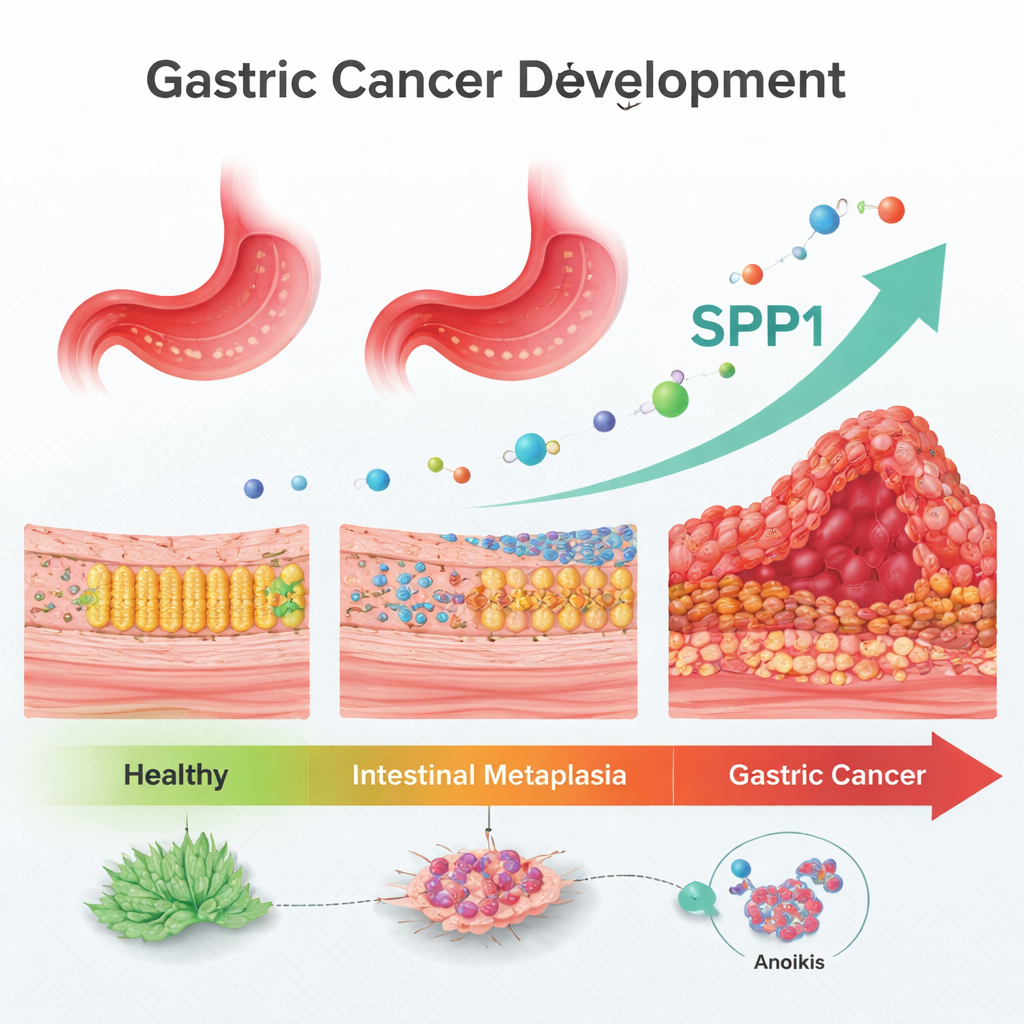
Ein Zwischenschritt auf dem Weg zum Krebs
Ärztinnen und Ärzte wissen seit langem, dass intestinale Metaplasie eine prämaligne Veränderung ist, doch fehlen verlässliche Marker, um vorherzusagen, wer tatsächlich zu Krebs fortschreitet. Die Forschenden konzentrierten sich auf eine Form des Zelltods namens Anoikis, die normalerweise Zellen abtötet, die sich von ihrem richtigen Ort im Gewebe lösen. Krebszellen müssen Anoikis widerstehen lernen, um sich zu bewegen, im Blut überleben zu können und entfernte Tumoren zu bilden. Durch die Auswertung großer öffentlicher Gen-Datenbanken aus Hunderten von Patienten suchte das Team nach anoikis-assoziierten Genen, die sich stetig entlang der „Correa-Kaskade“ verändern: gesunde Magenschleimhaut, intestinale Metaplasie und schließlich Magenkrebs.
Fokussierung auf ein zentrales Warnmolekül
Mithilfe fortgeschrittener statistischer Werkzeuge und Netzwerk‑Analysen identifizierten die Wissenschaftler wiederholt ein auffälliges Gen: SPP1, das für das Protein Osteopontin kodiert. In drei unabhängigen Datensätzen waren die SPP1-Werte konsistent niedrig im gesunden Magengewebe, erhöht bei intestinaler Metaplasie und am höchsten beim Magenkrebs. Dieses stufenweise Muster hielt auch nach Korrektur technischer Unterschiede zwischen den Studien stand. Weitere Rechenanalysen von Tausenden Genen zeigten, dass hohe SPP1-Spiegel oft zusammen mit Veränderungen in immunbezogenen Signalwegen und Reaktionen auf Umwelt‑ und chemischen Stress auftraten, was nahelegt, dass das Molekül Zellüberleben, chronische Reizung und das Immunsystem während der Krebsentstehung miteinander verknüpfen könnte.
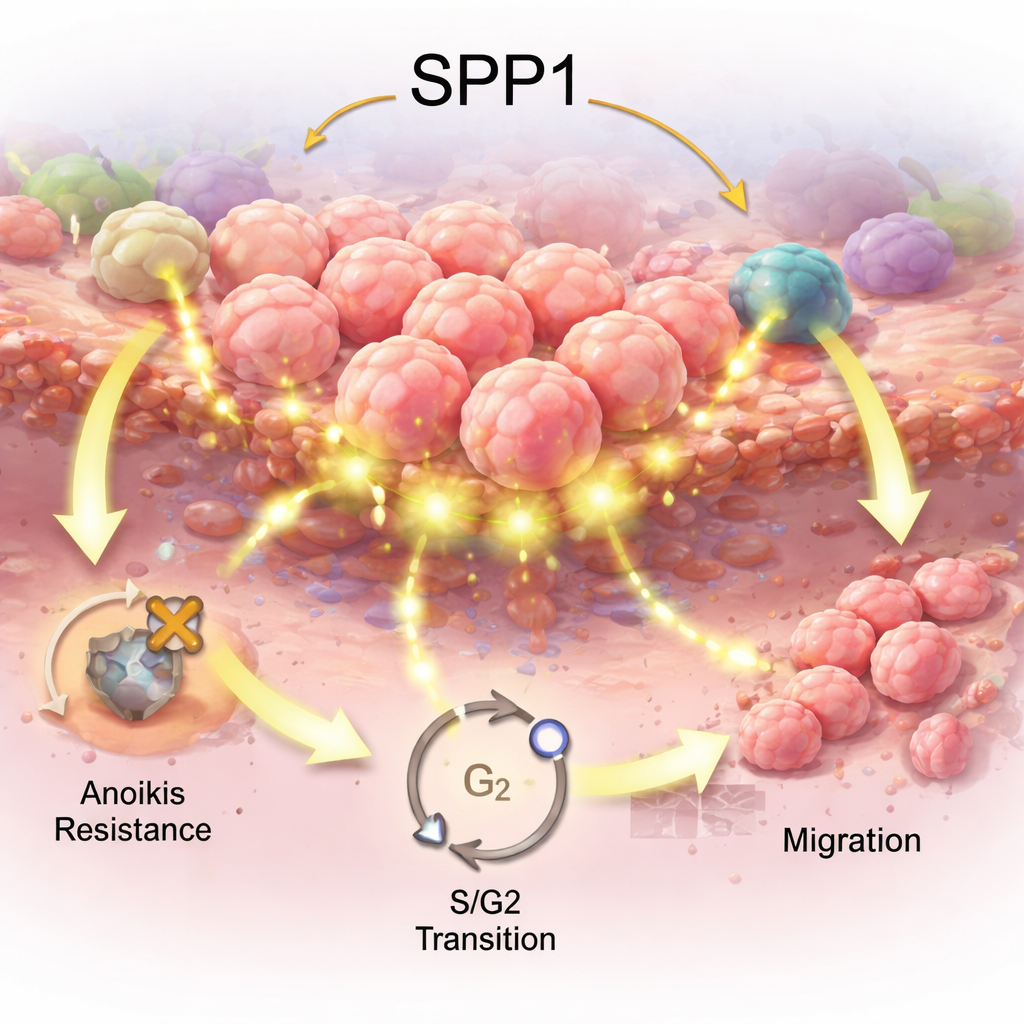
Hinweise aus den Abwehrzellen des Körpers
Als Nächstes untersuchte das Team, wie SPP1 mit den in Tumoren einwandernden Immunzellen zusammenhängt. In Bulk-Tumorproben war ein höheres SPP1 mit Verschiebungen im Gleichgewicht der Immunzelltypen verbunden, darunter Zunahmen bestimmter Makrophagen und T‑Zellen, die Tumoren entweder angreifen oder von ihnen ausgeschaltet werden können. Einzelzell-RNA-Sequenzierung — das Erfassen der Genaktivität auf Einzelzell‑Ebene — zeigte, dass SPP1 in tumorumgebungsassoziierten Makrophagen und anderen Zellen des Tumorumfelds stark aktiviert war. Signale, an denen SPP1 und der Partnerrezeptor CD44 beteiligt sind, schienen diese Makrophagen mit Helfer‑T‑Zellen zu verbinden, was nahelegt, dass dieser Signalweg ein immunologisches „Nachbarschaftsbild“ schaffen könnte, das das Tumorüberleben eher begünstigt als dessen Beseitigung. Obwohl diese Zusammenhänge korrelativ sind, deuten sie auf SPP1 als möglichen Akteur darin hin, wie Magen‑Tumoren der Immunabwehr entgehen.
Von Big Data zu echten Geweben und Zellen
Um zu prüfen, ob die Computerdaten der Realität entsprechen, maßen die Forschenden SPP1 in 32 menschlichen Magengewebeproben. Sowohl Gen‑ als auch Proteinanalysen zeigten denselben Trend: die niedrigsten Werte im normalen Gewebe, höhere in der intestinalen Metaplasie und am höchsten beim Magenkrebs. Patientinnen und Patienten, deren Tumoren mehr SPP1 exprimierten, hatten deutlich schlechteres Gesamtüberleben, und statistische Modelle deuteten darauf hin, dass SPP1 half, Ein‑, Drei‑ und Fünfjahres‑Ergebnisse vorherzusagen. In Zellkultur führte die Herunterregulation von SPP1 in einer Magenkrebszelllinie zu verlangsamtem Wachstum, verringerter Wanderungsfähigkeit, erhöhter programmierter Zellsterblichkeit und einem Stillstand der Zellen in einer kritischen Phase des Zellzyklus. Diese Experimente stützen die Idee, dass SPP1 aktiv dazu beiträgt, Krebszellen vor dem Absterben zu bewahren und ihre Teilung zu fördern.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht‑Spezialisten lautet die Botschaft: SPP1 verhält sich wie eine zunehmende Alarmglocke auf dem Weg von einer „riskanten, aber noch nicht krebsartigen“ Magenschleimhaut bis zum ausgewachsenen Krebs. Hohe Spiegel dieses Moleküls kennzeichnen Gewebe, die mit höherer Wahrscheinlichkeit voranschreiten, und Patienten mit wahrscheinlicheren schlechten Verläufen. Obwohl weitere Arbeit nötig ist — insbesondere größere Patientenkohorten und Tierversuche — könnte die Überwachung von SPP1 in Biopsien aus intestinaler Metaplasie eines Tages Ärztinnen und Ärzten helfen zu entscheiden, wer engmaschiger überwacht oder früher behandelt werden sollte. Bei bereits etabliertem Magenkrebs könnten Medikamente, die SPP1 oder seine zentralen Partner blockieren, die Tumorabwehr schwächen, indem sie Krebszellen anfälliger für Zelltod machen und gleichzeitig die umliegenden Immunzellen so umgestalten, dass sie die Erkrankung effektiver bekämpfen.
Zitation: Wu, K., Ye, Y., Pei, B. et al. Identification and verification of SPP1 in anoikis as a prognostic biomarker for intestinal metaplasia and gastric cancer. Sci Rep 16, 5842 (2026). https://doi.org/10.1038/s41598-026-36714-9
Schlüsselwörter: Magenkrebs, intestinale Metaplasie, Biomarker, Osteopontin SPP1, tumormikroumgebung