Clear Sky Science · de
Kann evolutionäre Therapie beim nicht‑kleinzelligen Lungenkrebs angewendet werden?
Die Krebsbehandlung als evolutionären Wettstreit neu denken
Die Krebsversorgung wird oft als einfacher Kampf dargestellt: möglichst starke Medikamente geben und versuchen, jede einzelne Krebszelle auszurotten. Doch bei schnell wachsenden, aggressiven Tumoren wie fortgeschrittenem nicht‑kleinzelligem Lungenkrebs (NSCLC) geht diese „Maximalattacke“ oft nach hinten los. Die Tumoren schrumpfen zunächst, wachsen aber fast immer wieder nach — nun beherrscht von medikamentenresistenten Zellen. Diese Studie stellt eine provokante Frage: Was wäre, wenn Ärzte statt auf Auslöschung den Tumor als sich entwickelndes Ökosystem behandeln und Medikamentenschemata einsetzen, die gezielt einige medikamentenempfindliche Zellen am Leben erhalten, um resistente Zellen in Schach zu halten?
Warum die Standard‑Hochdosisbehandlung die Resistenz beschleunigen kann
In der derzeitigen Praxis erhalten Patientinnen und Patienten mit metastasiertem NSCLC und bestimmten genetischen Veränderungen häufig täglich eingenommene Tyrosinkinasehemmer (TKIs) wie Erlotinib. Diese Wirkstoffe können Tumoren anfangs drastisch verkleinern, doch nahezu alle Patientinnen und Patienten erleiden schließlich ein Rezidiv, weil resistente Krebszellen überleben und die Oberhand gewinnen. Wenn Ärzte die Dosis auf das maximum tolerierbare Niveau steigern, töten sie vor allem die empfindlichen Zellen, die gut auf das Medikament ansprechen. Resistente Zellen, die auch hohe Dosen überstehen, sehen sich plötzlich weniger Konkurrenz um Raum und Nährstoffe gegenüber. Das Ergebnis ist ein evolutionärer „Sieg“ für die härtesten Krebszellen, und der Tumor kehrt zurück — jetzt deutlich schwerer behandelbar. 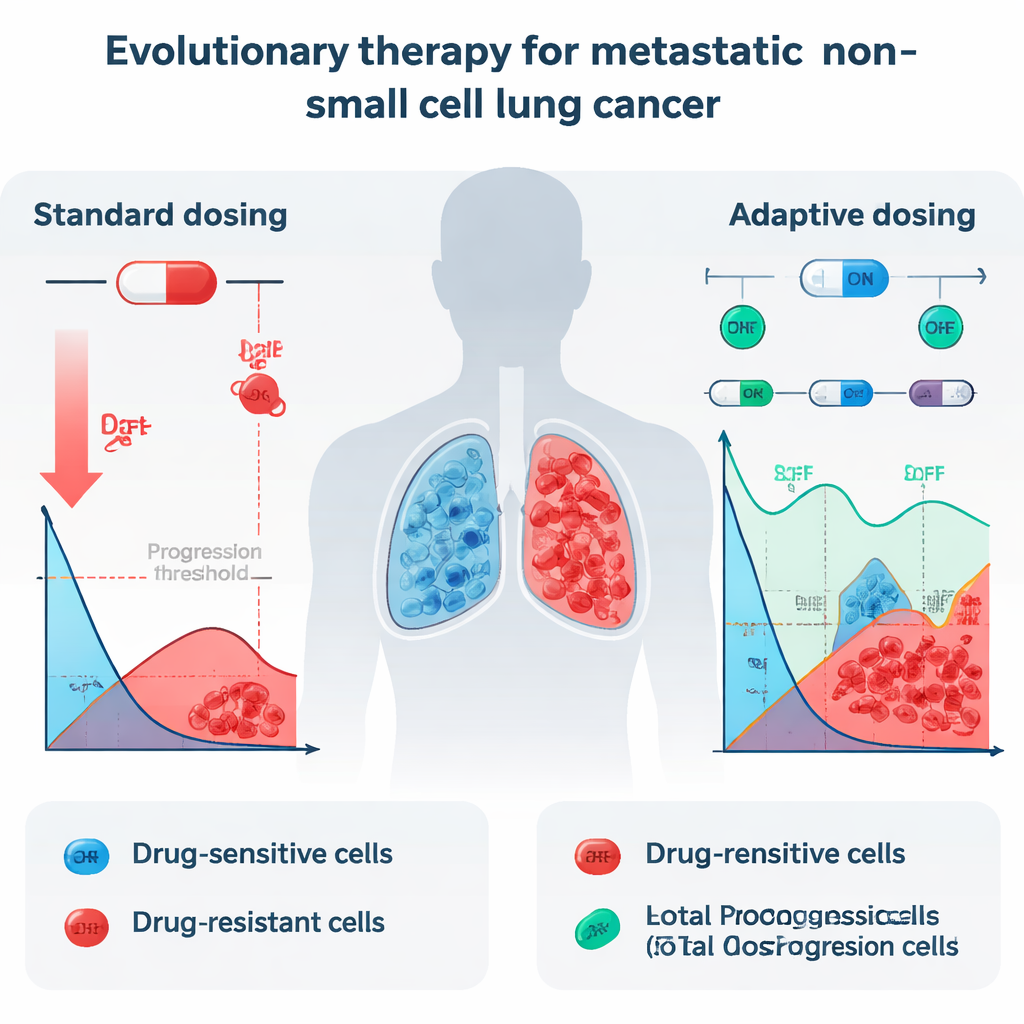
Mathematik nutzen, um eine neue Dosierungsstrategie an echten Patienten zu testen
Die Forschenden untersuchten, ob eine andere Strategie, genannt evolutionäre Therapie, im Stadium IV des NSCLC funktionieren könnte. Evolutionäre Therapie zielt nicht darauf ab, den Tumor komplett zu vernichten. Stattdessen versucht sie, ihn zu kontrollieren, indem ein stabiles Gemisch aus empfindlichen und resistenten Zellen erhalten bleibt, sodass die empfindlichen Zellen die resistenten „auskonkurrenzieren“. Das Team übernahm ein konkretes Ein‑Aus‑Dosierungsprotokoll, das bereits bei Prostatakrebs vielversprechend war, und fragte: Wäre eine derartige Strategie theoretisch auch beim Lungenkrebs wirksam? Um das zu beantworten, analysierten sie detaillierte Tumorgrößenmessungen von 13 NSCLC‑Patienten, die in einer klinischen Studie mit Erlotinib behandelt worden waren, wandeln die Scans in das gesamte Tumorvolumen über die Zeit um und speisten diese Daten in eine Reihe mathematischer Modelle ein.
Das Modell finden, das Resistenz wirklich erfasst
Die Forschenden testeten 26 verschiedene Modelle für Tumorwachstum, die alle Krebszellen in zwei Gruppen einteilten: medikamentenempfindliche und medikamentenresistente. Diese Modelle unterschieden sich darin, wie sie Wachstumsgrenzen beschrieben, wie die beiden Zelltypen miteinander konkurrieren, wie das Medikament im Körper verarbeitet wird und wie die Behandlung Zellen abtötet. Viele einfachere Modelle passten die Patientendaten noch einigermaßen, wenn die Tumoren nur schrumpften. Wenn die Tumoren jedoch einem realistischeren „U‑förmigen“ Verlauf folgten — zunächst Schrumpfung unter Therapie, dann Wiederwachstum durch entstehende Resistenz — scheiterten die meisten Modelle. Die beste Übereinstimmung ergab sich mit einem sogenannten Gompertz‑Modell, das zwei entscheidende Ideen einschloss: erstens können Tumoren nicht unbegrenzt wachsen (sie spüren die Verdrängung durch Dichte), und zweitens konkurrieren sensible und resistente Zellen asymmetrisch, sodass der Erfolg eines Typs davon abhängt, wie viele Zellen des anderen Typs vorhanden sind.
Adaptive Therapie gegen Standardversorgung simulieren
Sobald sie die am besten passenden Modelle identifiziert hatten, nutzte das Team diese, um für jeden Patienten zwei Behandlungsstrategien zu simulieren: die übliche konstante Maximaldosis und ein adaptives Protokoll nach Zhang und Kollegen. Beim adaptiven Ansatz wird Erlotinib so lange gegeben, bis der Tumor auf die Hälfte seiner Ausgangsgröße geschrumpft ist; dann wird das Medikament pausiert, damit sich empfindliche Zellen wieder erholen; die Behandlung wird wieder aufgenommen, sobald der Tumor seine Ausgangsgröße erreicht, und dieser Zyklus wiederholt sich. Über alle gut funktionierenden Modelle mit Konkurrenz zwischen den Zelltypen verzögerte diese adaptive Strategie konstant den Zeitpunkt, an dem der Tumor 110 % seiner ursprünglichen Größe überschritt — ein gebräuchlicher Schwellenwert für Progression. In dem am besten passenden Gompertz‑Modell mit Konkurrenz verlängerte sich die mediane Zeit bis zur Progression von etwa 24,8 Monaten bei Standarddosierung auf 42,3 Monate unter dem adaptiven Protokoll — ein Gewinn von ungefähr anderthalb Jahren. 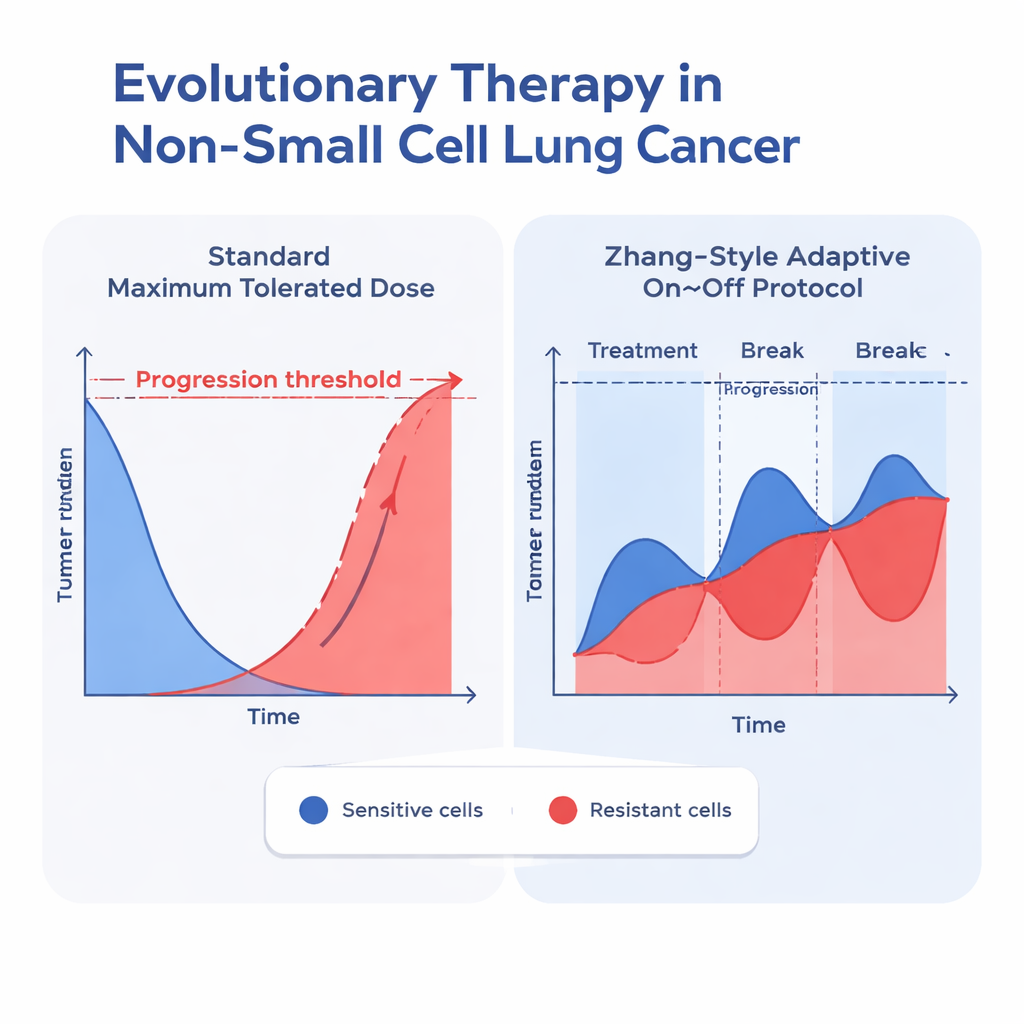
Was das für künftige Patientinnen und Patienten bedeuten könnte
Diese Arbeit verändert noch nicht die heutige Behandlungspraxis von NSCLC‑Patienten, liefert aber einen starken Machbarkeitsnachweis. Indem die Autorinnen und Autoren ihre Modelle an echten Patientendaten verankerten und darauf bestanden, dass die Modelle nicht nur frühe Schrumpfungen, sondern auch resistenzbedingtes Wiederwachstum reproduzieren, zeigen sie, dass evolutionäre Therapie theoretisch selbst bei einem schnell wachsenden und tödlichen Krebs denkbar ist. Ihre Ergebnisse deuten darauf hin, dass wohlgetaktete Behandlungsunterbrechungen die Kontrolle der Krankheit verlängern könnten, indem medikamentenempfindliche Zellen als Verbündete benutzt werden statt als Kollateralschaden. Um diese Idee in die Praxis zu überführen, sind jedoch mehr Daten nötig, bessere Biomarker — etwa Bluttests, die Tumor‑DNA verfolgen — und rigorose klinische Studien. Die Botschaft an interessierte Laien ist dennoch klar: Manchmal ist es nicht die klügste Strategie, Krebs so hart wie möglich zu treffen, sondern seine Evolution so zu steuern, dass er ein beherrschbarer, langsamerer Gegner bleibt.
Zitation: Jansén-Storbacka, L.R., Honasoge, K.S., Molnárová, E. et al. Can evolutionary therapy be applied in non-small cell lung cancer?. Sci Rep 16, 7442 (2026). https://doi.org/10.1038/s41598-026-36712-x
Schlüsselwörter: evolutionäre Therapie, nicht‑kleinzelliger Lungenkrebs, Arzneimittelresistenz, adaptive Dosierung, mathematische Onkologie