Clear Sky Science · de
Von Cholangiokarzinom stammende Exosomen schwächen die antitumoralen Funktionen von NK-Zellen
Wie ein versteckter Krebs das Immunsystem überlistet
Cholangiokarzinom, ein Krebs der Gallenwege innerhalb der Leber, ist berüchtigt dafür, früh schwer zu erkennen und schwer zu behandeln zu sein. Diese Studie untersucht eine subtile Taktik, die diese Tumoren einsetzen, um an den natürlichen Abwehrkräften des Körpers vorbeizuschlüpfen: Sie senden winzige Pakete namens Exosomen aus, die die natürlichen Killerzellen (NK-Zellen) – eine Einsatztruppe des Immunsystems, die auf die Jagd und Vernichtung von Krebs spezialisiert ist – still und leise schwächen. Das Verständnis dieser Tarnstrategie könnte neue Wege für Therapien eröffnen, die die Fähigkeit des Immunsystems zur Gegenwehr wiederherstellen.
Die First-Responder der Krebsabwehr
NK-Zellen gehören zum angeborenen Immunsystem, der Schnellreaktionskraft des Körpers. Im Gegensatz zu vielen Immunzellen, die Zeit brauchen, um eine spezifische Bedrohung zu erkennen, können NK-Zellen rasch abnorme Zellen angreifen, einschließlich virusinfizierter und krebsartiger Zellen. Sie tun dies, indem sie an Zielzellen andocken und toxische Moleküle wie Granzyme B sowie Signalmoleküle wie Interferon-gamma (IFN-γ) freisetzen, die sowohl Tumorzellen abtöten als auch weitere Immunzellen mobilisieren. Bei vielen Blutkrebserkrankungen und einigen soliden Tumoren hat die Stärkung der NK-Zell-Aktivität therapeutisches Potenzial gezeigt. Bei soliden Tumoren wie dem Gallengangskarzinom jedoch erscheinen NK-Zellen oft auffallend rar und träge gerade dort, wo sie am dringendsten gebraucht werden.
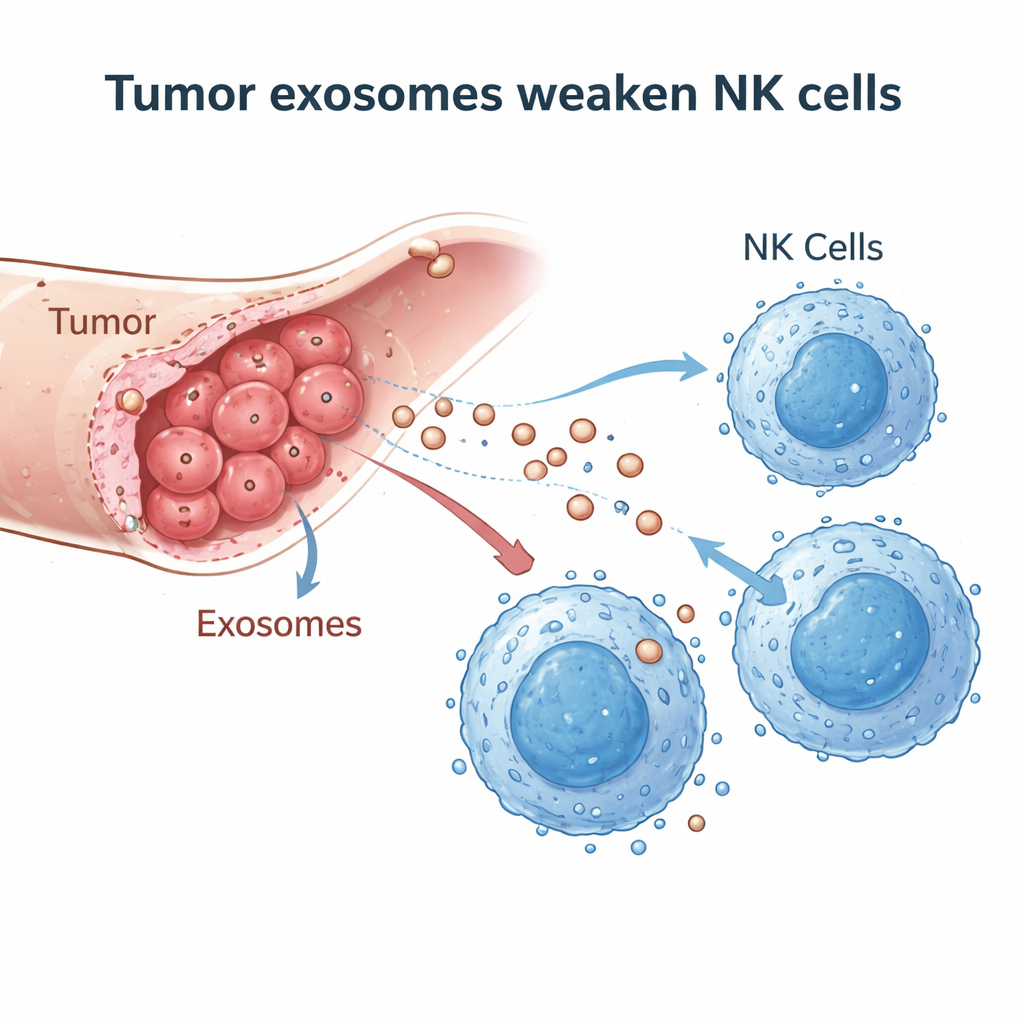
Kleine Vesikel mit großer Wirkung
Die Forschenden vermuteten, dass Cholangiokarzinomzellen NK-Zellen mithilfe von Exosomen sabotieren könnten — nanoskalige Membranbläschen, die mit Proteinen und genetischem Material beladen sind und von Zellen zur Kommunikation freigesetzt werden. Sie isolierten Exosomen aus einer menschlichen Gallengangskarzinom-Zelllinie und aus dem Blut von Cholangiokarzinom-Patienten und bestätigten deren Identität und Größe mit Elektronenmikroskopie, Partikelverfolgung und üblichen Exosomen-Markern. In Tumorgewebeproben von 20 Patientinnen und Patienten verglichen sie krebsbefallene Bereiche mit benachbartem, nicht tumoralem Lebergewebe und fanden deutlich weniger NK-Zellen, die die Tumore infiltrierten, was darauf hindeutet, dass etwas in der Tumorumgebung NK-Zellen fernhält oder deaktiviert.
Abschalten von Überlebens- und Tötungssignalen
Um zu untersuchen, wie diese Tumor-Exosomen NK-Zellen beeinflussen, setzten die Forschenden eine NK-Zell-Linie (NK-92) Exosomen aus Krebszellen und Patientenblut aus. Die NK-Zellen zeigten erhöhte Anteile programmierter Zellsterblichkeit, insbesondere nach Behandlung mit Exosomen der Tumorzelllinie. Auf molekularer Ebene reduzierten die NK-Zellen die Produktion zentraler "Überlebens"-Proteine (BCL-2 und BCL-XL), wodurch das Gleichgewicht zugunsten des Zelltods kippte. Interessanterweise änderte sich ihre Gesamtproliferation nicht, was bedeutet, dass die Exosomen vor allem die Sterblichkeit der NK-Zellen erhöhten, statt deren Teilung zu verlangsamen. Die Exosom-behandelten NK-Zellen schütteten außerdem weniger IFN-γ und weniger Granzyme B aus, wodurch sowohl ihre direkte Fähigkeit, Ziele zu töten, als auch ihre Kapazität, breitere Immunantworten zu koordinieren, geschwächt wurden. In Labortests, die die zytotoxische Leistungsfähigkeit der NK-Zellen gegen Standardzielzellen maßen, zeigte sich ein Rückgang der Tötungskraft nach Exosomen-Exposition aus Cholangiokarzinomen.
Störung der Zusammenarbeit von Immunzellen
NK-Zellen müssen aneinander und an Tumorzellen haften, um effektiv zu arbeiten; dafür sind Oberflächen-Adhäsionsmoleküle nötig, die wie molekulares Klett wirken. Nach Behandlung mit krebsabgeleiteten Exosomen verloren NK-Zellen ihr typisches geschlossenes Wachstumsbild und erschienen verstreuter. Die Forschenden fanden, dass die Level mehrerer wichtiger Adhäsionsmoleküle (CD11a, CD18 und CD54) sowohl auf Gen- als auch auf Proteinebene sanken, während ein anderer Adhäsionsmarker, CD2, unverändert blieb. Dieser Verlust an Adhäsion erschwert wahrscheinlich das Erreichen von Tumoren, die Bildung stabiler Kontakte mit Krebszellen und die Ausführung tödlicher Angriffe. Entscheidenderweise zeigten untersuchte NK-Zellen direkt aus dem Blut von Cholangiokarzinom-Patienten dieselben Kennzeichen: schwächere zytotoxische Aktivität und reduzierte Spiegel derselben Adhäsionsmoleküle im Vergleich zu NK-Zellen gesunder Kontrollpersonen.
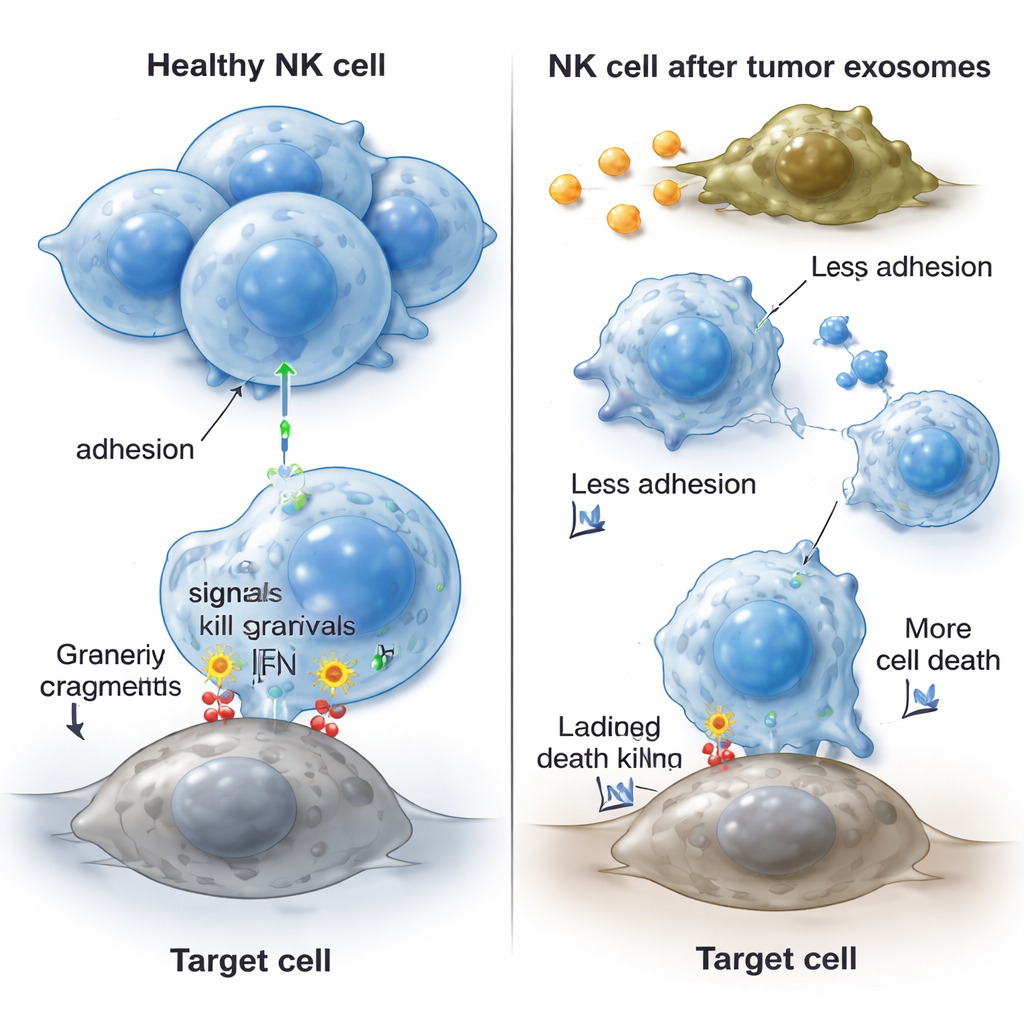
Was das für Patientinnen, Patienten und künftige Therapien bedeutet
Zusammengefasst legen die Ergebnisse nahe, dass das Cholangiokarzinom Exosomen als eine Form molekularer Sabotage einsetzt, um der Immunabwehr zu entkommen. Diese winzigen Vesikel treiben NK-Zellen in Richtung Zelltod, verringern deren Produktion zentraler Tötungsfaktoren und entfernen die Adhäsionsproteine, die ihnen ermöglichen, sich zu gruppieren und Tumoren anzugreifen. Das Ergebnis sind weniger funktionale NK-Zellen in und um den Tumor und eine abgeschwächte Immunantwort, die dem Krebs mehr Raum zum Wachsen lässt. Obwohl diese Arbeit größtenteils in kontrollierten Laborbedingungen und mit einer begrenzten Zahl von Patientenproben durchgeführt wurde, weist sie auf neue Strategien hin: das Blockieren tumoraler Exosomen, das Wiederherstellen von NK-Überlebenssignalen oder das Auffrischen von Adhäsionsmolekülen könnte helfen, die natürlichen Abwehrkräfte gegen diesen tödlichen Gallengangskarzinom wiederzubeleben.
Zitation: Wang, X., Zhang, F., Cao, Z. et al. Cholangiocarcinoma derived exosomes attenuate the anti-tumor functions of NK cells. Sci Rep 16, 5810 (2026). https://doi.org/10.1038/s41598-026-36706-9
Schlüsselwörter: Cholangiokarzinom, natürliche Killerzellen, Exosomen, Tumor-Immunevasion, Tumormikroumgebung