Clear Sky Science · de
Bioinformatische Charakterisierung und automatisierte Erkennung metabolisch aktivierter Monozytenunterpopulationen bei Dyslipidämie
Warum versteckte Immunzellen für die Herzgesundheit wichtig sind
Über Cholesterinprobleme wird meist in Bezug auf Ernährung, Bluttestergebnisse und das Risiko von Herzinfarkten gesprochen. Unter diesen Zahlen jedoch verändert sich unser Immunsystem still und leise. Diese Studie untersucht eine spezielle Gruppe weißer Blutkörperchen im Blut junger Erwachsener mit erhöhtem LDL-(„schlechtem“) Cholesterin. Diese Zellen scheinen „metabolisch aktiviert“ zu werden und sich an früheren Kontakt mit überschüssigen Fetten zu erinnern, was Entzündungen in den Arterien — und damit künftige Herzkrankheiten — wahrscheinlicher machen könnte. Das Verständnis dieser verborgenen Zelltypen könnte Ärztinnen und Ärzten helfen, Probleme früher zu erkennen und präzisere Behandlungen zu entwickeln.
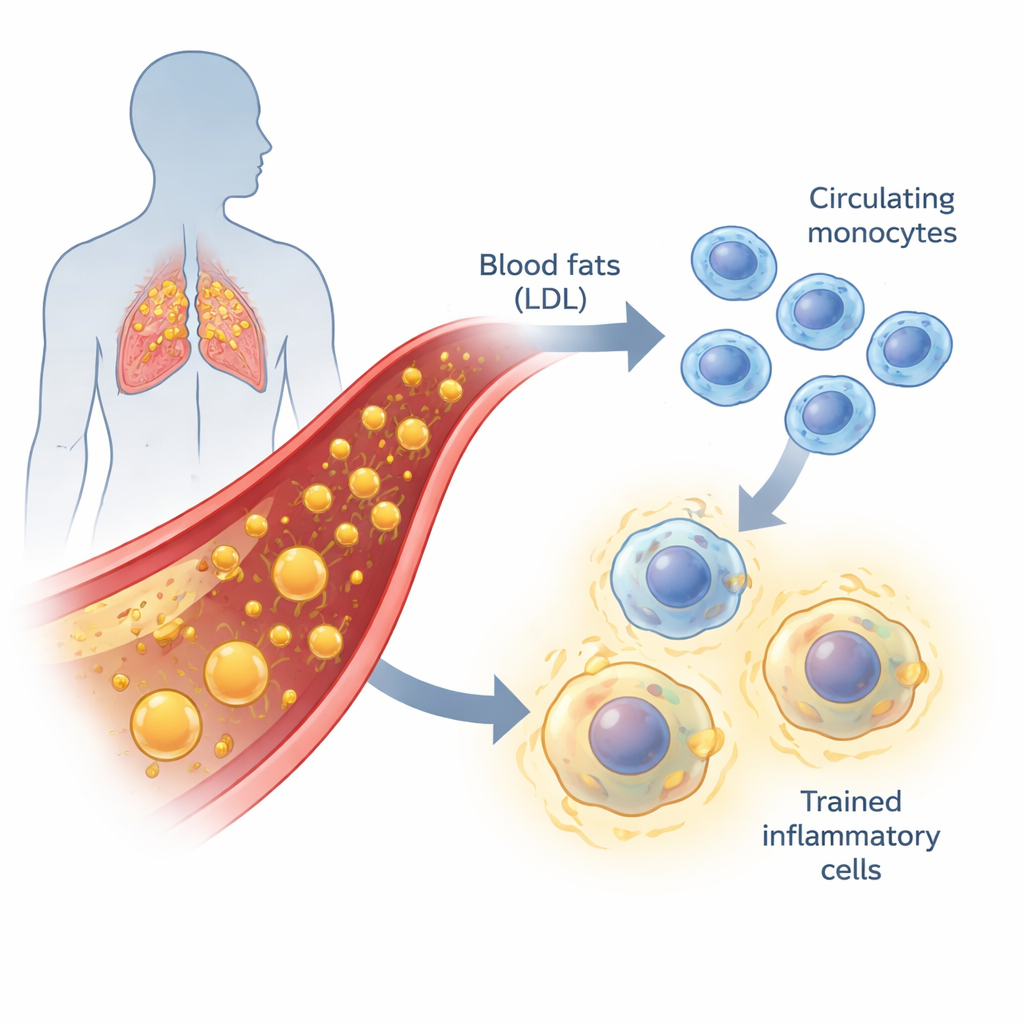
Fett im Blut und schwelende Entzündung
Atherosklerose, der Prozess, der zu verengten Arterien führt, ist nicht nur das Anhaften von Fett an Gefäßwänden. Es ist auch eine langsame, chronische Entzündungskrankheit. Wenn LDL-Cholesterin erhöht ist, insbesondere in oxidierter Form, reizt es die Gefäßinnenhaut. Monozyten — zirkulierende weiße Blutkörperchen — und die Makrophagen, in die sie sich verwandeln, werden in diese Bereiche gelenkt und beginnen, Fett aufzunehmen. Wenn dieser Reinigungsprozess schlecht reguliert ist, verwandeln sich die Zellen in „Schaumzellen“ und tragen zum Aufbau fettiger Plaques bei. Klassischerweise haben Forschende Blutmonozyten in drei Gruppen eingeteilt, basierend auf Oberflächenmarkern, mit jeweils unterschiedlichen Rollen beim Patrouillieren der Gefäße, Auslösen von Entzündungen oder der Erhaltung des Gewebehaushalts.
Jenseits einfacher Etiketten: Entdeckung neuer Monozytentypen
Die Autorinnen und Autoren vermuteten, dass einige zirkulierende Monozyten bei Menschen mit Dyslipidämie bereits in einen metabolisch aktiven Zustand umprogrammiert sein könnten, bereit dazu, schädliche Makrophagen zu werden. Um dies zu untersuchen, sammelten sie Blut von 23 jungen Erwachsenen mit hohem LDL-Cholesterin und 17 gesunden Teilnehmern mit normalen Lipidprofilen. Keiner erhielt cholesterinsenkende Medikamente oder hatte andere schwere Erkrankungen, was half, die Auswirkungen der Dyslipidämie isoliert zu betrachten. Mithilfe einer Technik namens Durchflusszytometrie maßen sie nicht nur klassische Oberflächenmarker, sondern auch Proteine, die an der Fettverarbeitung beteiligt sind, sowie chemische Markierungen an Histonen — winzigen Proteinspulen, die steuern, welche Gene in einer Zelle ein- oder ausgeschaltet werden.
Schlaue Algorithmen zur Lesung komplexer Immunlandschaften
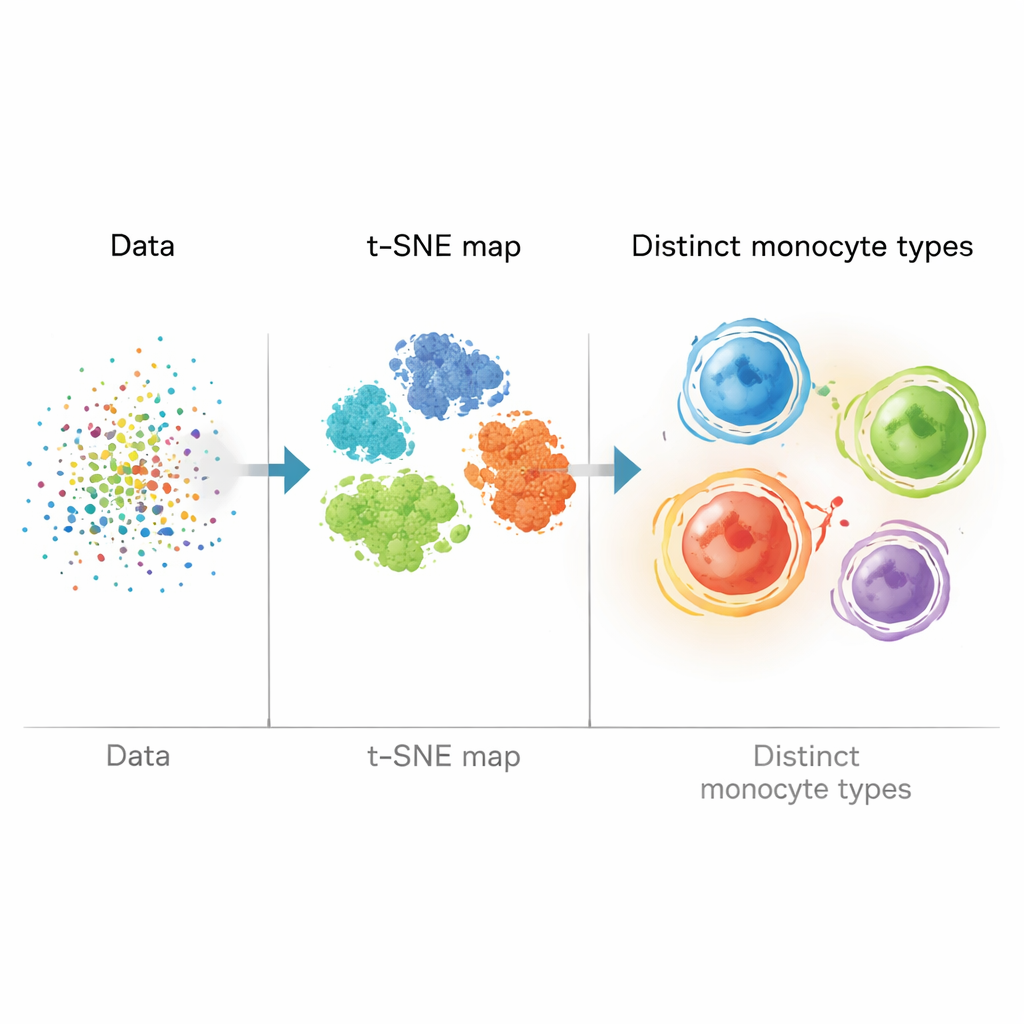
Statt sich nur auf manuelles „Gating“ (per Auge gezogene Grenzen in Zwei-Markoren-Diagrammen) zu verlassen, entwickelten die Forschenden eine bioinformatische Pipeline, die jede Zelle als Punkt in einem hochdimensionalen Raum behandelte. Sie bereinigten und standardisierten die Daten und nutzten dann t-SNE, eine mathematische Methode, die Messungen mit vielen Markern in eine zweidimensionale Karte überführt, auf der ähnliche Zellen zusammenclustern. Anschließend wandten sie Clustering-Algorithmen (X-shift und FlowSOM) an, um automatisch Zellen mit ähnlichen Markerprofilen zu gruppieren. Dadurch konnten sie über die drei klassischen Monozytentypen hinaus vier Hauptpopulationen identifizieren, definiert durch Kombinationen von Fett-verarbeitenden Proteinen (ABCA1, PLIN2, CD36) und den üblichen CD14- und CD16-Markern.
Eine entzündlich vorgeprägte Population bei Dyslipidämie
Zwei dieser vier Monozytengruppen hoben sich deutlich ab. Besonders eine — charakterisiert durch hohes CD14, fehlendes CD16 sowie starkes ABCA1 mit variablem PLIN2 und CD36 — entsprach dem Profil „metabolisch aktivierter“ Monozyten (MoMe). Bei Personen mit Dyslipidämie waren diese MoMe-Zellen und eine verwandte Gruppe deutlich häufiger vertreten als bei gesunden Kontrollen. Bei der Untersuchung epigenetischer Markierungen — speziell H3K4me3 und H3K27me3, chemische Tags auf Histonproteinen, die mit Genaktivität verknüpft sind — fanden die Forschenden, dass MoMe-Zellen von dyslipidämischen Individuen erhöhte H3K4me3-Werte aufwiesen. Dieses Zeichen steht im Zusammenhang mit Genen, die Entzündungen fördern, und deutet darauf hin, dass diese Zellen eine Form angeborenen „Gedächtnisses“ oder trainierter Immunität nach wiederholter Exposition gegenüber hohem LDL tragen.
Von zirkulierenden Zellen zu plaquebildenden Makrophagen
Um zu sehen, was diese Monozyten im Gewebe werden könnten, kultivierte das Team gereinigte Monozyten in einem Laborumfeld, das das metabolische Syndrom nachahmte, und stimulierte sie zur Differenzierung in Makrophagen. Wieder nutzten sie fortgeschrittene Analysen, um Makrophagenuntergruppen zu identifizieren und maßen deren epigenetische Markierungen. Interessanterweise zeigten Makrophagen aus gesunden Spendern häufig höhere Werte aktivierender Histon-Tags als solche aus dyslipidämischen Patienten, was darauf hindeutet, dass das entzündliche Training sich anders darstellen kann, sobald Zellen den Blutkreislauf verlassen. Obwohl die Stichprobe klein war, stützen die Befunde die Idee, dass langfristige Exposition gegenüber überschüssigen Blutlipiden Monozyten sowohl auf Proteinebene als auch epigenetisch umgestaltet und sie zu stärkeren Entzündungsreaktionen prädisponiert.
Was das für Patientinnen, Patienten und künftige Versorgung bedeutet
Für Laien lautet die Kernbotschaft: Hohes LDL-Cholesterin ist nicht nur ein Problem von „zu viel Fett“, sondern auch von „umverdrahteten“ Immunzellen. Diese Studie zeigt, dass bereits bei jungen Erwachsenen Dyslipidämie mit einer klaren Monozytenpopulation verbunden ist, die metabolisch aufgeladen und epigenetisch darauf vorbereitet erscheint, Arterienentzündungen zu fördern. Durch die Kombination leistungsfähiger Rechenwerkzeuge mit detaillierten Zellmessungen können Forschende diese risikobehafteten Zelltypen nun im Blut erkennen — lange bevor ein Herzinfarkt eintritt. Zukünftig könnten solche Ansätze Ärztinnen und Ärzten helfen, das kardiovaskuläre Risiko besser einzuschätzen, zu überwachen, wie wirksam Behandlungen das schädliche Immun-Training umkehren, und letztlich Therapien zu entwickeln, die nicht nur Cholesterinwerte, sondern auch die darauf reagierenden Immunzellen ansprechen.
Zitation: Ramírez-Torres, R., Ramírez-Segovia, S.G., González-Huerta, M.J. et al. Bioinformatic characterization and automated detection of metabolically activated monocyte subpopulations in dyslipidemia. Sci Rep 16, 6170 (2026). https://doi.org/10.1038/s41598-026-36678-w
Schlüsselwörter: Dyslipidämie, Monozyten, trainierte Immunität, Atherosklerose, Durchflusszytometrie