Clear Sky Science · de
Anwendung eines Scl1-exprimierenden Lactococcus als neuartige Immuntherapie gegen duktales adenokarzinom des Pankreas
Freundliche Bakterien als Krebsbekämpfer
Pankreaskarzinome gehören zu den tödlichsten Krebsarten, teils weil sie sich hinter starken Schutzmechanismen verbergen, die das Immunsystem lahmlegen. Diese Studie untersucht einen unerwarteten Verbündeten im Kampf gegen die Krankheit: ein verbreitetes „gutes“ Milchsäurebakterium aus der Lebensmittelwelt, das so umgebaut wurde, dass es gezielt Pankreastumoren ansteuert und dem Immunsystem hilft, diese effektiver anzugreifen. Indem die Forschenden ein klebriges Oberflächenprotein von einem gefährlichen Streptokokkenkeim übernahmen, verwandelten sie ein harmloses Mikroorganismus in ein in Mäusen getestetes, zielgerichtetes Anti-Krebs-Werkzeug.
Ein hartnäckiger Krebs, der das Immunsystem auszutricksen weiß
Das duktale Adenokarzinom des Pankreas ist berüchtigt tödlich: Nur etwa einer von acht Patienten lebt fünf Jahre nach Diagnose noch. Ein wesentlicher Grund ist die Tumormikroumgebung: eine dichte, narbenartige Hülle voller unterstützender Zellen und Moleküle, die Immunangriffe dämpft und viele Medikamente blockiert. Zu den Übeltätern gehören neutrophile extrazelluläre Fallen, kurz NETs – Netze aus DNA und Proteinen, die neutrophile Granulozyten in die Umgebung auswerfen. Bei Pankreaskrebs richten diese klebrigen Netze mehr Schaden als Nutzen an: Sie fördern das Tumorwachstum, halten killerische T‑Zellen fern und korrelieren mit schlechteren Verläufen. NETs zu unterdrücken und gleichzeitig die anti‑tumorale Immunität zu reaktivieren, hat sich deshalb als vielversprechende Strategie erwiesen.
Das klebrige Protein nutzen, aber nicht den gefährlichen Erreger
Frühere Arbeiten zeigten, dass ein Oberflächenprotein der Gruppe‑A‑Streptokokken, genannt Scl1, sowohl an tumorumgebende Fasern binden als auch die NET‑Bildung dämpfen kann, wodurch das Pankreastumorwachstum in Mäusen verlangsamt wurde. Gruppe‑A‑Streptokokken sind jedoch auch die Erreger von Rachenentzündungen und schweren invasiven Infektionen, daher eignen sie sich nicht als Lebendtherapie. Um das nützliche Protein zu bewahren, aber den schädlichen Keim zu meiden, entwickelten die Forschenden Lactococcus lactis – ein in Lebensmitteln weit verbreitetes und als sicher geltendes Probiotikum – so, dass es Scl1 auf seiner Oberfläche präsentiert. Dieser neue Stamm, bezeichnet als Lactococcus::620, wurde an Mäusen mit Pankreastumoren getestet, sowohl in einfachen Flankentumor‑Modellen als auch in realistischeren Tumoren, die in der Bauchspeicheldrüse wachsen.
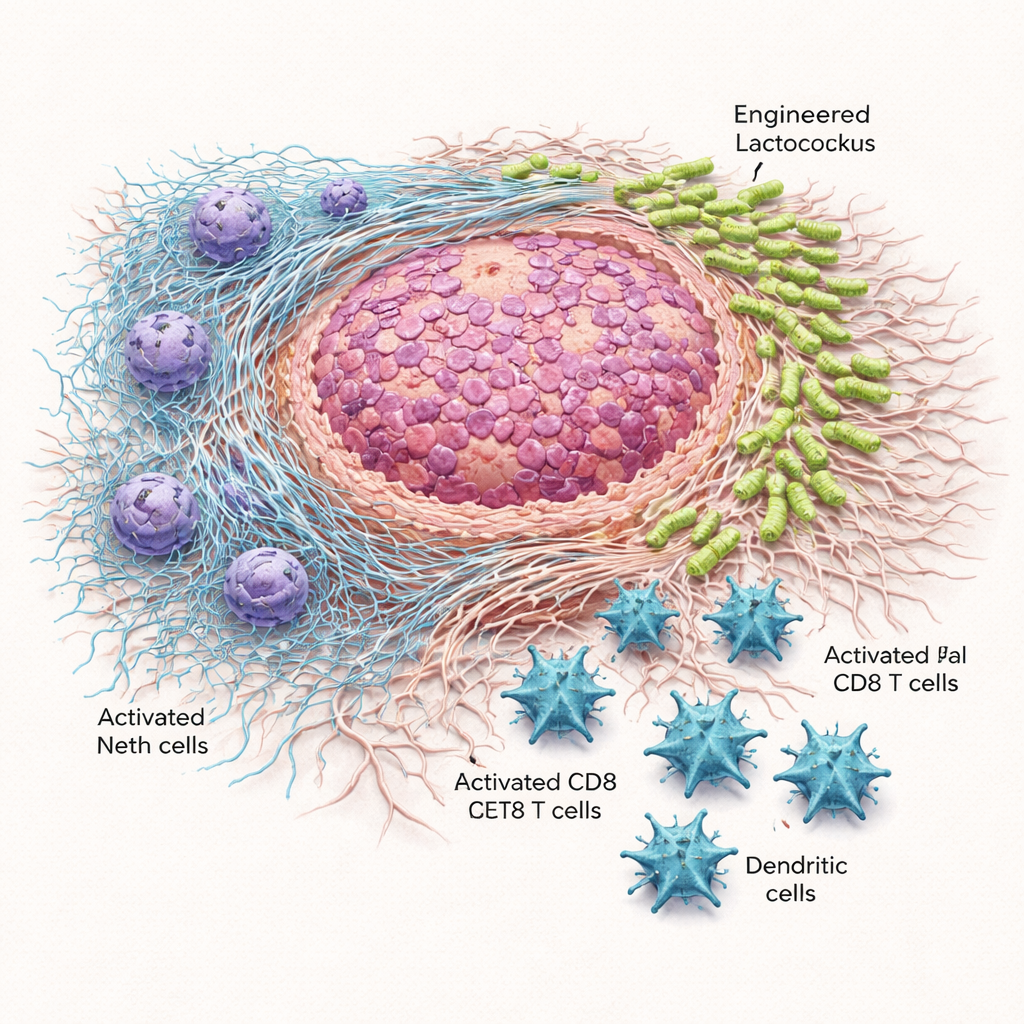
Gelenkte Bakterien verringern Tumorwachstum und verlängern das Überleben
Wurde eine einmalige Dosis der gentechnisch veränderten Bakterien direkt in Flankentumoren injiziert oder in die Bauchhöhle eingebracht, wuchsen die Tumoren langsamer und wogen weniger als bei Mäusen, die normales Lactococcus oder eine Salzlösung erhielten. Im anspruchsvolleren Pankreasmodell waren wiederholte Gaben alle drei Tage nötig, doch der Nutzen war deutlich: Lactococcus::620 verkleinerte Tumoren, reduzierte deren Gewicht und verlängerte das Überleben der Tiere, ohne behandlungsbedingte Todesfälle zu verursachen. Mikroskopie und Kulturuntersuchungen von Tumorgewebe zeigten, dass die Scl1‑tragenden Bakterien sich zuverlässig in der Tumorumgebung anreicherten, vor allem in der von tumorauslösenden Fibroblasten gebildeten fibrösen Matrix, während die Milz größtenteils verschont blieb. Im Gegensatz dazu verbreitete sich unverändertes Lactococcus weiter im Körper und war bei systemischer Verabreichung teilweise toxisch.
Schädliche Netze entschärfen und Immunzellen eindringen lassen
Die gentechnisch veränderten Bakterien veränderten auch die immunologische Landschaft rund um die Tumoren. Tumoren von mit Lactococcus::620 behandelten Mäusen enthielten mehr CD8‑„Killer“‑T‑Zellen und dendritische Zellen – Schlüsselfiguren bei der Erkennung und Zerstörung von Krebszellen – und diese T‑Zellen zeigten weniger Erschöpfungsmarker und mehr aktivitätsbezogene Moleküle. Gleichzeitig sanken Messwerte für NET‑Aktivität. In Laborversuchen setzten Neutrophile, die mit Lactococcus::620 in Kontakt kamen, weniger freie DNA frei und wiesen eine geringere Aktivität der Myeloperoxidase auf, eines Enzyms, das für den Aufbau von NETs nötig ist. Bei behandelten Mäusen war die zirkulierende, NET‑assoziierte DNA reduziert. Entscheidend ist: In genetisch veränderten Mäusen, die keine NETs bilden können, bremsten die konstruierten Bakterien das Tumorwachstum nicht mehr. Dieser Verlust des Nutzens legt nahe, dass die Blockade der NETs zentral für die Wirksamkeit der Therapie ist.
Welche Bedeutung das für die künftige Krebsbehandlung haben könnte
Insgesamt skizzieren die Ergebnisse ein neues Konzept: Ein sicheres, lebensmitteltaugliches Bakterium als programmierbares Liefervehikel zu nutzen, um ein NET‑blockierendes, tumorumhendes Protein direkt in die feindliche Umgebung des Pankreaskrebses zu bringen. In Mäusen verringerte dieser Ansatz die Tumorlast, verbesserte das Überleben und schuf Raum dafür, dass Immunzellen effektiver wirken können. Zwar ist vor einer Erprobung am Menschen noch viel zu tun – unter anderem Tests in Modellen mit metastasierten Erkrankungen und Kombinationen mit modernen Immuntherapien – doch die Studie zeigt, dass sorgfältig konstruierte „gute“ Bakterien eines Tages dazu beitragen könnten, das Blatt gegen einen unserer resistentesten Krebsarten zu wenden.
Zitation: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
Schlüsselwörter: Pankreaskarzinom, Probiotische Therapie, Tumormikroumgebung, Immunmodulation, Neutrophile extrazelluläre Fallen