Clear Sky Science · de
Klinische Validierung leichter CNN-Architekturen für eine verlässliche Mehrklassenklassifikation von Lungenkrebs mit histopathologischen Bildgebungsverfahren
Warum diese Forschung für Patientinnen, Patienten und Ärztinnen wichtig ist
Lungenkrebs ist oft tödlich, weil er spät entdeckt oder falsch klassifiziert wird, was die richtige Behandlung verzögern kann. Diese Studie untersucht, ob kleine, effiziente Computerprogramme – statt großer, energiehungriger Modelle – zuverlässig verschiedene Arten von Lungenkrebs in mikroskopischen Gewebebildern erkennen können. Wenn solche leichten Werkzeuge gut funktionieren, könnten sie in Krankenhäusern weltweit eingesetzt werden, auch dort mit begrenzten Rechenressourcen, um Pathologen bei schnelleren und konsistenteren Diagnosen zu unterstützen.
Den Krebs mit digitalen Mikroskopen genau betrachten
Wenn ein verdächtiger Lungenknoten entfernt oder biopsiert wird, untersuchen Pathologen dünn geschnittenes, gefärbtes Gewebe unter dem Mikroskop, um zu entscheiden, ob es gutartig ist oder zu einer der Krebsarten gehört. In dieser Arbeit konzentrieren sich die Autoren auf drei Hauptkategorien: gutartiges Lungengewebe, Lungenadenokarzinom und Plattenepithelkarzinom der Lunge. Diese Subtypen sind wichtig, weil sie unterschiedlich auf Therapien ansprechen. Das Team verwendet digitale Aufnahmen dieser Präparate – histopathologische Bilder – und fragt, ob kompakte neuronale Netze die feinen visuellen Muster lernen können, die jede Klasse unterscheiden, von Zellformen bis zur Gewebearchitektur, und das ebenso zuverlässig wie deutlich größere Modelle.
Kleinere, aber intelligentere digitale Klassifizierer entwickeln
Die meisten modernen Bildverarbeitungssysteme sind sehr groß und erfordern teure Grafikprozessoren, was ihren Einsatz in vielen Kliniken erschwert. Die Forscher entwerfen stattdessen vier „lite“ Bildanalysemodelle, genannt Lite-V0, Lite-V1, Lite-V2 und Lite-V4, jeweils eine verschlankte Version eines konvolutionalen neuronalen Netzes (CNN). Alle vier folgen demselben Grundprinzip: Sie extrahieren schrittweise visuelle Merkmale durch eine Abfolge einfacher Bausteine, fassen das Bild zusammen und geben eines der drei Gewebeetiketten aus. Unterscheidungen zwischen den Versionen betreffen die Anzahl und Breite der Blöcke – also die Kapazität des Modells, komplexe Muster zu lernen. Dieses kontrollierte Design ermöglicht dem Team zu untersuchen, wie viel Komplexität wirklich für eine verlässliche Krebsklassifikation erforderlich ist.
Training, Testen und die fairste Modellwahl
Um die Modelle zu trainieren und zu testen, stellen die Autoren eine ausgeglichene Sammlung von 15.000 Lungengewebebildern zusammen, die sorgfältig in Trainings-, Validierungs- und Testgruppen mit gleichen Anteilen jeder Klasse aufgeteilt sind. Vor dem Training wird jedes Bild skaliert, normalisiert und vorsichtig durch Spiegelungen, kleine Rotationen und Zooms augmentiert, um die Variationen zu simulieren, wie Präparate unter unterschiedlichen Bedingungen erscheinen können. Entscheidend ist, dass das Team die Modelle nicht allein an der Rohgenauigkeit misst, weil diese Metrik schlechte Leistungen einer Klasse verbergen kann. Stattdessen verwenden sie die Macro-F1-Maßzahl, die das Modell dazu zwingt, bei allen drei Gewebearten gut zu sein, nicht nur bei den einfachsten. Ein maßgeschneidertes Trainingsverfahren überwacht kontinuierlich diese ausgewogene Kennzahl und stoppt das Training automatisch, wenn Verbesserungen ausbleiben, wobei die beste Version jedes Modells zur Vergleichbarkeit gesichert wird. 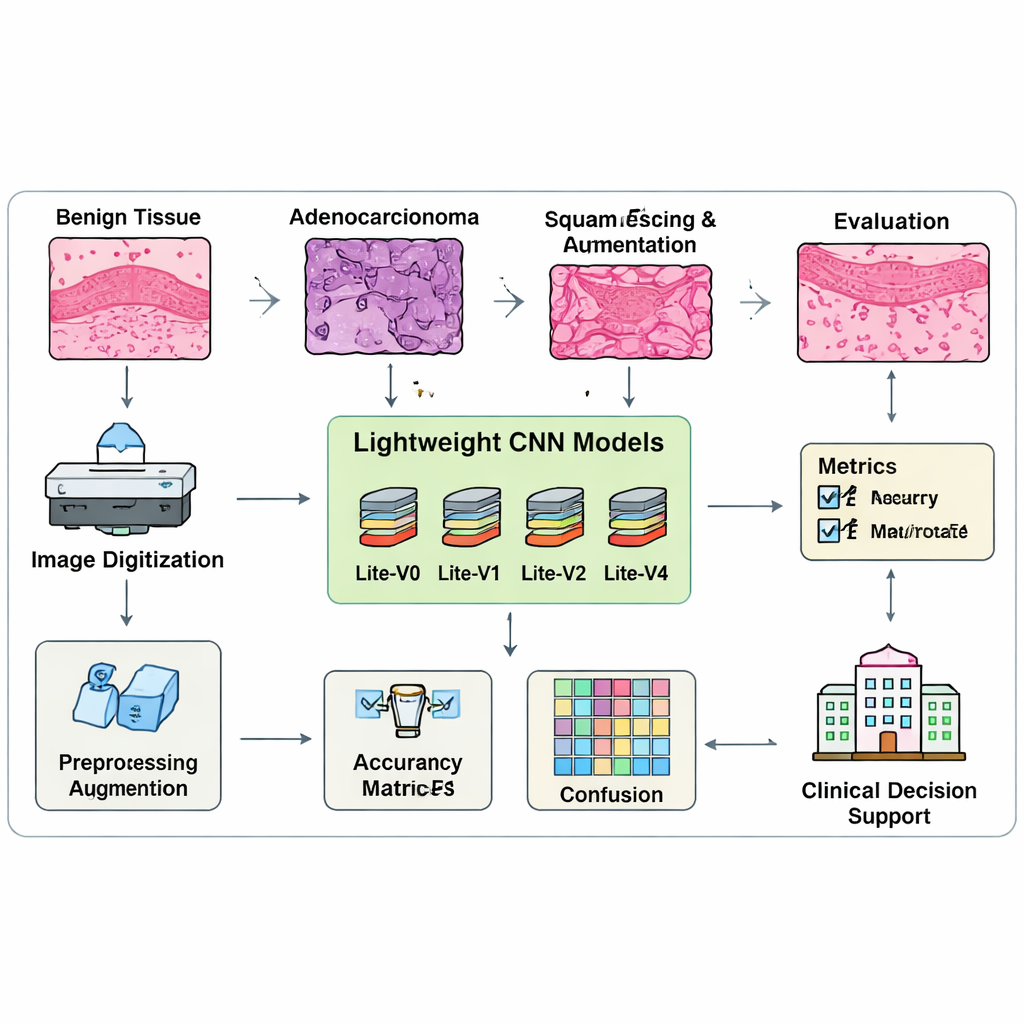
Was das beste leichte Modell wirklich leisten kann
Am Ende sticht eine Variante – Lite-V2 – hervor. Sie ist weder das kleinste noch das größte Netzwerk, sondern liegt in der Mitte und erreicht das beste Gleichgewicht zwischen Genauigkeit und Effizienz. Auf bisher ungesehenen Testbildern klassifiziert Lite-V2 gutartiges Gewebe, Adenokarzinom und Plattenepithelkarzinom mit hoher und gleichmäßig verteilter Leistung und erreicht eine Macro-F1-Score von etwa 0,96. Verwechslungs-Matrizen zeigen, dass die drei Kategorien selten durcheinandergebracht werden, während tiefere Versionen zu überanpassen beginnen, das Trainingmaterial auswendig lernen und an Zuverlässigkeit bei neuen Fällen verlieren. Die Autoren führen Lite-V2 zudem mehrfach mit unterschiedlichen zufälligen Startbedingungen aus und verwenden einen statistischen Test, um zu bestätigen, dass sein Vorteil gegenüber den anderen Varianten kein Zufall ist. 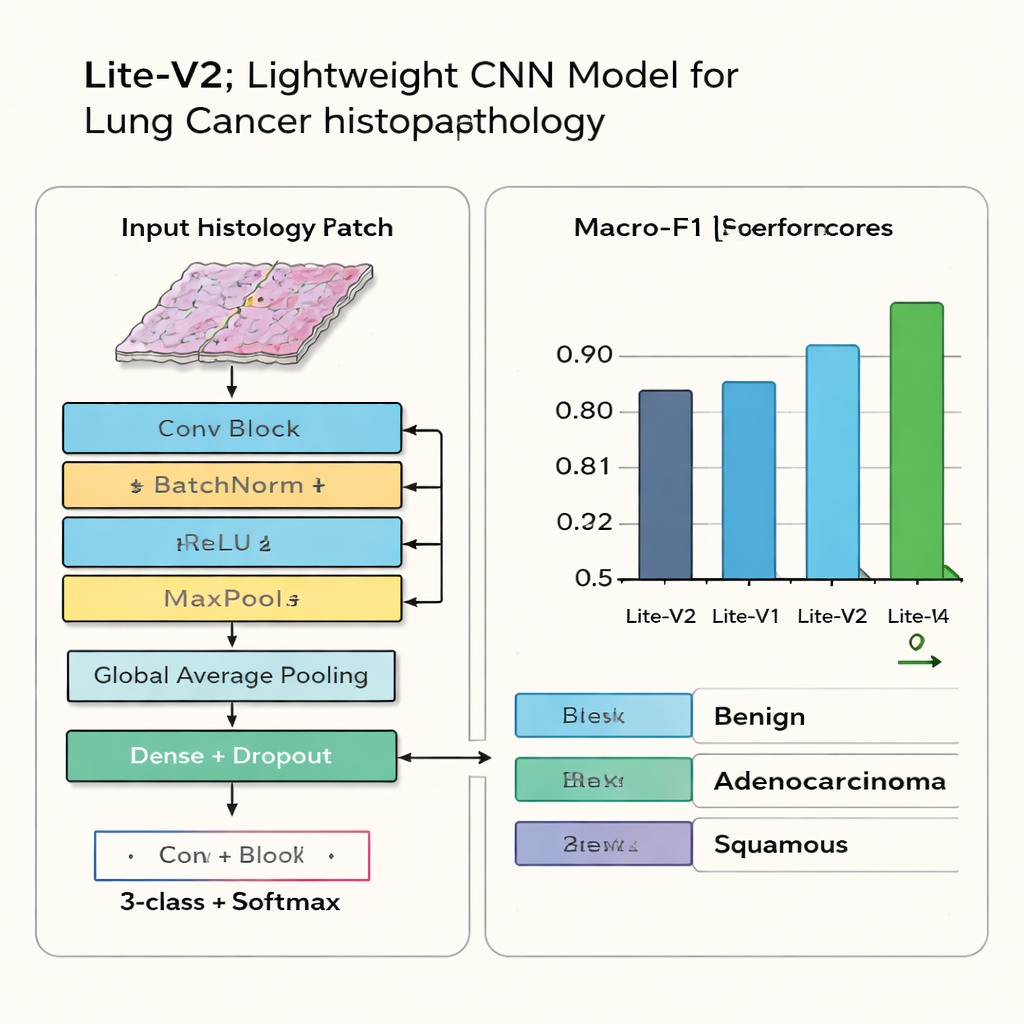
Vom Forschungscode zur Unterstützung in der Praxis
Über Leistungszahlen hinaus betont die Studie die praktische Einsetzbarkeit. Da Lite-V2 und seine Schwestermodelle kompakt sind, können sie auf bescheidener Krankenhaus-Hardware oder sogar auf Edge-Geräten laufen, ohne sensible Bilder in die Cloud zu schicken. Die Autoren veröffentlichen einen reproduzierbaren Rahmen, der jedes experimentelle Detail protokolliert, von der Datenverarbeitung bis zu Trainingsverläufen und Fehlerbildern, sodass andere Teams die Arbeit überprüfen oder ausbauen können. Für Patientinnen, Patienten und Klinikpersonal ist die zentrale Botschaft: Durchdacht entworfene, leichte KI kann die verlässliche Lungenkrebsklassifikation näher an die tägliche Pathologiepraxis bringen und schnellere, konsistentere Entscheidungen unterstützen – auch in Kliniken ohne Spitzenrechner.
Zitation: Raza, A., Hanif, F. & Mohammed, H.A. Clinical validation of lightweight CNN architectures for reliable multi-class classification of lung cancer using histopathological imaging techniques. Sci Rep 16, 6512 (2026). https://doi.org/10.1038/s41598-026-36652-6
Schlüsselwörter: Lungenkrebs, Histopathologie, konvolutionale neuronale Netze, medizinische Bildgebungs-KI, computerunterstützte Diagnose