Clear Sky Science · de
Nicotinamid wirkt Rotenon-induzierter mitochondrialer und neuronaler Dysfunktion in einem translationalen Modell der frühen Lebensphase entgegen
Warum winzige Zellmotoren für das sich entwickelnde Gehirn wichtig sind
Während der Gehirnentwicklung müssen Milliarden junger Nervenzellen lange Verzweigungen ausbilden und präzise Verbindungen formen. Diese Studie untersucht, wie die „Kraftwerke“ der Zelle — die Mitochondrien — diesen Prozess beeinflussen und was passiert, wenn sie durch eine pesticideähnliche Verbindung subtil vergiftet werden. Die Forschenden prüfen außerdem, ob ein verbreitetes, an Vitaminen angelehntes Molekül, Nicotinamid, entwickelnde Gehirnzellen vor diesem verdeckten Energiestress schützen kann, mit möglichen Folgen für Erkrankungen wie Schizophrenie.
Vom Pestizid-Modell zum Experiment an Gehirnzellen
Das Team baute auf früheren Arbeiten auf, die zeigten, dass neugeborene Ratten, die kurzzeitig Rotenon ausgesetzt waren — ein Pestizid, das einen wichtigen Schritt der mitochondrialen Energieproduktion (Komplex I) blockiert — später Verhaltensweisen zeigen, die an Schizophrenie erinnern. Um zu verstehen, was auf der Ebene einzelner Gehirnzellen geschieht, isolierten sie unreife Nervenzellen aus der Rattenrinde und setzten sie genau der Konzentration von Rotenon aus, die in den Gehirnen der Tiere gemessen worden war. Dieser „translationale“ Ansatz erlaubte die Frage: Führt Rotenon bei realistischen, niedrigen Dosen, die die Zellen nicht abtöten, dennoch dazu, dass Neuronen in ihrem Wachstum und ihrer Verschaltung fehlgeleitet werden?
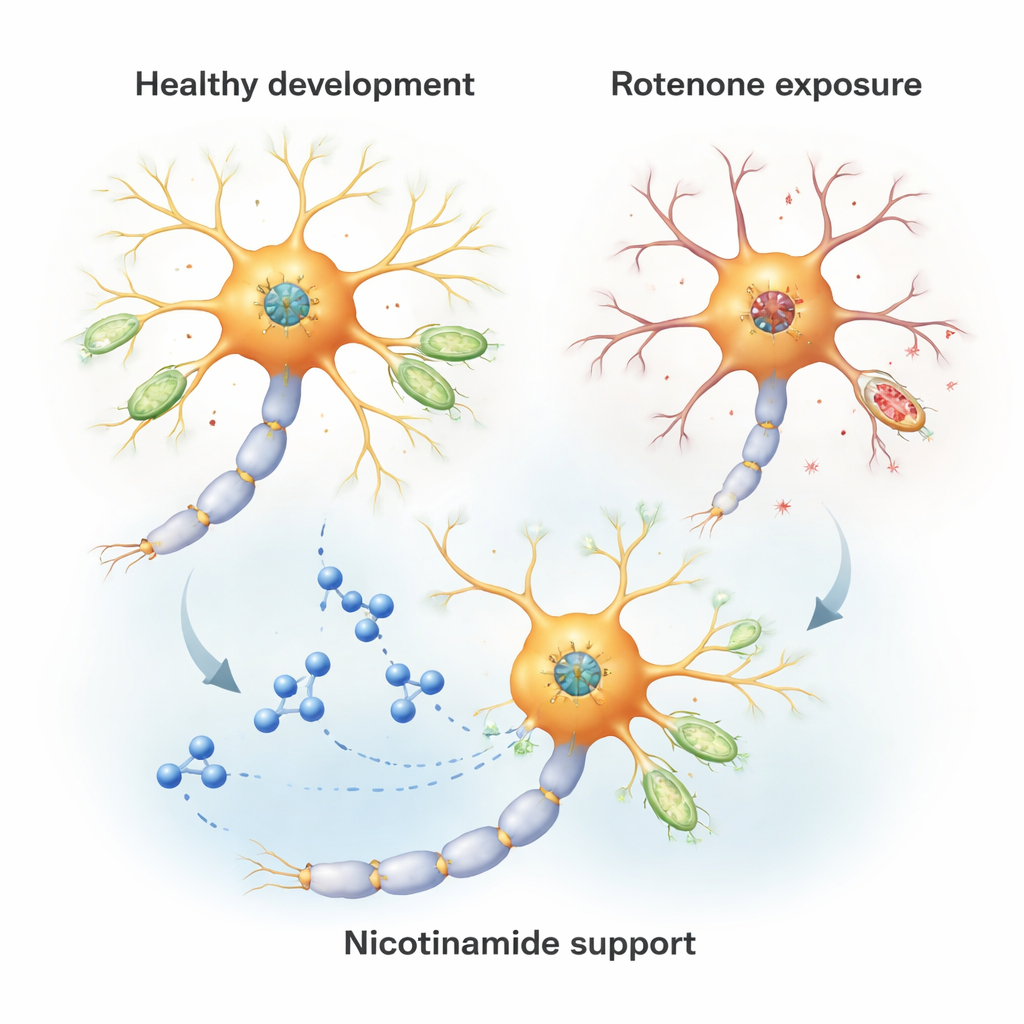
Energieabfall ohne offensichtlichen Zelltod
Überraschenderweise führte die niedrige Rotenon-Dosis nicht zum Absterben der Neuronen und störte auch nicht das grundlegende Kalziumgleichgewicht oder die elektrische Ladung über mitochondrialen Membranen — Merkmale, die oft bei akuten Zellschäden zu sehen sind. Stattdessen zeigte sich eine leisere, aber wichtige Verschiebung im Stoffwechsel. Mitochondrien produzierten weniger Energie (ATP) und verbrauchten weniger Sauerstoff, und die Gesamtaktivität von Komplex I sank. Gleichzeitig nahm die Produktion eines bestimmten reaktiven Moleküls, mitochondrialer Superoxid, ab statt zuzunehmen. Dieser Befund steht im Gegensatz zu Studien mit hohen Rotenon-Dosen, die meist einen toxischen Anstieg reaktiver Sauerstoffspezies berichten. Hier ergibt sich das Bild eines „langsamen Motors“ statt eines rauchenden, überhitzten Aggregats.
Veränderungen in Qualitätskontrolle und Zellgestalt
Wenn die mitochondriale Leistung nachlässt, formen Zellen diese Organellen typischerweise um und recyceln sie. Die Forschenden fanden Hinweise darauf, dass dieses Qualitätskontrollsystem gestört war. Proteine, die am Zerschneiden und Umbauen von Mitochondrien beteiligt sind, sowie solche, die die Anzahl der Mitochondrien markieren, waren nach Rotenon-Exposition verändert. Komponenten des zellulären Recyclingwegs (Autophagie) häuften sich ebenfalls in Mustern, die darauf hindeuten, dass Abfallpakete gebildet, aber nicht effizient abgebaut wurden. Gleichzeitig wurden die Neuronen selbst strukturell einfacher: Ihre baumartigen Dendriten waren kürzer und weniger zahlreich. Da Dendriten entscheidend für den Empfang von Signalen sind, deutet dieses Beschneiden darauf hin, dass selbst milder, chronischer mitochondrialer Stress bleibende Spuren in der Gehirnverschaltung hinterlassen kann.
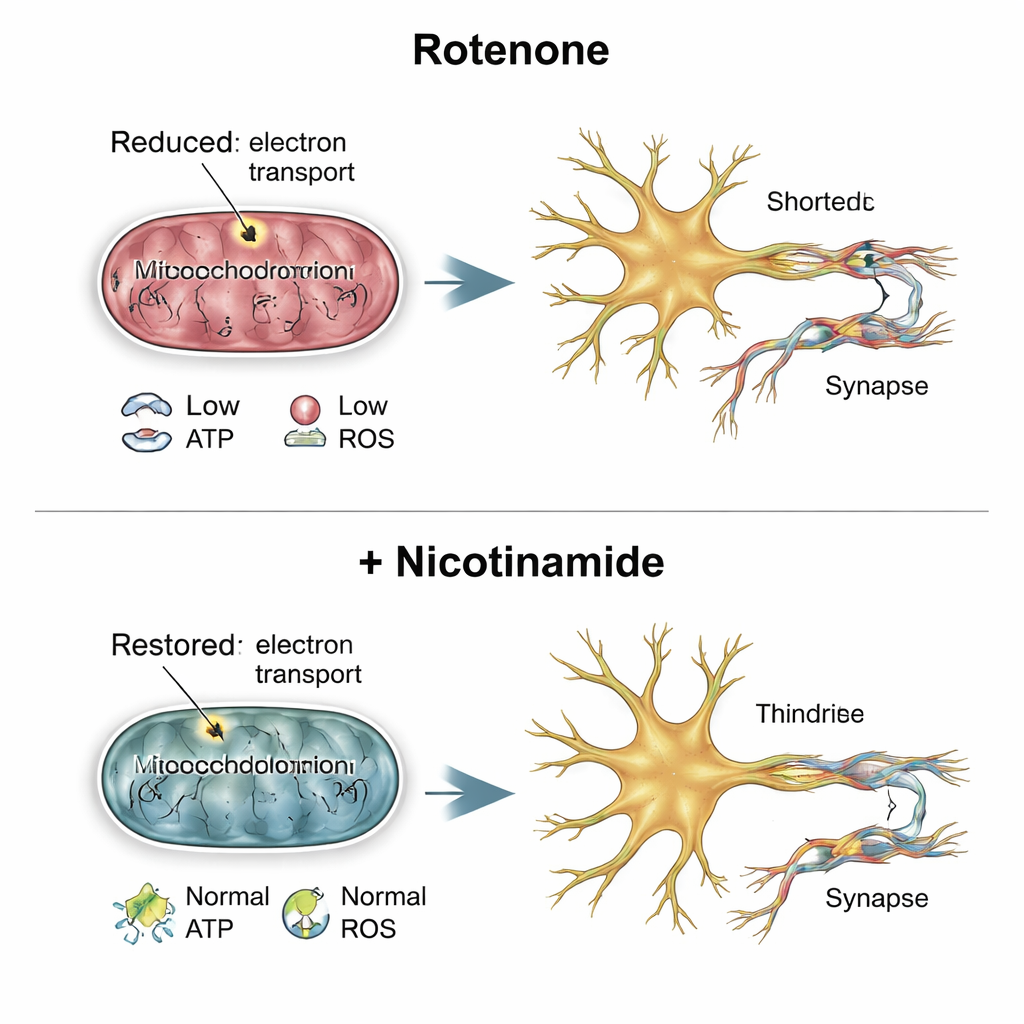
Geschwächte Synapsen und wie Nicotinamid hilft
Das Team fragte dann, ob die Kommunikationspunkte zwischen Neuronen — die Synapsen — betroffen sind. Mit fluoreszierenden Markern für prä- und postsynaptische Proteine beobachteten sie, dass rotènon-behandelte Neuronen mehr synaptische Komponenten aufwiesen, aber eine schlechtere Ausrichtung zwischen diesen, was impliziert, dass die Maschinerie sich anhäufte, ohne voll funktionsfähige Verbindungen zu bilden. Die Gabe von Nicotinamid vor der Rotenon-Exposition veränderte dieses Bild. Nicotinamid, ein Baustein für das energietragende Molekül NAD, stellte die mitochondriale Atmung, ATP-Spiegel und Superoxidproduktion wieder auf normale Werte zurück. Es normalisierte außerdem Recyclingmarker, reduzierte die abnorme Ansammlung synaptischer Proteine, verbesserte deren Ausrichtung und brachte Anzahl und Länge der Dendriten wieder auf das Niveau unbehandelter Zellen.
Was das für Gehirnerkrankungen bedeuten könnte
Insgesamt deuten die Ergebnisse darauf hin, dass selbst mäßige, nicht-tödliche Beeinträchtigungen der mitochondrialen Funktion in frühen Lebensphasen weitreichende Folgen für Zellgestalt und Synapsenbildung haben können — Prozesse, die bei Störungen wie Schizophrenie verändert sein sollen. Nicotinamid setzte nicht jede molekulare Veränderung rückgängig, war aber ausreichend, um Energiehaushalt, Recyclingsysteme, dendritische Architektur und synaptische Organisation in diesem Zellkulturmodell zu retten. Für Laien lautet die Kernbotschaft, dass die Gesundheit der zellulären „Kraftwerke“ während der Entwicklung zentral für den Aufbau robuster Gehirnschaltkreise sein könnte und dass die Unterstützung mitochondrialer Energiewege mit an Vitamin B3 verwandten Molekülen ein Weg sein könnte, subtile frühkindliche Schädigungen abzufedern. Zwar ist noch viel Arbeit nötig, bevor eine Behandlung für Menschen in Betracht gezogen werden kann, doch bietet diese Studie eine mechanistische Verbindung zwischen Umweltexpositionen, mitochondrialem Stress und langfristiger Gehirngesundheit.
Zitation: Siena, A., Souza e Silva, L.F., Araujo, V.C. et al. Nicotinamide counteracts Rotenone-induced mitochondrial and neuronal dysfunction in a translational early-life model. Sci Rep 16, 7159 (2026). https://doi.org/10.1038/s41598-026-36651-7
Schlüsselwörter: Mitochondrien, Gehirnentwicklung, Schizophrenie, Nicotinamid, Rotenon