Clear Sky Science · de
Eine automatische Methode zur Bewertung der kongenitalen Radio‑ulnaren Synostose (CRUS‑DE): Integration von TLT‑SAM und GPMM‑R zur Landmarkenbestimmung
Warum das für Armoperationen bei Kindern wichtig ist
Bei einigen Kindern sind die beiden Unterarmknochen in der Nähe des Ellenbogens von Geburt an miteinander verwachsen, ein Zustand, der als kongenitale Radio‑ulnare Synostose bezeichnet wird. Weil sich die Knochen nicht richtig drehen können, sind einfache Tätigkeiten wie das Drehen eines Türknaufs oder die Benutzung von Besteck erschwert oder unmöglich. Chirurgen können das Problem durch sorgfältig geplante Knochenschnitte korrigieren, doch heute erfolgt diese Planung oft langsam und stark abhängig von individueller Erfahrung. Diese Studie stellt eine computergestützte Methode vor, die Standard‑CT‑Scans auswertet und automatisch misst, wie stark die Knochen verdreht und gebogen sind, mit dem Ziel, die Behandlung präziser, reproduzierbarer und breiter verfügbar zu machen.
Wenn zwei Unterarmknochen als einer wachsen
Im gesunden Arm wirken Radius und Ulna wie zwei parallele Schienen, die umeinander rollen können und so das Drehen der Hand mit Handfläche nach oben oder unten ermöglichen. Bei der kongenitalen Radio‑ulnaren Synostose ist ein Abschnitt dieser Knochen von Geburt an, meist in Ellenbogennähe, verwachsen. Das fixiert den Unterarm in einer festen Drehstellung und führt häufig zusätzlich zu Biegungen in mehreren Richtungen, was Alltagsaktivitäten einschränkt und Selbstvertrauen sowie soziale Teilhabe beeinträchtigen kann. Chirurgen können eine Osteotomie durchführen — den Knochen durchtrennen und neu ausrichten — um die Funktion zu verbessern. Um jedoch zu entscheiden, wo und wie viel geschnitten werden muss, müssen sie die Deformität zuerst dreidimensional quantifizieren, eine Aufgabe, die auf Röntgenbildern oder selbst CT‑Bildern visuell extrem schwierig ist. 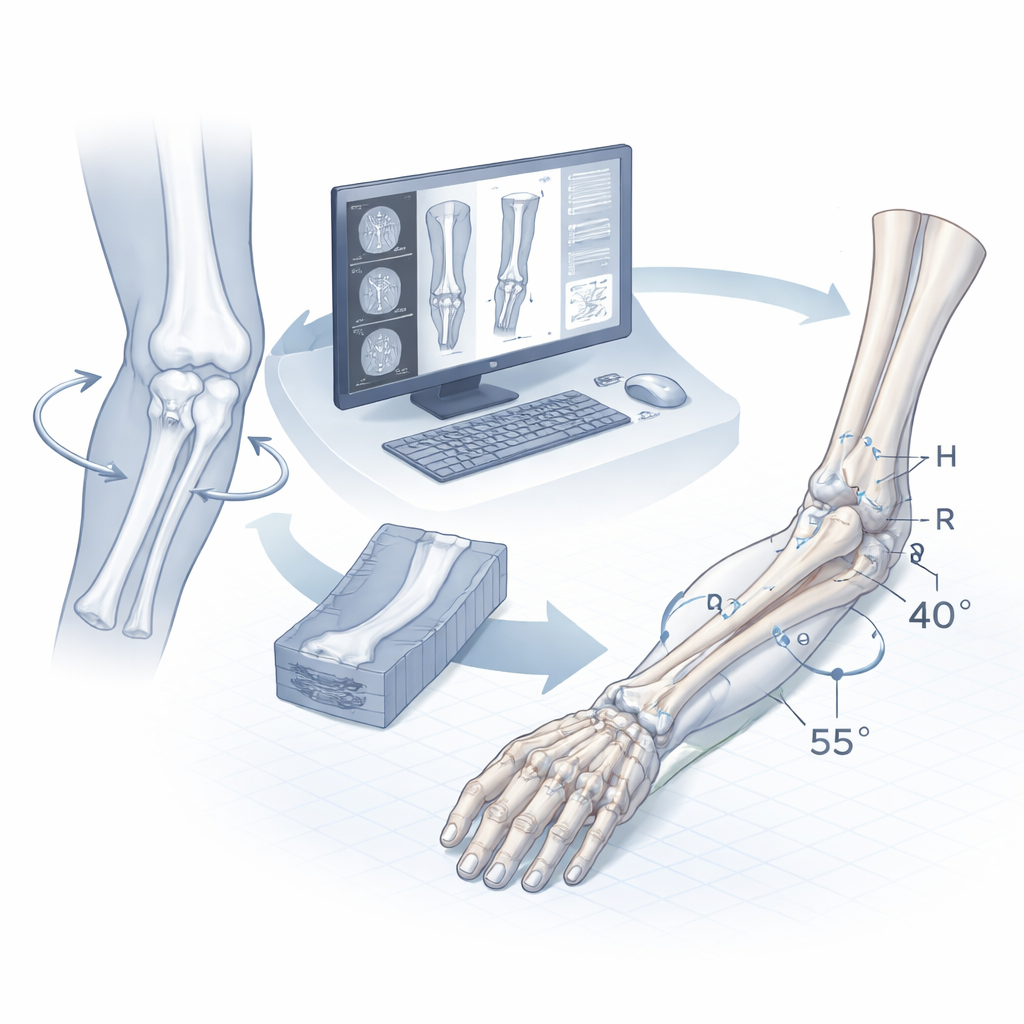
Computern beibringen, Kinderknochen zu erkennen
Die Forschenden entwickelten eine Pipeline, die sie CRUS‑DE nennen und die bei gewöhnlichen CT‑Scans beider Unterarme ansetzt. Zuerst muss das System die Knochen finden und vom umliegenden Gewebe trennen. Anstatt ein großes Deep‑Learning‑Netz zu trainieren, das Tausende seltener pädiatrischer Fälle benötigen würde, kombinierte das Team eine traditionelle „Threshold“-Methode mit einem modernen Vision‑Werkzeug, dem Segment Anything Model. Ihre Threshold‑Layer‑Verfolgung folgt dem knöchernen Erscheinungsbild schichtweise durch den Scan, während das neuere Modell die Konturen bereinigt und vervollständigt, selbst dort, wo der Knochen schwach oder teilweise unscharf erscheint. Tests gegen sorgfältige manuelle Segmentierungen durch einen erfahrenen Chirurgen zeigten, dass dieser hybride Ansatz die menschlichen Konturen sehr genau nachbildet.
Kleine Landmarken auf wachsenden Knochen lokalisieren
Exakte Messungen beruhen auf einem konsistenten Satz anatomischer Landmarken: kleinen Erhebungen, Spitzen und Kanten an Radius und Ulna, die lokale Koordinatensysteme definieren. Bei Kindern sind diese Merkmale oft glatt und subtil, und bei verwachsenen Knochen können sie verzerrt oder teilweise fehlen. Um damit umzugehen, bauten die Autorinnen und Autoren statistische „Form‑Vorlagen“ normaler pädiatrischer Knochen mithilfe einer Technik namens Gaussian Process Morphable Models auf. Der Computer lernt, wie Knochenformen typischerweise über viele gesunde Kinder hinweg variieren, und verformt diese Vorlage behutsam, um zu jedem neuen Patienten zu passen. Aus dieser Anpassung erhält er vorläufige Landmarkenpositionen, die dann mit einfachen, anatomisch abgestimmten geometrischen Regeln verfeinert werden — etwa durch Auswahl des am stärksten hervortretenden Punktes in einer kleinen Nachbarschaft. Über 40 Knochen betrug der durchschnittliche Abstand zwischen automatisch und von Experten definierten Landmarken etwa ein bis anderthalb Millimeter, ohne nennenswerte Unterschiede zur manuellen Markierung. 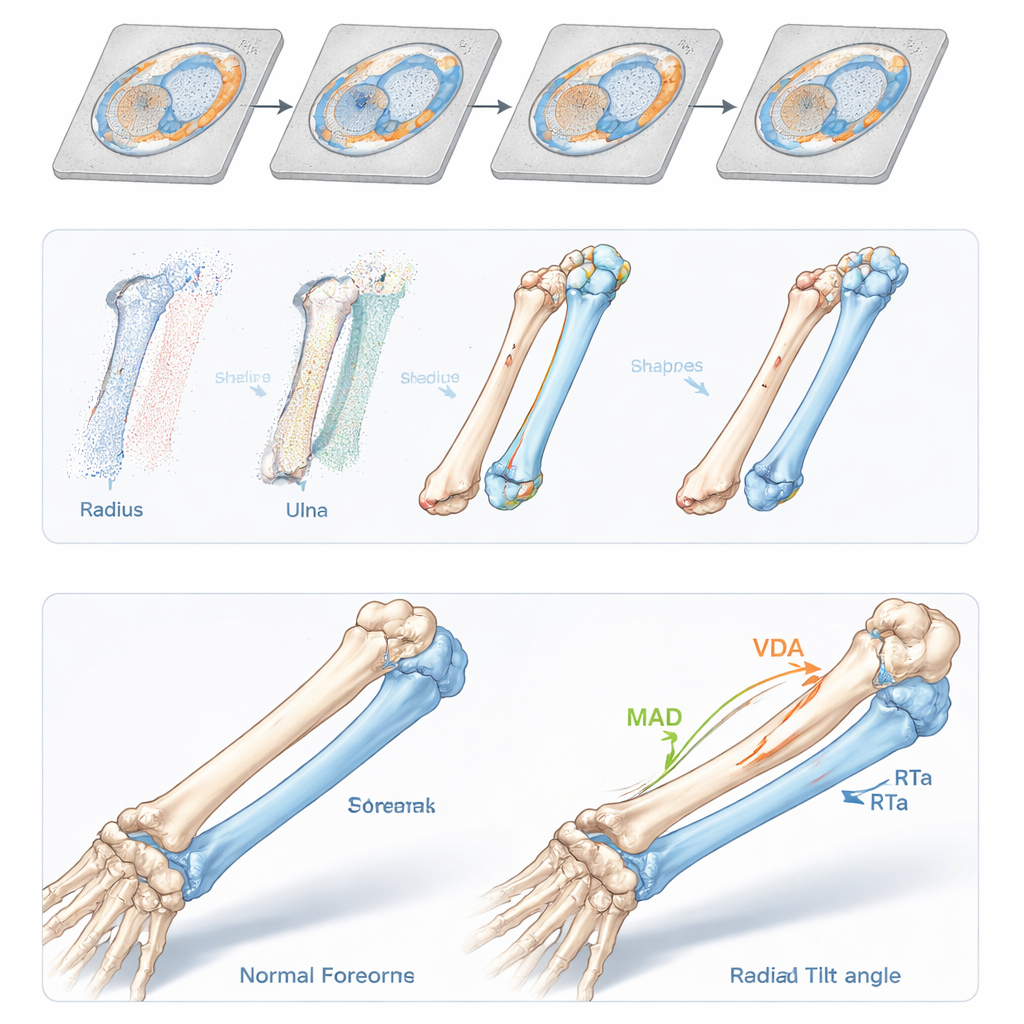
Formen in aussagekräftige Winkel verwandeln
Mit segmentierten Knochen und identifizierten Landmarken konstruiert CRUS‑DE lokale Koordinatensysteme am Handgelenk und Ellenbogen. Es richtet den betroffenen Unterarm eines Patienten an einer normalen Referenz aus und berechnet, wie stark sich Radius und Ulna in verschiedene Richtungen abweichen — zur Daumen‑ oder Kleinfingerseite, zur Handinnen‑ oder Handrückenseite und inwieweit sie nach innen gedreht sind. Bei 40 Unterarmen, einschließlich normaler und verwachsener Fälle, unterschieden sich die automatisch berechneten Winkel im Mittel um weniger als etwa 2,5 Grad von Expertenmessungen. Wichtig ist, dass alle sechs gemessenen Winkel normal von CRUS‑Unterarmen klar unterschieden, wobei sowohl die zusätzlichen Biegungen als auch die oft sehr große Innenrotation der Patientinnen und Patienten erfasst wurden.
Was das für die Zukunft der Chirurgie bedeuten könnte
Für Familien ist die zentrale Botschaft, dass Computer Chirurgen inzwischen dabei unterstützen können, die Unterarmdeformität eines Kindes in präzisen, objektiven Zahlen statt in groben visuellen Eindrücken zu beschreiben. Diese Methode verwandelt CT‑Daten in ein 3D‑Modell mit hervorgehobenen Landmarken und quantifizierten Winkeln, die genau zeigen, wie die Knochen fehlgestellt sind. Solche Informationen können die präoperative Planung leiten, weniger erfahrenen Chirurgen helfen, ähnliche Ergebnisse wie Experten zu erzielen, und die Bewertung des Operationserfolgs im Anschluss erleichtern. Die Autoren sehen auch vor, diese automatischen Messungen mit individuellen Schnittschablonen und robotischen Werkzeugen zu kombinieren, was langfristig zu sichereren, genaueren und stärker personalisierten Eingriffen für Kinder mit dieser herausfordernden Fehlbildung führen könnte.
Zitation: Liu, L., Cui, Y., Zhou, T. et al. An automatic congenital radio-ulnar synostosis deformity evaluation method (CRUS-DE): integrating TLT-SAM and GPMM-R for landmark identification. Sci Rep 16, 6434 (2026). https://doi.org/10.1038/s41598-026-36638-4
Schlüsselwörter: kongenitale Radio‑ulnare Synostose, Unterarmdeformität, Osteotomie‑Planung, medizinische Bildanalyse, pädiatrische Orthopädie