Clear Sky Science · de
Antibakterielle, antibiofilm- und metabolomische Profilbildung der neu entdeckten Süßwasserpilze Longipedicellata megafusiformis und Wicklowia fusiformispora
Verborgene Verbündete im Kampf gegen Superkeime
Während Mediziner mit Infektionen ringen, die auf unsere üblichen Antibiotika nicht mehr ansprechen, suchen Wissenschaftler nach neuen Waffen an unerwarteten Orten. Diese Studie wendet sich verrottendem Holz in tropischen Flüssen zu und entdeckt zwei wenig erforschte Süßwasserpilze, die ein reichhaltiges Cocktail aus natürlichen Chemikalien produzieren, das gefährliche Bakterien verlangsamen und die schleimigen Filme blockieren kann, die ihnen auf medizinischen Geräten und Geweben das Überleben erleichtern.
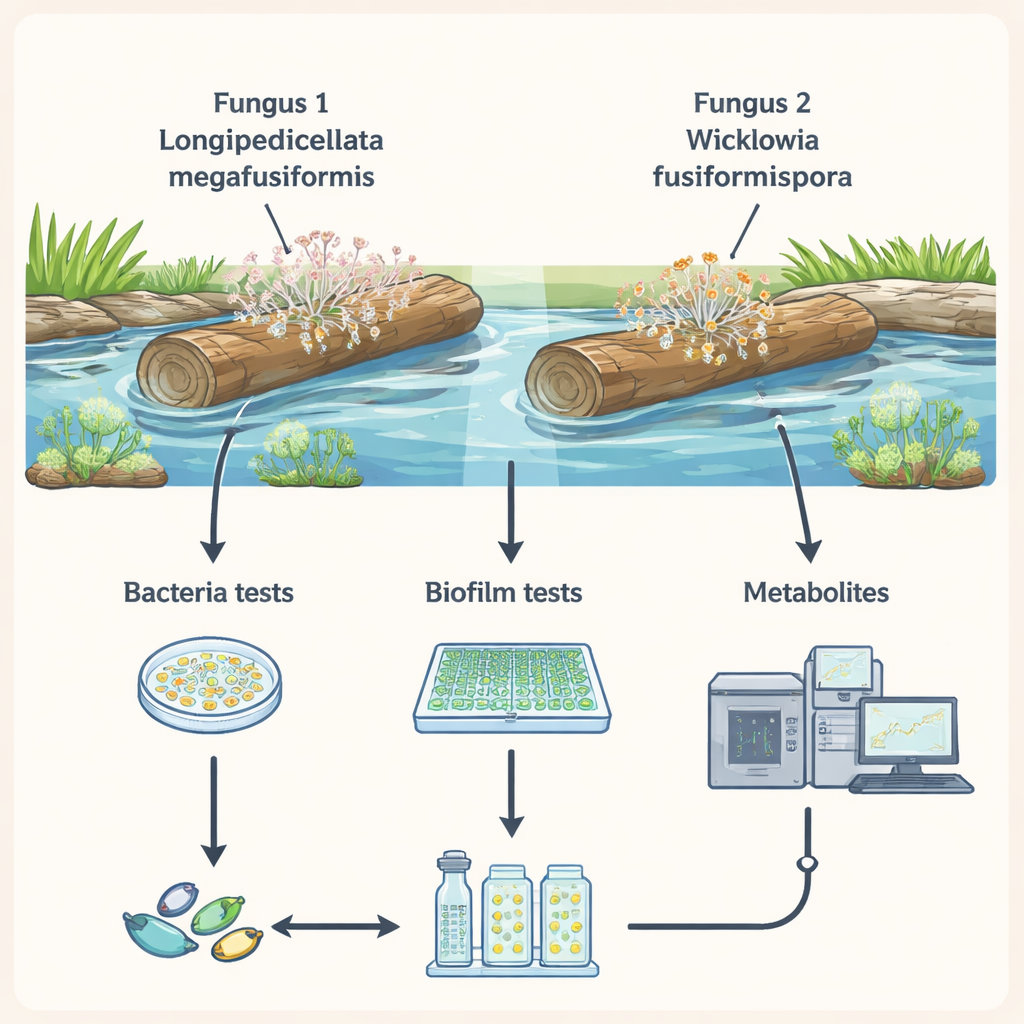
Flusswood als Apotheke
In den warmen Bächen Nordthailands bauen Pilze still fallengebliebene Zweige ab und recyceln Nährstoffe ins Ökosystem. Die Forschenden isolierten zwei neu beschriebene Pilze aus untergetauchtem Holz und züchteten sie im Labor. Im Fokus standen die sogenannten „sekundären Metabolite“, die diese Pilze freisetzen—kleine Moleküle, die nicht für das Grundüberleben nötig sind, sondern als chemische Abwehrstoffe und Werkzeuge in ihren mikroskopischen Auseinandersetzungen mit benachbarten Mikroben dienen. Da Süßwasserpilze weit weniger untersucht sind als ihre terrestrischen oder marinen Verwandten, könnten sie bislang unerschlossene Sammlungen nützlicher, antibiotikaähnlicher Substanzen bergen.
Die Pilzextrakte auf dem Prüfstand
Das Team extrahierte Gemische aus den Pilzkulturen mit einem gebräuchlichen Lösungsmittel und prüfte sie gegen vier bekannte bakterielle Problemkeime, darunter Staphylococcus aureus und Escherichia coli. Auf Agarplatten erzeugten alle Pilzextrakte klare, bakterienfreie Bereiche, was zeigte, dass die Gemische sowohl das Wachstum von grampositiven als auch gramnegativen Bakterien stoppen konnten. Als die Forschenden die niedrigste Dosis bestimmten, die in Flüssigkultur noch Wachstum hemmt, zeigten beide Pilze Aktivität im Mikrogramm-pro-Milliliter-Bereich—stark genug, um wissenschaftliches Interesse zu wecken, auch wenn sie noch nicht mit Standardwirkstoffen wie Ampicillin konkurrieren.
Bakterielle Festungen aufbrechen
Da viele hartnäckige Infektionen von Biofilmen abhängen—klebrigen, geschichteten Gemeinschaften, die Bakterien vor Antibiotika schützen—prüften die Forschenden auch, ob die Pilzgemsiche diese Schutzschicht stören können. In einem Plattentest ließen sie Bakterien in Anwesenheit der Pilzextrakte Biofilme anlegen und färbten anschließend den verbleibenden Schleim. Beide Pilze reduzierten die Biofilmbildung bei der getesteten Dosis um etwa die Hälfte oder mehr, einige Kombinationen schnitten die Bildung um über 70% zurück. Diese Ergebnisse deuten darauf hin, dass die natürlichen Gemische frühe Stadien der Biofilmbildung schwächen können—eine vielversprechende Eigenschaft zur Vorbeugung von Infektionen an Kathetern, Implantaten und anderen medizinischen Oberflächen, obwohl hier nicht auf gereifte, bereits etablierte Biofilme eingegangen wurde.
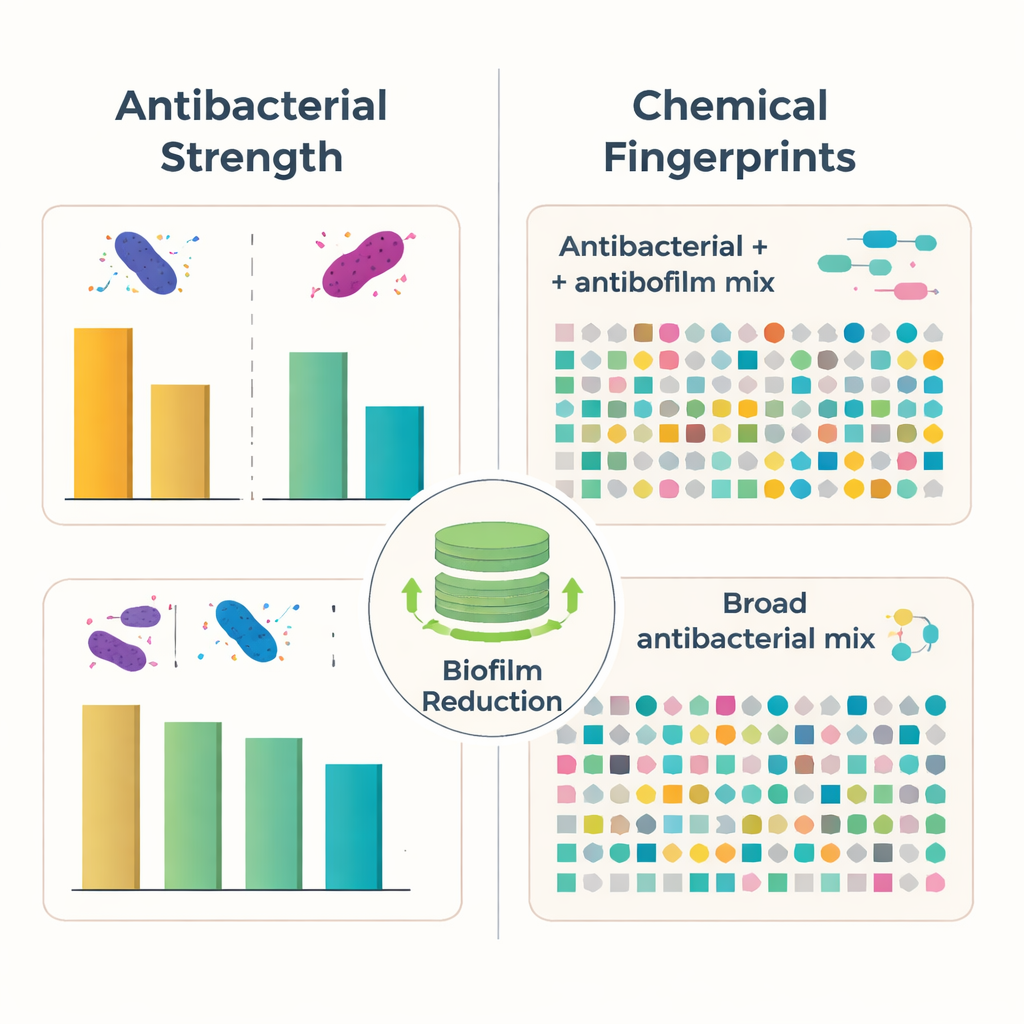
Ein Blick in die chemische Werkzeugkiste
Um zu verstehen, was diesen Effekten zugrunde liegen könnte, verwendete das Team hochauflösende Flüssigchromatographie–Massenspektrometrie, eine Technik, die Moleküle mit hoher Präzision trennt und gewichtet, um einen „chemischen Fingerabdruck“ für jeden Pilz zu skizzieren. Eine Art, Longipedicellata megafusiformis, enthielt mindestens 27 verschiedene Verbindungen, darunter Alkaloide, Peptide, pigmentähnliche Moleküle und andere Strukturen, die in der wissenschaftlichen Literatur bereits als bakterienhemmend oder biofilmstörend beschrieben sind. Der andere, Wicklowia fusiformispora, produzierte mindestens 33 verschiedene Verbindungen und bildete damit eine breit gefächerte antibakterielle Mischung, ohne dass einzelne Moleküle bislang direkt auf Biofilme zurückgeführt werden konnten. In beiden Pilzen weist die chemische Diversität auf eine komplexe Strategie hin: Statt sich auf eine einzelne Wunderwaffe zu verlassen, setzen sie gleichzeitig viele verwandte und unzusammenhängende Moleküle ein.
Was das für zukünftige Arzneimittel bedeutet
Für Nichtfachleute lautet die Kernbotschaft, dass unscheinbare Flusspilze ausgeklügelte chemische Gemische herstellen können, die schädliche Bakterien verlangsamen und ihre schützenden Schleimschichten untergraben. Die Studie erhebt keinen Anspruch, ein fertiges Medikament gefunden zu haben; vielmehr kartiert sie, wo sich die vielversprechendsten Moleküle verbergen könnten, und zeigt, dass ganze Extrakte bereits bedeutende antibakterielle und antibiofilmische Effekte besitzen. Durch die Kombination klassischer Labortests mit moderner chemischer Profilierung legt die Arbeit eine Roadmap für künftige Anstrengungen vor, die stärksten Inhaltsstoffe zu isolieren, zu verfeinern und zu verstehen—Schritte, die diese stillen Flussbewohner letztlich zu wertvollen Verbündeten im Kampf gegen antibiotikaresistente Infektionen machen könnten.
Zitation: Khruengsai, S., Sripahco, T., Kittakoop, P. et al. Antibacterial, antibiofilm, and metabolomic profiling of the novel freshwater fungi Longipedicellata megafusiformis and Wicklowia fusiformispora. Sci Rep 16, 6083 (2026). https://doi.org/10.1038/s41598-026-36637-5
Schlüsselwörter: Süßwasserpilze, Antibiotikaresistenz, Biofilme, Naturstoffe, antibakterielle Verbindungen