Clear Sky Science · de
Die morpho-kinetische Landschaft makrophagaler Modi während der Wundheilung bei Zebrafischen
Warum winzige Wundhelfer wichtig sind
Jeder Schnitt oder Kratzer in unserer Haut löst einen komplizierten Reparaturprozess aus, den unser Körper meist unbemerkt bewältigt. Zentral für diesen Vorgang sind Makrophagen – wandernde Immunzellen, die Trümmer beseitigen, Erreger bekämpfen und den Wiederaufbau von Gewebe unterstützen. In dieser Studie werden transparente Zebrafischlarven und moderne Bildgebung genutzt, um Tausende einzelner Makrophagen in Aktion zu beobachten und zu zeigen, wie sich ihre Form und Bewegungsmuster im Verlauf der Wundheilung verändern. Das Verständnis dieser feinen Verhaltensweisen könnte eines Tages Ärzten helfen, Entzündungen gezielter zu steuern und die Heilung chronischer Wunden sowie anderer Erkrankungen zu verbessern.
Immunzellen in Bewegung
Makrophagen werden oft in zwei breite Modi eingeteilt. Kurz nach einer Verletzung lösen „M1-ähnliche“ Zellen Entzündungen aus, töten Mikroben und räumen Trümmer weg. Später helfen „M2-ähnliche“ Zellen, die Entzündung zu dämpfen und die Gewebereparatur zu unterstützen. In lebendem Gewebe ist dieser Wechsel jedoch kein simpler Ein-/Ausschalter. An Modellen mit Schwanzflossenverletzungen von Zebrafischen filmten die Forschenden Makrophagen in Echtzeit und nutzten Computerwerkzeuge, um den Weg und die Kontur jeder Zelle zu verfolgen. Aus diesen Zeitrafferfilmen extrahierten sie 63 verschiedene Messgrößen, die beschreiben, wie rund oder länglich jede Zelle war, wie schnell sie sich bewegte, wie gerade oder verschlungen ihre Bahn verlief und wie sie sich in Relation zur Wunde bewegte.
Verschiedene Aufgaben, verschiedene Bewegungsstile
Beim Vergleich früher M1-ähnlicher Makrophagen mit späteren M2-ähnlichen fanden die Autoren deutliche Verhaltensunterschiede. M1-ähnliche Zellen waren im Allgemeinen runder und bewegten sich in geraderen, stärker gerichteten Bahnen, die sie zur Wunde lenkten und in deren Nähe hielten. M2-ähnliche Zellen dagegen waren stärker verlängert, streiften in geschlungenen oder mäandrierenden Bahnen umher und hielten sich tendenziell weiter von der Verletzung entfernt. Die Forschenden quantifizierten „zufallsähnliche“ Bewegungen, indem sie nach Bahnen suchten, die sich selbst kreuzten; M2-ähnliche Zellen verbrachten mehr Zeit in diesen Schleifenmustern, was zu einem eher erkundenden oder weniger streng geleiteten Verhalten passt, sobald die akute Entzündungsphase vorüber ist.
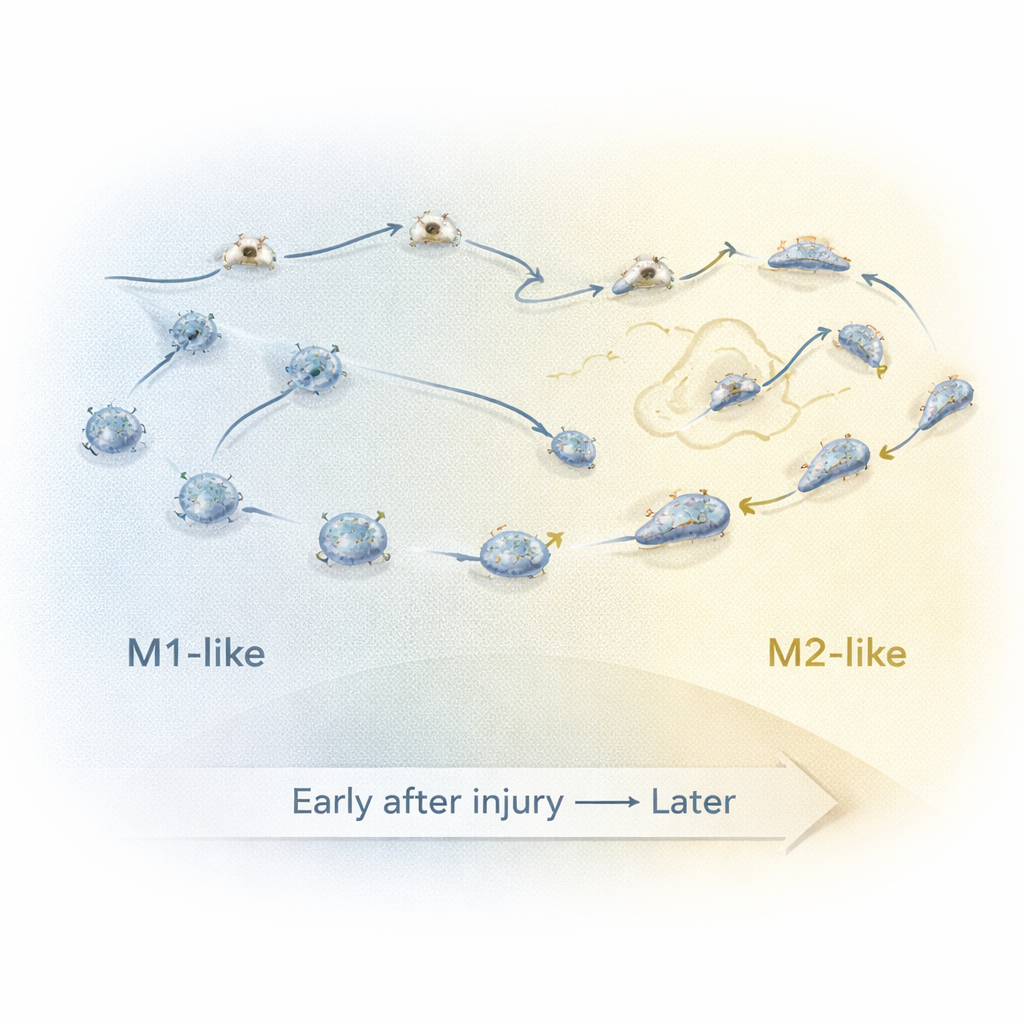
Zellen im Übergang einfangen
Um zu verstehen, was zwischen den frühen und späten Phasen passiert, konzentrierten sich die Forschenden auf eine „Übergangsperiode“ mehrere Stunden nach der Verletzung. Sie trainierten einen Computerklassifikator mit den detaillierten Bewegungs- und Formmerkmalen eindeutig früher (M1-ähnlicher) und später (M2-ähnlicher) Makrophagen und nutzten ihn dann, um Zellen, die während dieses mittleren Zeitfensters aufgezeichnet wurden, als „klassifizierte M1-ähnlich“ (cM1-ähnlich) oder „klassifizierte M2-ähnlich“ (cM2-ähnlich) zu kennzeichnen. Durch die Gruppierung der Daten in 20-Minuten-Scheiben konnten sie verfolgen, wie sich zentrale Merkmale zeitlich veränderten. Etwa 7,5 bis 9 Stunden nach der Verletzung begannen Zellen mit M2-ähnlichem Verhalten, ihre gerichtete Bewegung zur Wunde hin zu verlieren, zogen sich dann aktiv zurück, wurden dabei länglicher und beschleunigten kurzzeitig. Dieses Zeitfenster markiert wahrscheinlich den Zeitpunkt, an dem viele Makrophagen von entzündungsaktiven Kämpfern zu Reparaturunterstützern wechseln.
Makrophagen ohne klaren Alarm
Die Studie untersuchte außerdem zwei weitere Gruppen: Zellen, die in der Nähe einer Wunde kein zentrales entzündungsförderndes Signal (TNF) aktivierten, und Makrophagen in völlig unverletzten Fischen. Die nicht-TNF-exprimierenden Zellen nahe einer Verletzung sahen aus und bewegten sich eher wie frühe M1-ähnliche Zellen, blieben jedoch weiter von der Wunde entfernt und verlangsamten sich im Zeitverlauf, was darauf hindeutet, dass starke entzündliche Aktivierung mit physischer Nähe zum beschädigten Gewebe verknüpft ist. In unverletzten Fischen drifteten Makrophagen langsam ohne ausgeprägte Richtung, oft auf gekrümmten, zufälligen Pfaden. Ihre Formen waren runder und ihre Geschwindigkeiten niedriger als in jedem verletzten Zustand, was einen ruhigen, patrouillierenden Modus statt einer Notfallreaktion widerspiegelt.
Was das für die Heilung bedeutet
Indem Filme lebender Immunzellen in Zahlen übersetzt werden, kartiert diese Arbeit eine „Verhaltenslandschaft“ für Makrophagen, während eine Wunde von früher Entzündung zur Auflösung übergeht. Sie zeigt, dass Aussehen und Bewegung dieser Zellen eng mit ihrer Funktion verknüpft sind — ob sie geradewegs zur Wunde eilen, in Schleifen Gewebe umgestalten oder leise in gesundem Gewebe umherwandern. Solche quantitativen Fingerabdrücke könnten Forschenden helfen, zu erkennen, wann die Heilung aus dem Gleichgewicht gerät, Therapien zu entwickeln, die Makrophagen in hilfreiche Modi lenken, und entzündliche Erkrankungen besser zu verstehen, bei denen dieses Gleichgewicht gestört ist.
Zitation: Park, S.A., Lupi, G., Ozbilgic, R. et al. The morpho-kinetic landscape of macrophage modes during wound healing in zebrafish. Sci Rep 16, 6506 (2026). https://doi.org/10.1038/s41598-026-36624-w
Schlüsselwörter: Wundheilung, Makrophagen, Zebrafisch, Zellmigration, Entzündung