Clear Sky Science · de
Kombinierte Wirkungen von Nitrat und antimikrobiellen Verbindungen auf in vitro subgingivale Biofilme
Warum Ihr Zahnfleisch und Darmmedizin verbunden sind
Blutendes Zahnfleisch und Parodontitis werden meist „schlechten“ Bakterien zugeschrieben. Um sie zu bekämpfen, greifen Zahnärzte oft zu starken Mundspülungen und Antibiotika. Diese Studie stellt eine größere Frage: Was, wenn einige dieser Behandlungen heimlich die hilfreichen Bakterien schädigen, die wir brauchen, während ein einfache Nährstoff, der in Blattgemüse vorkommt, die Mundmikroben tatsächlich in Richtung Gesundheit schubsen kann?
Zahnfleischerkrankung als Gemeinschaftsproblem
Parodontitis ist eine langanhaltende Infektion rund um die Zähne, die das Gewebe zerstört, das sie an ihrem Platz hält, und mit Herzkrankheiten, Diabetes und sogar Erkrankungen des Gehirns in Verbindung gebracht wird. Anstatt von einem einzelnen Keim verursacht zu werden, entsteht sie, wenn sich die gesamte Gemeinschaft der Mundbakterien in einen schädlichen Zustand verschiebt, genannt Dysbiose. Die moderne Behandlung setzt nach wie vor stark auf breit wirkende Mittel: Antibiotika wie Amoxicillin und Metronidazol sowie antiseptische Spülungen wie Chlorhexidin. Diese Produkte können Problemkeime abtöten – sie können aber auch freundliche Bakterien auslöschen und möglicherweise die Entwicklung von Resistenzen fördern.
Ein genauerer Blick auf Biofilme aus echten Patienten
Um zu sehen, was diese Behandlungen tatsächlich mit Zahnfleischbakterien anstellen, sammelten die Forschenden Plaque aus tiefen Taschen um die Zähne von 12 Personen mit Parodontitis. Im Labor züchteten sie diese Proben als dünne Bakterienschichten, sogenannte Biofilme, über acht Stunden unter acht verschiedenen Bedingungen: keine Behandlung, nur Nitrat, jedes Medikament allein und jedes Medikament kombiniert mit Nitrat. Nitrat, eine natürliche Verbindung, die in Spinat, Salat und Rote Bete reichlich vorkommt, kann von bestimmten Mundbakterien in Stickstoffmonoxid umgewandelt werden, ein Gas, das Blutgefäße entspannt und das Wachstum krankheitsassoziierter Mikroben verlangsamen kann. Das Team maß, wie viel Biofilm entstand, wie gut er Nitrat umwandelte und welche Bakterienarten unter jeder Behandlung gediehen.
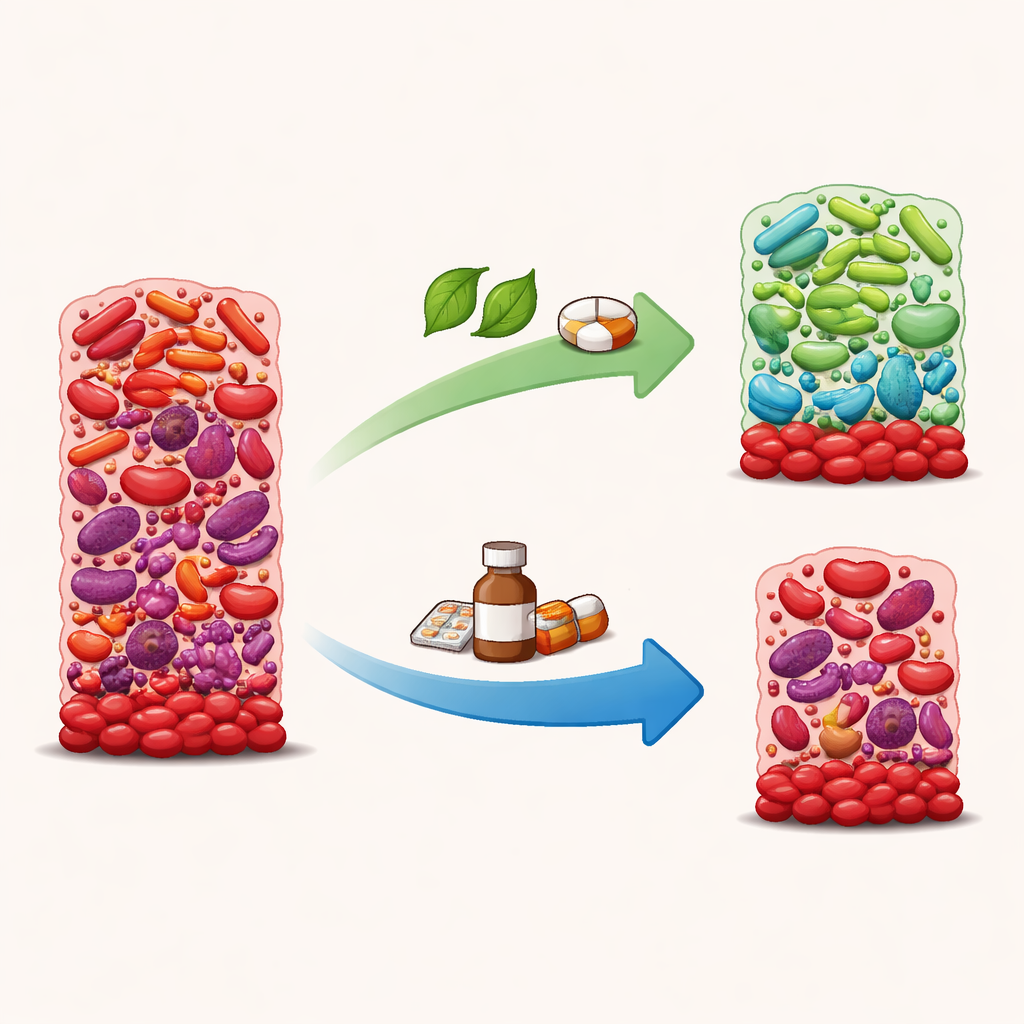
Wirkstoffe, die das Wachstum verringern, aber das Gleichgewicht verschlechtern können
Niedrige Dosen von Chlorhexidin und Amoxicillin halbierten etwa das Biofilmwachstum und reduzierten stark die Fähigkeit der Bakterien, Nitrat zu verarbeiten. Das war aber kein selektives „gutes Aufräumen“. DNA‑Sequenzierung zeigte, dass unter diesen Bedingungen gesundheitsassoziierte Bakterien wie Rothia, Gemella und Kingella tendenziell abnahmen, während mehrere mit Zahnfleischerkrankungen verbundene Arten – darunter Fusobacterium, Treponema und Eubacterium – entweder gleich blieben oder prominenter wurden. Ein Index, der bewertet, wie „krankhaft“ eine Gemeinschaft mikroskopisch erscheint, war bei Chlorhexidin und Amoxicillin höher als bei Nitrat, was darauf hindeutet, dass diese Mittel den Biofilm trotz Wachstumsunterdrückung in einen schädlicheren, unausgewogeneren Zustand treiben können.
Blattgrünes Brennstoff und ein sanfteres Antibiotikum
Nitrat erzählte eine andere Geschichte. Wenn Plaque nur mit Nitrat gezüchtet wurde, nahmen Bakterien zu, die darauf spezialisiert sind, Nitrat in nützliche Produkte umzuwandeln, wie Neisseria und einige Aggregatibacter‑Arten. Der Dysbiose‑Score sank im Vergleich zu Chlorhexidin‑ oder Amoxicillin‑Bedingungen und deutete auf eine gesündere Gemeinschaft hin. Metronidazol, in einer Konzentration ähnlich derer, die tatsächlich in Zahnfleischtaschen von Patienten ankommt, reduzierte allein weder deutlich das Wachstum noch die Nitratnutzung. In Kombination mit Nitrat schien es jedoch das Gleichgewicht auf eine hilfreiche Weise zu kippen: Krankheitsassoziierte Arten wie Fusobacterium und Treponema nahmen ab, während Nitrat nutzende Neisseria und Kingella zunahmen. Diese Kombination schien die schlimmsten Übeltäter zurückzuschneiden, ohne wichtige Funktionen zu entfernen.
Was das für die tägliche Pflege bedeutet
Für Menschen mit Parodontitis deuten diese Ergebnisse darauf hin, dass „stärker“ nicht immer „besser“ ist, wenn es um antimikrobielle Maßnahmen geht. In diesem Labormodell verlangsamten niedrig dosierte Chlorhexidin‑ und Amoxicillinbehandlungen das Bakterienwachstum, schwächten aber gleichzeitig einen natürlichen, nitratbasierten Weg, der sowohl die Mund‑ als auch die Ganzkörpergesundheit unterstützt, und sie standen im Zusammenhang mit eher krankheitsähnlichen mikrobiellen Mustern. Nitrat, besonders in Kombination mit Metronidazol, begünstigte Bakterien, die mit gesünderem Zahnfleisch verbunden sind, und erhielt die Nitratstoffwechselaktivität. Obwohl echte Münder komplexer sind als Laborgefäße, stützt diese Arbeit die Idee schonender, mikrobiomfreundlicher Strategien – etwa nitratreiche Ernährung und sorgfältig ausgewählte Antibiotika –, um Parodontitis zu behandeln, ohne die Bakterien zu untergraben, die uns helfen, gesund zu bleiben.
Zitation: Moran, S.P., Nadal-Ruiz, M., Mira, A. et al. Combined effects of nitrate and antimicrobial compounds on in vitro subgingival biofilms. Sci Rep 16, 6686 (2026). https://doi.org/10.1038/s41598-026-36588-x
Schlüsselwörter: Zahnfleischerkrankung, orale Mikrobiota, Nitrat, Mundspülung, Antibiotika