Clear Sky Science · de
Diagnose der Alzheimer-Krankheit mit hoher Genauigkeit durch Petri-Netz-Modellierung von Signalwegen
Warum die frühe Erkennung von Hirnerkrankungen uns alle betrifft
Die Alzheimer-Krankheit raubt langsam Gedächtnis und Selbstständigkeit, oft lange bevor klare Symptome sichtbar werden. Die heutigen Diagnosewerkzeuge wie Hirnscans und kognitive Tests sind häufig teuer, schwer zugänglich und in den frühesten Stadien nicht sehr sensitiv. Diese Studie stellt eine neue Methode vor, die das molekulare "Verdrahtungsbild" des Körpers anhand von Blut- oder Gewebeproben liest, mithilfe eines mathematischen Rahmens namens Petri-Netz. Das Ziel ist einfach, aber bedeutend: mit sehr hoher Genauigkeit zu entscheiden, ob das Genaktivitätsmuster einer Person eher dem eines gesunden Menschen oder dem eines Alzheimer-Patienten ähnelt — idealerweise früh genug, um den Krankheitsverlauf zu beeinflussen.
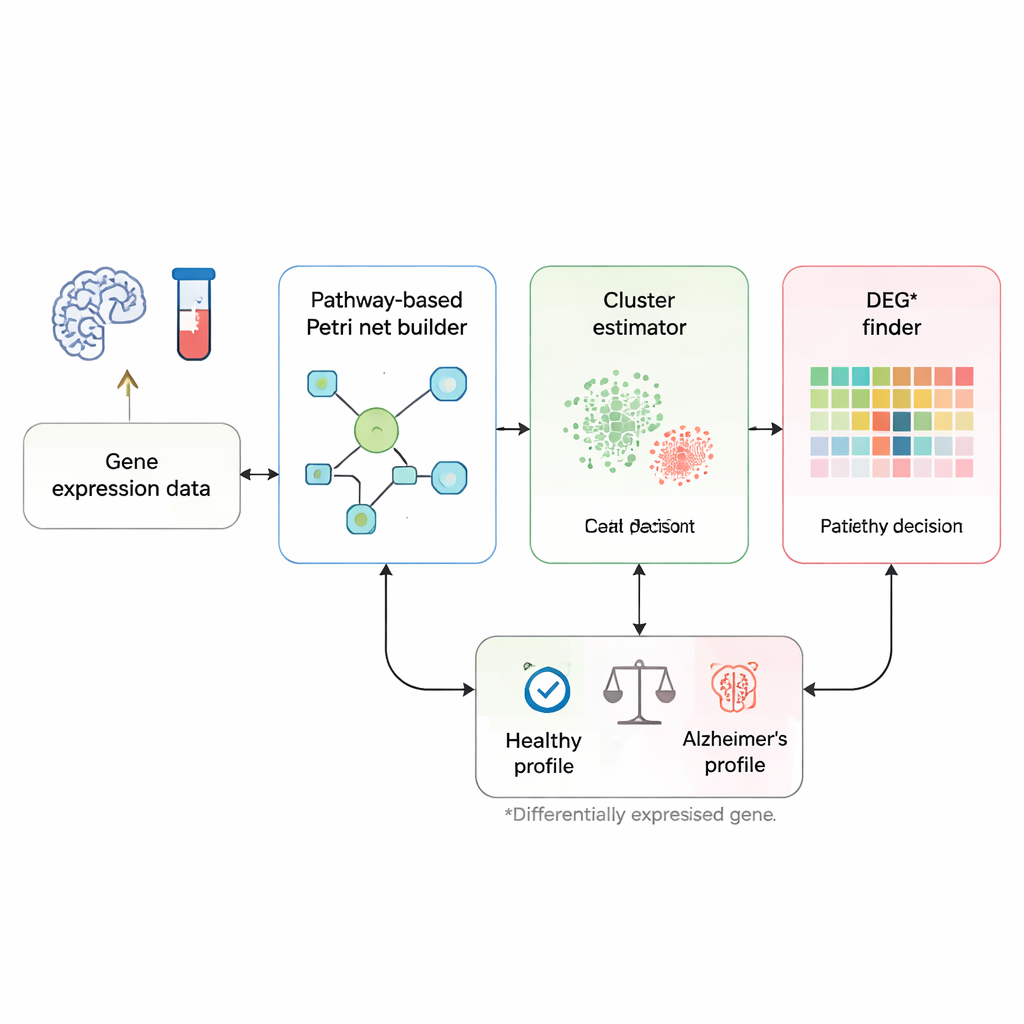
Die Krankheit in den "Schaltkreisen" der Signalübertragung lesen
Anstatt jedes Gen als isolierten Marker zu behandeln, richten die Forscher ihren Fokus darauf, wie Gene entlang bekannter biologischer Signalwege miteinander kommunizieren, die mit Alzheimer in Verbindung stehen. Sie beginnen mit einer kuratierten Pfadkarte aus der KEGG-Datenbank, die Gene und die aktivierenden oder hemmenden Beziehungen zwischen ihnen auflistet. Dieser Weg wird in ein Petri-Netz überführt — eine Art Flussdiagramm, in dem Kreise für Gene stehen, Rechtecke für Interaktionen und kleine Tokens für Signale, die durch das Netzwerk wandern. Wenn ein Token von einem Ende des Weges zu speziellen "Krankheits"-Knoten gelangt, steht das für eine Kette von Genereignissen, die zum Absterben von Nervenzellen und zur Demenz führen könnten.
Von einer Blutprobe zur Ja-oder-Nein-Antwort
Die Methode beginnt mit Genexpressionsprofilen: Messungen, die anzeigen, wie aktiv Tausende von Genen in Blut- oder Gewebeproben einer Person sind. Zunächst vergleicht ein maßgeschneiderter "Cluster-Schätzer" eine neue Probe mit zuvor beschrifteten gesunden und Patientenproben und konzentriert sich dabei auf Gene, von denen bereits bekannt ist, dass sie sich zwischen diesen Gruppen unterscheiden. Für jedes dieser Gene prüft das Werkzeug, welche Trainingsproben die ähnlichsten Expressionswerte aufweisen, und verwendet eine Art Nachbarschaftsentscheid, um der neuen Probe ein vorläufiges Label zu geben — wahrscheinlich gesund oder wahrscheinlich erkrankt. Dieser Schritt bildet zwei Arbeitsgruppen beziehungsweise Cluster von Proben: eines, das typische gesunde Muster repräsentiert, und eines, das typische Alzheimer-Muster darstellt.
Die aussagekräftigsten Gene für jede Person finden
Im nächsten Schritt wird es persönlicher. Für eine gegebene Person betrachtet die Methode Gen für Gen, wo deren Expressionswerte wirklich hervorstechen. Für jedes Gen wird der Wert dieser Person mit dem Bereich verglichen, der sowohl im gesunden Cluster als auch im Patientencluster beobachtet wurde, wobei robuste Statistik verwendet wird, die den Einfluss lauter Ausreißer abschwächt. Wenn der Expressionswert eines Gens klar innerhalb des "krankhaften" Bereichs und außerhalb des gesunden Bereichs liegt, wird es als DEG* markiert — ein für diese Person besonders aufschlussreiches Gen. Diese DEG*-Gene erhalten Initialtokens im Petri-Netz, die markieren, wo die abnormale Aktivität zuerst im Signalweg auftaucht.
Das Netzwerk ablaufen lassen bis zur Diagnose
Sobald die Tokens platziert sind, läuft das Petri-Netz Schritt für Schritt ab. In jedem Schritt "feuert" jede Interaktion, deren Eingangs-Gene genügend Tokens besitzen, und bewegt Tokens zu downstream gelegenen Genen, wobei Aktivierungs- und Hemmungsregeln beachtet werden. Dies setzt sich fort, bis keine weiteren Verschiebungen möglich sind. Erreicht am Ende mindestens ein Token den finalen Krankheitsknoten des Netzwerks — der Prozesse wie Neuronenverlust oder Neurodegeneration repräsentiert —, wird die Probe als Alzheimer klassifiziert; andernfalls gilt sie als gesund. Weil jeder Feuerschritt protokolliert wird, können Forschende einen klaren Pfad von der ungewöhnlichen Genaktivität einer Person bis zum gesunden oder kranken Ergebnis zurückverfolgen, anstatt sich auf eine undurchsichtige statistische Kennzahl zu verlassen.
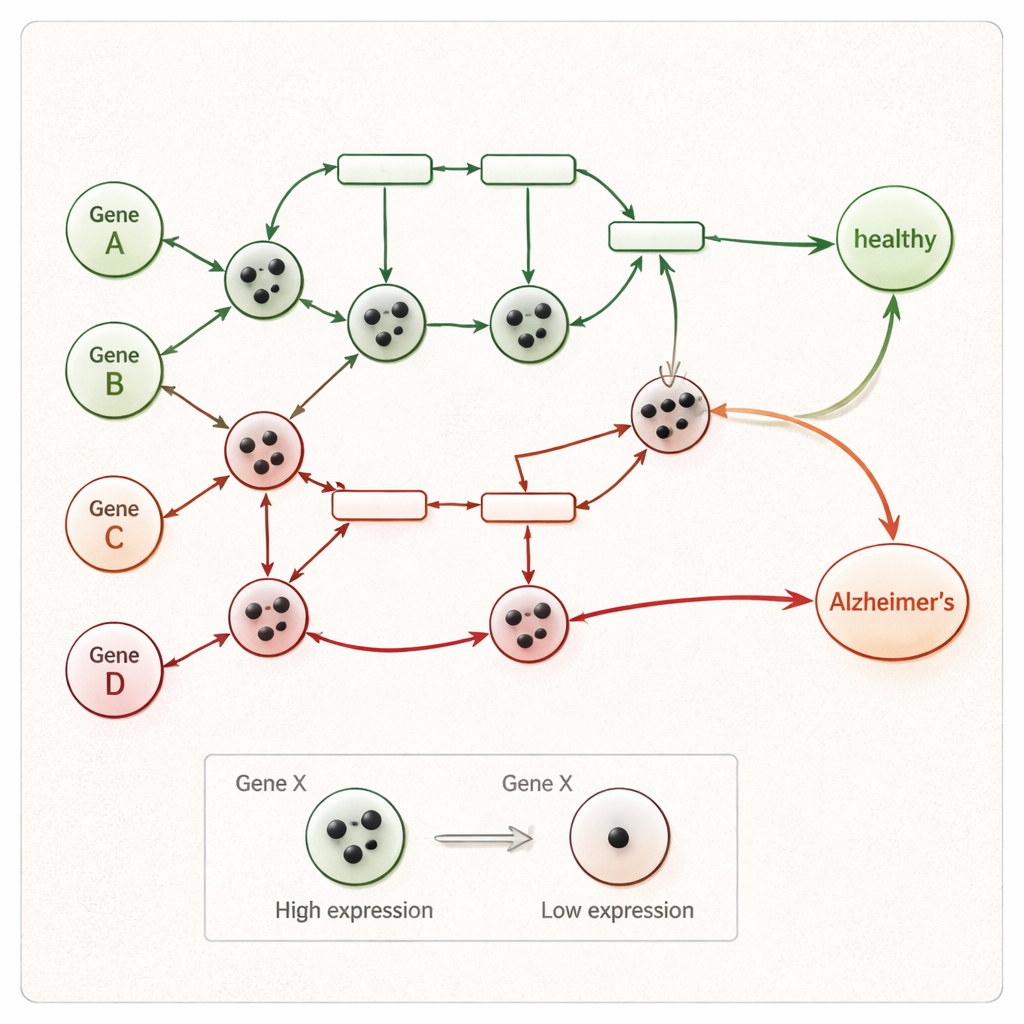
Wie genau ist dieser Ansatz in der Praxis?
Das Team testete sein Framework an mehreren großen, öffentlich verfügbaren Genexpressionsdatensätzen aus Blut- und Hirngewebe. In zwei weit verbreiteten Blutdatensätzen unterschied ihre Methode Alzheimer-Patienten in etwa 98–99 % der Fälle korrekt von gesunden Personen und übertraf damit frühere maschinelle Lernverfahren, die oft nur 65–81 % Genauigkeit erreichten. Sie zeigten zudem starke Leistungen in weiteren Hirn- und Blutdatensätzen, selbst wenn die Fallzahlen klein waren. Wichtig ist, dass ihre Methode — anders als viele Konkurrenten — keine verrauschten oder schwer zu interpretierenden Proben ausschloss; stattdessen nutzt sie ihr internes Design, um Variabilität zu handhaben und alle Daten in die Analyse einzubeziehen.
Was das für künftige Alzheimer-Tests bedeutet
Für Laien lautet die Hauptaussage: Die Studie verwandelt komplexe Genetik und Pfaddiagramme in einen klaren, schrittweisen Entscheidungsprozess, der frühe Anzeichen der Alzheimer-Krankheit aus einer einfachen Probe, potenziell nur Blut, lesen kann. Indem modelliert wird, wie abnorme Gene zusammenwirken und nicht nur, wie sie sich einzeln verhalten, liefert das Petri-Netz-Framework sowohl hohe diagnostische Genauigkeit als auch eine verständliche "Geschichte" darüber, wie sich die Krankheit bei jeder Person entwickeln könnte. Obwohl diese Arbeit noch Forschungscharakter hat und noch kein klinischer Test ist, weist sie auf künftige Werkzeuge hin, die Alzheimer früher erkennen, Therapieentscheidungen leiten und schließlich auf andere Hirnerkrankungen und Krebserkrankungen mit demselben Grundprinzip übertragen werden könnten.
Zitation: Ebrahimian, H., Asadzadeh, F., Rahgozar, M. et al. Diagnosis of Alzheimer’s disease with high accuracy via Petri net modeling of signaling pathways. Sci Rep 16, 6457 (2026). https://doi.org/10.1038/s41598-026-36585-0
Schlüsselwörter: Alzheimer-Diagnose, Genexpressionsdaten, Signalwege, Petri-Netz-Modellierung, Blut-Biomarker