Clear Sky Science · de
Konstruktion und erste Validierung eines Schlüssel-Gen-Netzwerks für Progesteronresistenz beim Endometriumkarzinom basierend auf genomweiter CRISPR-Screening
Warum manche Gebärmutterkrebserkrankungen nicht mehr auf Hormone hören
Für viele Menschen mit frühem Endometriumkarzinom (Gebärmutterschleimhaut), die noch Kinder bekommen möchten, können Hormonpräparate, die das natürliche Progesteron nachahmen, Tumoren verkleinern und die Gebärmutter erhalten. Dennoch sprechen bis zu einem Drittel dieser Tumoren entweder nie an oder werden schnell resistent, sodass Patientinnen operativen Eingriffen oder aggressiveren Behandlungen zugeführt werden müssen. Diese Studie nutzt ein mächtiges Geneditierwerkzeug, um zu kartieren, welche Gene dazu führen, dass Endometriumkrebszellen Progesteron ignorieren, und weist damit den Weg zu künftigen Tests und Medikamenten, die diese Therapie länger wirksam halten könnten.
Mit Gen-Scheren das gesamte Genom durchsuchen
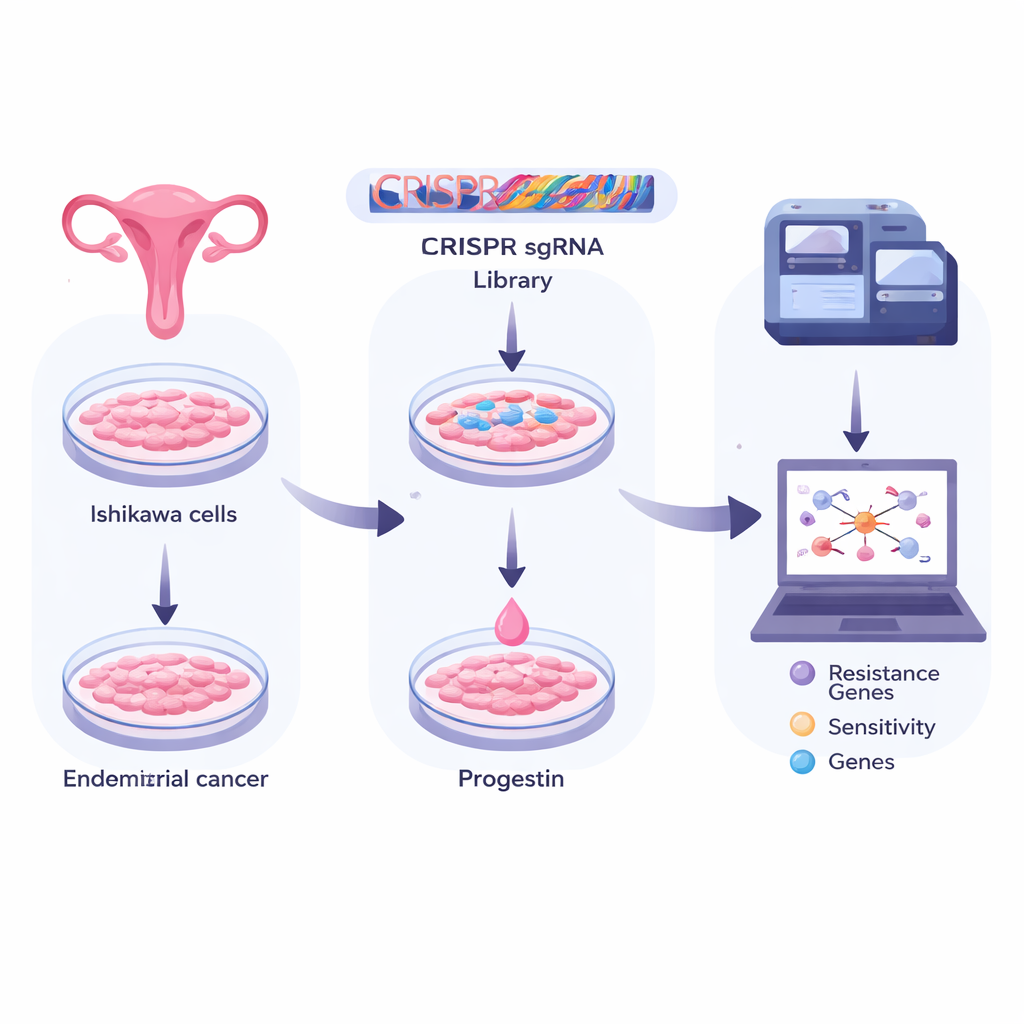
Die Forscher arbeiteten mit Ishikawa-Zellen, einem weit verbreiteten Modell für Endometriumkarzinom. Sie infizierten Millionen dieser Zellen mit einer Bibliothek von CRISPR-„Gen-Scheren“, von denen jede dafür programmiert war, ein anderes menschliches Gen auszuschalten. So entstand ein großes Pool, in dem prinzipiell jede Zelle ein einzigartig deaktiviertes Gen trug. Das Team teilte die Zellen dann in Gruppen auf: eine wurde als Ausgangsbaseline eingefroren, eine andere erhielt nur ein unschädliches Lösungsmittel, und eine weitere wurde über viele Tage mit einem gängigen synthetischen Progesteron (Medroxyprogesteron, MPA) behandelt. Durch tiefes Sequenzieren der CRISPR-Marker, die in jeder Gruppe überlebten, konnten sie erkennen, welche Gen-Knockouts den Zellen halfen, unter Progesteronbehandlung zu überleben oder zu sterben.
Gene ausfinden, die die Medikamentenwirkung fördern oder behindern
Die Analyse dieser Datenflut erforderte ausgefeilte Statistik. Das Team verwendete zwei komplementäre Methoden, RRA und MLE, um Gene danach zu ordnen, wie stark sie Zellen vor Progesteron schützten (Resistenzgene) oder Zellen anfälliger für das Absterben machten (Sensitivitätsgene). Sie fanden Hunderte von Kandidaten in beide Richtungen. Viele dieser Gene gruppierten sich in Signalwegen, die sich mit DNA-Kopie und -Reparatur, der Herstellung und Verarbeitung von RNA sowie allgemeinem Zellstoffwechsel befassen. Anders gesagt: Die grundlegenden Mechanismen, die Zellen ermöglichen, ihre genetischen Informationen zu lesen, zu erhalten und darauf zu reagieren, scheinen eng damit verknüpft zu sein, ob Endometriumkrebszellen dem „Wachstum stoppen“-Signal von Progesteron folgen.
Die Liste auf die wichtigsten Akteure eingrenzen
Um falschen Hinweisen vorzubeugen, verglichen die Wissenschaftler die CRISPR-Treffer mit einem älteren Datensatz aus ihrem Labor, in dem sie gewöhnliche Krebszellen mit einer Linien verglichen hatten, die im Laufe der Zeit Progesteronresistenz entwickelt hatte. Indem sie nach Genen suchten, die in beiden Screenings auftauchten und konsistente Veränderungen zeigten, reduzierten sie die Liste auf fünf Gene, die offenbar Resistenz fördern, und zwanzig, die ihr entgegenwirken. Öffentliche Krebsdatenbanken zeigten, dass viele der Resistenz-unterdrückenden Gene in der häufigsten Form des Endometriumkarzinoms stärker aktiv sind, während mehrere Resistenz-fördernde Gene mit schlechteren Patientenergebnissen korrelieren, was darauf hindeutet, dass diese Signale in echten Tumoren und nicht nur in Zellkulturen relevant sind.
Wichtige Gene in Zellen und in Mäusen testen
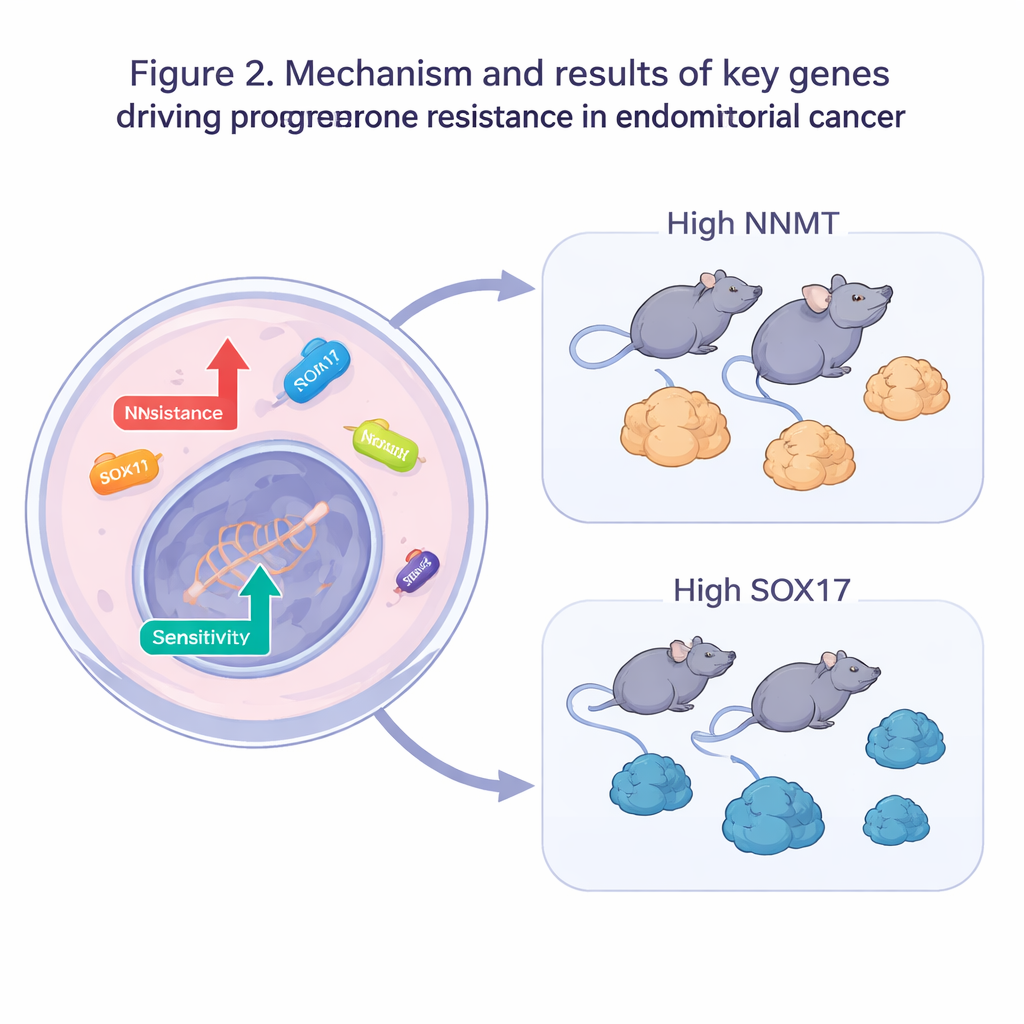
Das Team wechselte dann von Big Data zu experimentellen Prüfungen. In progesteronresistenten Zellen schalteten sie jeweils eines der fünf verdächtigten Resistenzgene aus oder verstärkten die Expression der fünf vermuteten Sensitivitätsgene. Bei Exposition gegenüber Progesteron starben viele dieser veränderten Zellen häufiger, und deutlich geringere Wirkstoffdosen reichten aus, um das Wachstum zu bremsen — ein Hinweis darauf, dass die Modulation einzelner Gene die Hormonempfindlichkeit wiederherstellen kann. Zwei Gene stachen hervor: NNMT, das am Zellstoffwechsel beteiligt ist, und SOX17, ein Gen, das die Entwicklung und das Verhalten von Zellen steuert. In Maus-Tumormodellen machte eine Erhöhung von NNMT die Tumoren weniger empfänglich für Progesteron, während eine Steigerung von SOX17 resistente Tumoren unter derselben Behandlung stärker schrumpfen ließ.
Was diese Ergebnisse für Patientinnen bedeuten könnten
Kurz gesagt stellt die Studie ein frühes „Schaltbild“ dafür zusammen, wie Endometriumkrebszellen entscheiden, ob sie auf Progesteron hören. Sie legt nahe, dass Resistenz nicht nur durch den Verlust des Progesteronrezeptors entsteht, sondern auch durch tiefgreifendere Veränderungen in der DNA- und RNA-Handhabung sowie durch Schlüsselregulatoren wie NNMT und SOX17. Künftig könnten Blut- oder Gewebetests, die dieses Gen-Netzwerk erfassen, Ärzten helfen vorherzusagen, wer von einer hormonbasierten, gebärmuttererhaltenden Therapie profitiert. Noch vielversprechender ist, dass Medikamente, die Resistenzgene dämpfen oder Sensitivitätsgene stärken, eines Tages mit Progesteron kombiniert werden könnten, um diese schonende Behandlungsoption für mehr Menschen länger wirksam zu machen.
Zitation: Li, X., Wang, S., Qiu, Z. et al. Construction and initial validation of key gene network for progesterone resistance in endometrial cancer based on genome-wide CRISPR screening. Sci Rep 16, 8030 (2026). https://doi.org/10.1038/s41598-026-36534-x
Schlüsselwörter: Endometriumkarzinom, Progesteronresistenz, CRISPR-Screening, Gen-Netzwerke, Hormontherapie