Clear Sky Science · de
Nachhaltige Herstellung von Batteriequalität-Nickel durch Wasserstoffreduktion von Saprolith
Den Nickel hinter Elektroautos sauberer machen
Nickel ist ein unscheinbarer Arbeitspferd der modernen Technik, vor allem in den leistungsstarken Batterien von Elektrofahrzeugen. Die Produktion dieses Metalls ist jedoch überraschend umweltschädlich und verursacht große Mengen Kohlendioxid. Diese Studie untersucht eine Möglichkeit, „Batteriequalität“-Nickel mit deutlich geringeren Emissionen herzustellen, indem Kohle in einem wichtigen Schmelzschritt durch Wasserstoffgas ersetzt wird — was den Klimafußabdruck der Elektromobilität erheblich verkleinern könnte.
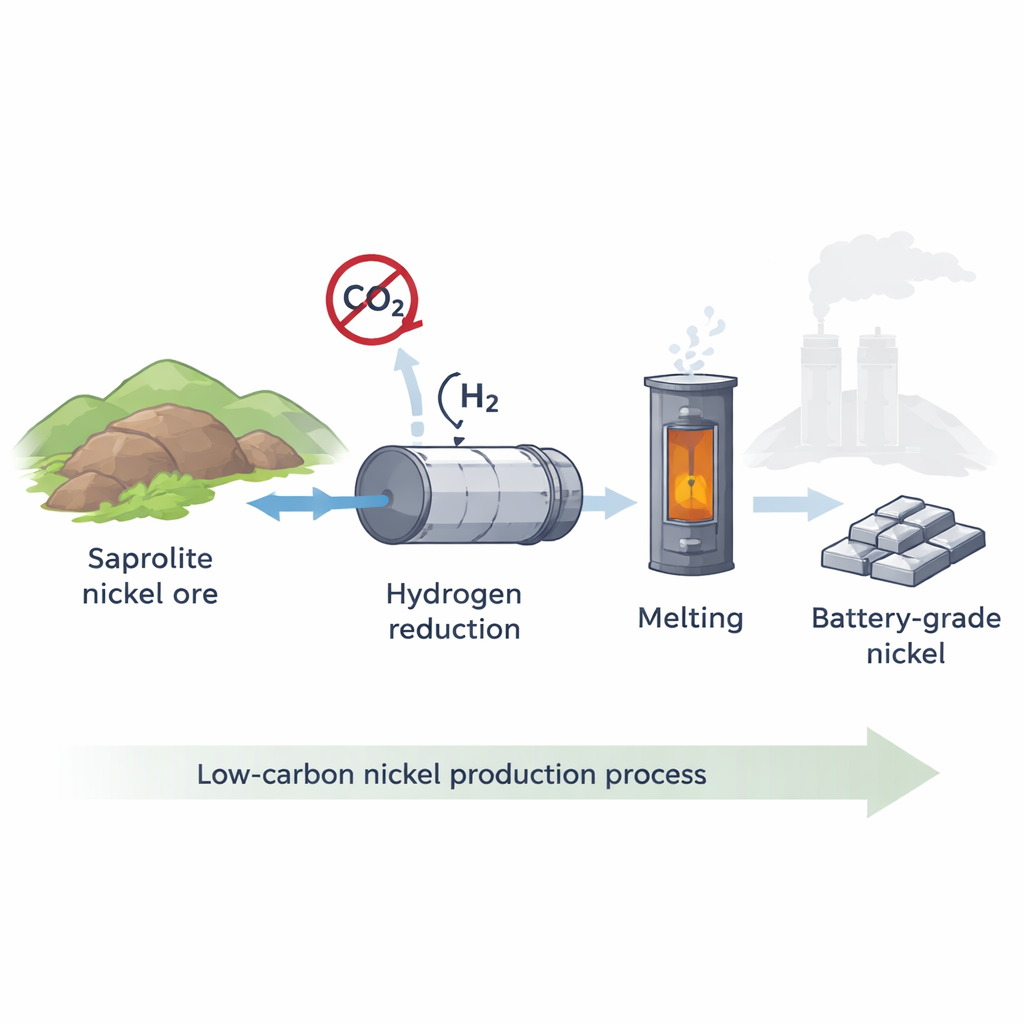
Warum diese Nickel-Erzart wichtig ist
Ein großer Teil des weltweiten Nickels stammt aus verwitterten tropischen Gesteinen, den sogenannten Lateriten. Eine verbreitete Sorte, Saprolith-Erz, ist reich an magnesiumhaltigen Silikatmineralen und enthält typischerweise mehr als 1,5 % Nickel. Heute wird nahezu sämtliches Saprolith durch ein Hochtemperaturverfahren behandelt, das als Rotary Kiln–Electric Furnace (RKEF) bekannt ist und Kohle sowohl als Brennstoff als auch als chemisches Reduktionsmittel verbrennt. Abhängig von den Bedingungen kann dies etwa 30 bis mehr als 60 Tonnen Kohlendioxid pro Tonne produziertem Nickel ausstoßen. Alternativen wie aggressive Säurelaugung sind oft sogar noch kohlenstoffintensiver. Während die Nachfrage nach Nickel mit dem Wachstum der Elektrofahrzeugflotte steigt und die Umweltauflagen verschärft werden, wächst der Druck, sauberere Schmelztechnologien zu finden.
Wasserstoff statt Kohle verwenden
Die Forschenden konzentrierten sich auf eine vielversprechende Alternative: Wasserstoffgas anstelle von Kohle zu verwenden, um Sauerstoff aus den nickel- und eisenhaltigen Mineralen im Saprolith zu entfernen. Sie bauten einen einen Meter langen rotierenden Stahlreaktor, der die Bewegung und den Gas-Feststoff-Kontakt eines industriellen Rundofens nachahmt. Fein zerkleinertes Saprolith aus Neukaledonien wurde in diese Kammer eingeführt, die zunächst unter Stickstoff aufgeheizt und dann einem kontrollierten Strom aus nahezu reinem Wasserstoff bei Temperaturen zwischen 800 und 950 °C ausgesetzt wurde. Durch sorgfältiges Verfolgen von Massenverlust und Veränderungen in der Mineralstruktur konnten sie beobachten, wie schnell und wie vollständig das Erz unter verschiedenen Betriebsbedingungen reduziert wurde, etwa bei unterschiedlichen Temperaturen, Gasströmen und Korngrößen.
Warum Korngröße der verborgene Hebel ist
Detaillierte mineralogische und chemische Analysen zeigten, dass grobe Partikel reicher an Magnesiumsilikaten sind, während feine Partikel anteilig mehr Eisenminerale enthalten; das Nickel selbst verteilt sich jedoch nahezu gleichmäßig über alle Korngrößen. Das bedeutet, dass eine physikalische Trennung der nickelhaltigen Minerale nicht praktikabel ist: Das gesamte Erz muss zusammen behandelt werden. Während der Wasserstoffbehandlung bei 900 °C verloren die Proben schnell etwa 20 % ihrer Masse — ein kombiniertes Signal von Wasserfreisetzung aus aufgeheizten Mineralen und Sauerstoffentzug bei der Metallbildung. Auffällig war, dass dieser Massenverlust innerhalb nur 15 Minuten seinen Endwert erreichte und sich bei längeren Zeiten kaum änderte. Stattdessen dominierten zwei physikalische Faktoren die Leistung: Gasfluss und Korngröße. Sobald der Wasserstofffluss etwa 3 Liter pro Minute überschritt, brachte mehr Gas keinen zusätzlichen Nutzen. Im Gegensatz dazu brachte eine feinere Zerkleinerung des Erzes einen deutlichen Vorteil: Die kleinsten Partikel, unter 45 Mikrometern, erzielten die höchste und schnellste Reduktion, weil Wasserstoff leichter durch das dünne Silikatrohrwerk diffundieren konnte, um die im Inneren eingeschlossenen Nickel- und Eisenatome zu erreichen.
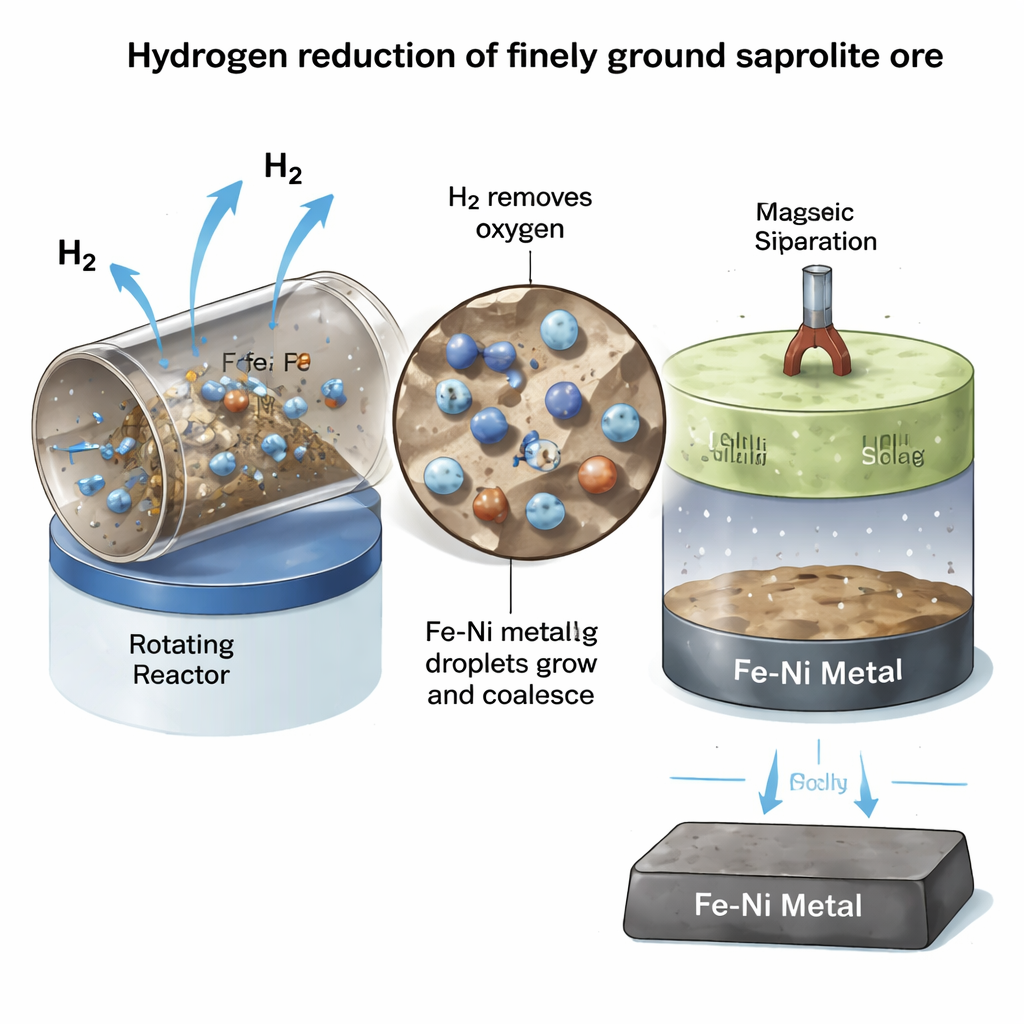
Vom reduzierten Erz zum Nickel in Batteriequalität
Um zu prüfen, ob dieses wasserstoffbehandelte Erz ein brauchbares Produkt liefern kann, schmolz das Team das reduzierte Pulver in einem hochtemperierten Vertikalschmelzofen unter inerten Argonatmosphäre. Bei 1550 °C separierte das Material sauber in zwei Schichten: eine dichte Eisen‑Nickel‑Legierung, die nach unten sank, und eine leichtere, magnesiumreiche Silikatschlacke, die obenauf schwamm. Mikroskopische Aufnahmen und chemische Kartierungen bestätigten, dass die Metallschicht etwa 73 % Eisen und 25 % Nickel enthielt — typisch für industrielles Nickelpig‑Eisen — während die Schlacke weitgehend metallfrei war. Da die Legierung stark magnetisch ist, konnte sie vollständig mit einfacher Magnettechnik separiert werden, was auf einen effizienten Weg vom Erz zum ofenfertigen Einsatzstoff ohne zusätzliche Chemikalien oder feste Reduktionsmittel hinweist.
Was das für sauberere Batterien bedeutet
Für Nichtfachleute lautet die wichtigste Botschaft: Die Art und Weise, wie wir Nickel verarbeiten, lässt sich deutlich sauberer gestalten, ohne die abgebauten Erztypen zu verändern. Durch feines Mahlen von Saprolith und das Aussetzen an einen kräftigen Wasserstoffstrom bei rund 900 °C kann das Erz in Minuten in ein Material verwandelt werden, das zu hochwertigem Nickelpig‑Eisen verschmilzt, mit einer klaren Trennung zwischen Metall und Gesteinsabfall. Weil Wasserstoff bei der chemischen „Entbindung“ Wasser statt Kohlendioxid erzeugt, könnte dieser Ansatz die Emissionen der Nickelschmelze erheblich reduzieren, sofern der Wasserstoff aus kohlenstoffarmer Energie stammt. Die Studie legt das Betriebsfenster — Temperatur, Gasfluss und Korngröße — dar, das Ingenieure zur Auslegung kohlenstoffarmer Anlagen nutzen können, und weist auf den nächsten Schritt hin: die Erprobung dieses wasserstoffbasierten Verfahrens in kontinuierlichen Pilotöfen, um zu beweisen, dass grüneres Nickel zuverlässig und im Maßstab hergestellt werden kann.
Zitation: Park, T., Han, S., Lee, W. et al. Sustainable production of battery-grade nickel via hydrogen reduction of saprolite. Sci Rep 16, 5553 (2026). https://doi.org/10.1038/s41598-026-36516-z
Schlüsselwörter: Nickelbatterien, Wasserstoffschmelzen, kohlenstoffarme Metalle, Laterit-Erz, Materialien für Elektrofahrzeuge