Clear Sky Science · de
Therapeutische Wirksamkeit und zugrundeliegender Mechanismus von Deinoxanthin in experimentellen Tier‑ und Zellmodellen der Parodontitis
Warum der Schutz Ihres Zahnfleisches wichtig ist
Blutendes Zahnfleisch und lockere Zähne mögen wie kleine Ärgernisse erscheinen, doch die chronische Zahnfleischerkrankung Parodontitis kann still und leise den Knochen abbauen, der die Zähne hält, und möglicherweise sogar die Gesundheit des gesamten Körpers beeinflussen. Diese Studie untersucht ein natürlich vorkommendes antioxidatives Pigment namens Deinoxanthin, das von einem ungewöhnlich widerstandsfähigen Bakterium produziert wird, um zu prüfen, ob es Zahnfleisch und Kieferknochen vor Schäden in experimentellen Modellen schwerer Zahnfleischerkrankung schützen kann.
Ein kraftvolles farbiges Molekül
Deinoxanthin ist ein leuchtend gelb‑orangefarbenes Carotinoidpigment, das vom strahlenresistenten Mikroorganismus Deinococcus radiodurans produziert wird. Carotinoide gehören zur gleichen Stoffgruppe, die Karotten und manchen Früchten ihre Farbe verleiht; viele wirken als starke Antioxidantien und binden schädliche reaktive Sauerstoffspezies – instabile Moleküle, die Zellen verletzen können. Frühere Arbeiten zeigten, dass Deinoxanthin besonders wirksam bestimmte Sauerstoffradikale neutralisiert. Die Forschenden fragten sich, ob dieses besonders starke Antioxidans den doppelten Kräften, die die Parodontitis antreiben – unkontrollierte Entzündung und oxidativer Stress im Zahnhalteapparat – entgegenwirken kann.
Test von Deinoxanthin in erkranktem Zahnfleisch
Um eine fortgeschrittene menschliche Zahnfleischerkrankung nachzuahmen, lösten die Forschenden bei Ratten Parodontitis aus, indem sie winzige Ligaturen um einen Backenzahn banden, nachdem sie diese mit dem bekannten Zahnbakterium Porphyromonas gingivalis beschichtet hatten. Dieses Modell erzeugt Entzündung, bakterielles Überwachsen und Knochenverlust rund um den Zahn. Nach einer Woche erhielten einige Ratten täglich orale Dosen von Deinoxanthin für zwei Wochen, während andere nur das Trägeröl bekamen. Hochauflösende 3D‑Röntgenaufnahmen zeigten, dass unbehandelte erkrankte Tiere einen erheblichen Verlust an Stützsubstanz erlitten, während die mit Deinoxanthin behandelten Tiere deutlich mehr Knochenmineral und Knochenvolumen behielten, nahe dem Niveau gesunder Kontrollen. Die mikroskopische Untersuchung ergab, dass bei Deinoxanthin‑behandeltem Zahnfleisch weniger eindringende entzündliche Zellen vorhanden waren und die Abstände zwischen Zahnoberfläche und Knochenkamm kürzer waren – beides Zeichen für erhaltenes Gewebe.
Entzündung und Knochenabbau beruhigen
Die Forschenden fragten anschließend, warum Knochen und Weichgewebe unter Deinoxanthin besser abschnitten. Bluttests und Gewebefärbungen zeigten, dass ligaturindu zierte Parodontitis klassische Entzündungsbotenstoffe wie TNF‑α, IL‑1β und COX‑2 erhöhte, die stark mit Gewebeabbau und Schmerzen verknüpft sind. Deinoxanthin senkte diese Signale deutlich sowohl im Blutkreislauf als auch im Parodontalband, das den Zahn verankert. Im Kieferknochen selbst nahm die Krankheit Anzahl und Größe der knochenabbauenden Zellen (Osteoklasten) zu und steigerte Moleküle, die deren Bildung fördern, darunter RANKL und Cathepsin K. Deinoxanthin reduzierte diese knochenresorbierenden Zellen und deren Marker, während zugleich Proteine wiederhergestellt wurden, die mit neuem Knochenaufbau assoziiert sind – wie RUNX2, BMP2, Osterix, Osteocalcin und Osteopontin – und ein innerer Schutzweg (Nrf2/HO‑1) gestärkt wurde, der Zellen hilft, mit oxidativem Stress zurechtzukommen.
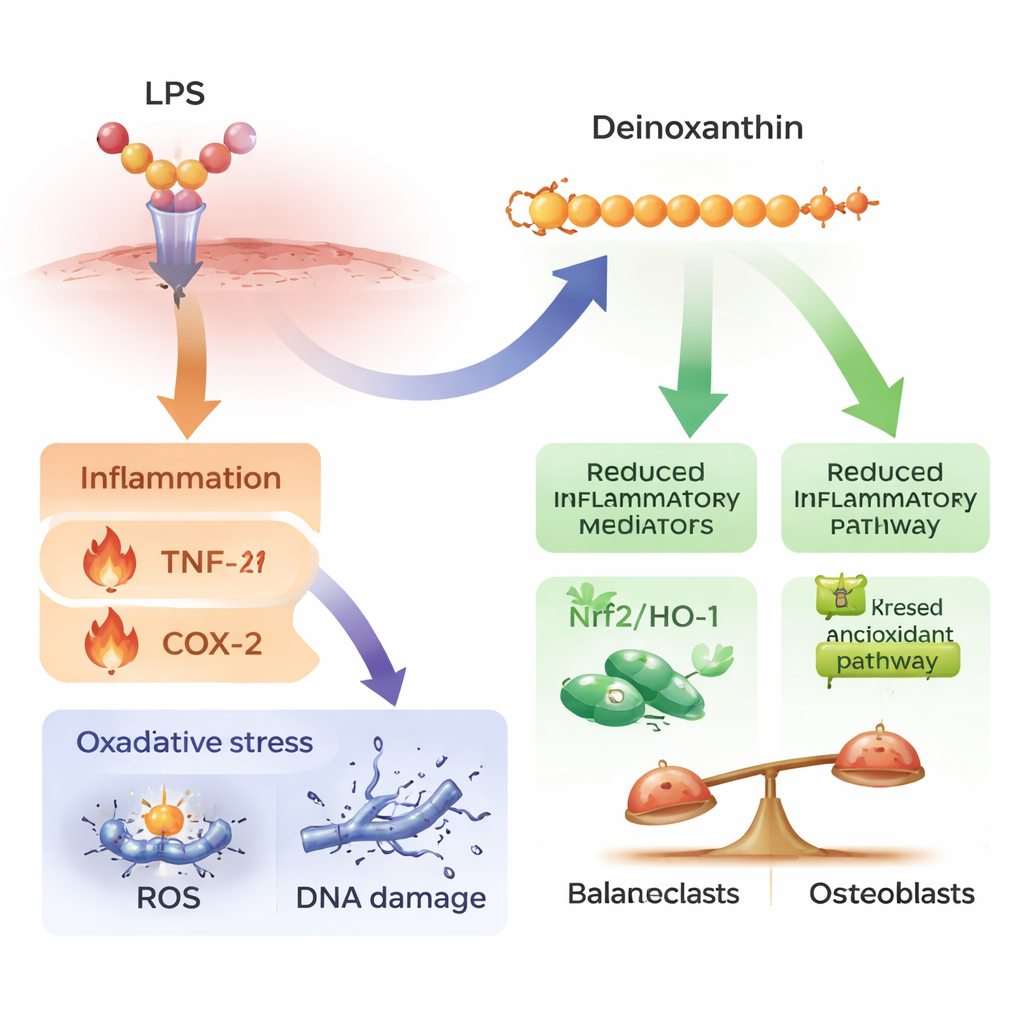
Zoom auf menschliche Zellen
Da Rattenstudien nicht vollständig erklären können, wie eine Verbindung beim Menschen wirken könnte, untersuchte das Team menschliche Parodontalbandzellen und eine menschliche Immunzelllinie im Labor. Sie setzten diese Zellen bakteriellen Komponenten aus, die normalerweise starke Entzündungsreaktionen und oxidativen Schaden auslösen. Unter diesem Stress produzierten die Zellen mehr entzündliche Faktoren, sammelten reaktive Sauerstoffspezies an, zeigten DNA‑Schäden und verloren teilweise ihre Fähigkeit zu wachsen, sich zu bewegen und Knochenbildung zu unterstützen. Die Zugabe einer niedrigen, nicht‑toxischen Dosis Deinoxanthin stellte das Zellwachstum wieder her, reduzierte oxidativen Stress und DNA‑Schäden und verbesserte die wundähnliche Heilung in Kultur. Außerdem verschob es die Genaktivität weg von Chemokinen und Zytokinen, die entzündliche Zellen anziehen und aktivieren, hin zu Programmen für Antioxidation und Gewebeerneuerung.
Vom Pigment zum potenziellen Therapieansatz
Insgesamt legt die Studie nahe, dass Deinoxanthin an mehreren Fronten wirken kann: Es dämpft zentrale Entzündungsmoleküle, verringert oxidativen Stress, bremst knochenzerstörende Zellen und unterstützt knochenbildende Zellen im Zahnfleischgewebe. Zwar stammen diese Befunde aus Tierversuchen und kultivierten menschlichen Zellen – und es bleibt viel zu tun, um Sicherheit, Dosierung und Wirksamkeit beim Menschen zu bestätigen – doch sie eröffnen die Möglichkeit, dass ein natürlich gewonnenes antioxidatives Pigment eines Tages die Standardbehandlung bei chronischer Parodontitis ergänzen könnte, um Patienten zu helfen, ihre Zähne und den sie stützenden Knochen besser zu erhalten.
Zitation: Bhattarai, G., An, YH., Shrestha, S.K. et al. Therapeutic potency and the related mechanism of deinoxanthin in experimental animal and cell models of periodontitis. Sci Rep 16, 5735 (2026). https://doi.org/10.1038/s41598-026-36514-1
Schlüsselwörter: Parodontitis, Deinoxanthin, Antioxidantien‑Therapie, Zahnfleischentzündung, Knochenabbau