Clear Sky Science · de
Wirtliche m6A-Modifikationen formen ein Mikrobiom, das zellenspezifische Ferroptose antreibt — ein kausaler Weg zu chronischen Atemwegserkrankungen
Warum Ihre Mikroben für Ihre Lungen wichtig sind
Chronische Atemwegsprobleme wie Asthma und chronisch obstruktive Lungenerkrankung (COPD) werden meist dem Rauchen, Umweltverschmutzung oder Allergien zugeschrieben. Diese Studie schlägt jedoch einen weniger offensichtlichen Akteur vor: die Billionen von Mikroben in unserem Darm und auf unserer Haut. Anhand groß angelegter genetischer Daten zeigen die Autorinnen und Autoren, dass bestimmte Mikroben Lungenerkrankungen nicht nur begleiten, sondern sie mithilfe subtiler chemischer Veränderungen in unseren Zellen und einer Form eisenabhängigen Zellschadens tatsächlich mitverursachen könnten. Das Verständnis dieses verborgenen Netzwerks könnte letztlich zu neuen Wegen führen, chronische Atemwegserkrankungen zu verhindern oder zu behandeln, indem man unsere Mikroben und deren molekulare Signalwege in gesündere Bahnen lenkt.
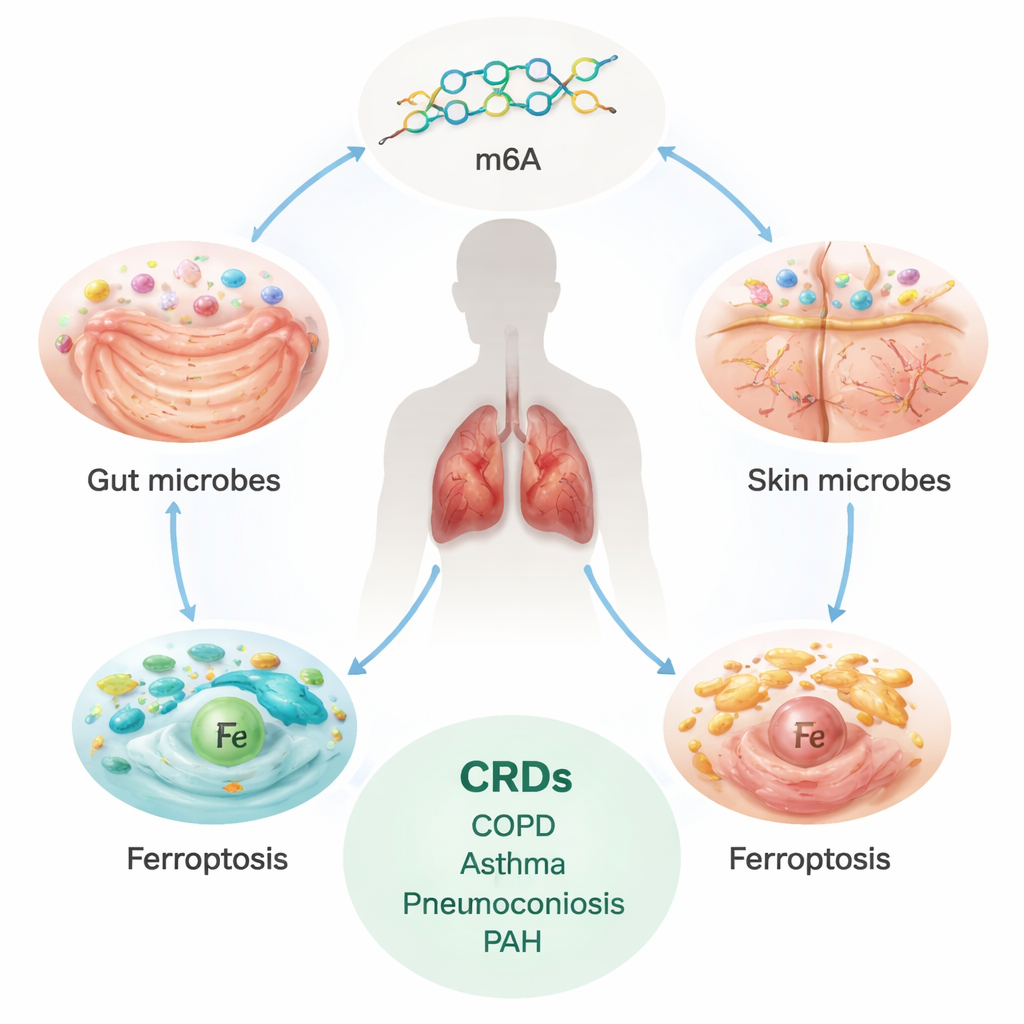
Die verborgene Last chronischer Lungenerkrankungen
Chronische Atemwegserkrankungen, darunter COPD, Asthma, interstitielle Lungenerkrankungen (ILD), Pneumokoniosen und pulmonale arterielle Hypertonie (PAH), betreffen weltweit Hunderte Millionen Menschen und verursachen jährlich Millionen von Todesfällen. Diese Erkrankungen schreiten oft langsam, aber unerbittlich voran, vernarben oder verändern Lungen und Blutgefäße und führen zu Atemnot. Die derzeitigen Therapien lindern hauptsächlich Symptome; sie stoppen oder kehren den zugrunde liegenden Schaden nicht vollständig um. Das treibt Forschende dazu, nach tiefer liegenden Ursachen zu suchen — insbesondere nach solchen, die sich vor dem Eintritt schwerer Erkrankung noch verändern lassen.
Mikrobielle Nachbarn im Darm und auf der Haut
Mittlerweile wissen wir, dass Darm und Haut komplexe mikrobielle Gemeinschaften beherbergen, die das Immunsystem trainieren, den Stoffwechsel formen und Barrierefunktionen erhalten. Aber treiben diese Mikroben tatsächlich Lungenerkrankungen voran, oder verändern sie sich nur, wenn Menschen krank werden? Um Ursache und Wirkung zu entwirren, nutzten die Forschenden eine Methode namens Mendelsche Randomisierung, die natürliche genetische Unterschiede zwischen Menschen als eine Art lebenslanges „Experiment“ verwendet. Sie kombinierten genetische Daten zu Hunderten von Darm- und Hautmikroben mit Daten zu fünf großen chronischen Lungenerkrankungen aus großen europäischen Studien und testeten, ob vererbte Neigungen zu höheren oder niedrigeren Mengen bestimmter Mikroben mit dem Risiko für jede Erkrankung verknüpft sind.
Mikroben, die der Lunge nützen oder schaden
Die Analyse identifizierte Dutzende von Darmmikroben, die das Risiko für einzelne Atemwegserkrankungen entweder erhöhten oder verringerten, oft in krankheitsspezifischen Mustern. So schienen bestimmte Darmbakterien vor COPD, Asthma oder PAH zu schützen, während andere die Wahrscheinlichkeit für ILD oder COPD erhöhten. Hautmikroben zeigten schwächere, aber dennoch nachweisbare Zusammenhänge, wobei einige Arten mit einem höheren und andere mit einem niedrigeren Risiko für verschiedene Erkrankungen assoziiert waren. Das Team drehte die Analyse auch um und fand, dass das genetische Risiko für COPD, Asthma und andere Lungenerkrankungen seinerseits Veränderungen im Darm- und Hautmikrobiom vorhersagte. Dieser bidirektionale Verkehr deutet auf eine Rückkopplungsschleife hin: Mikroben können die Lungenkrankheit mitgestalten, und die Lungenkrankheit kann unser mikrobielles Ökosystem verändern.
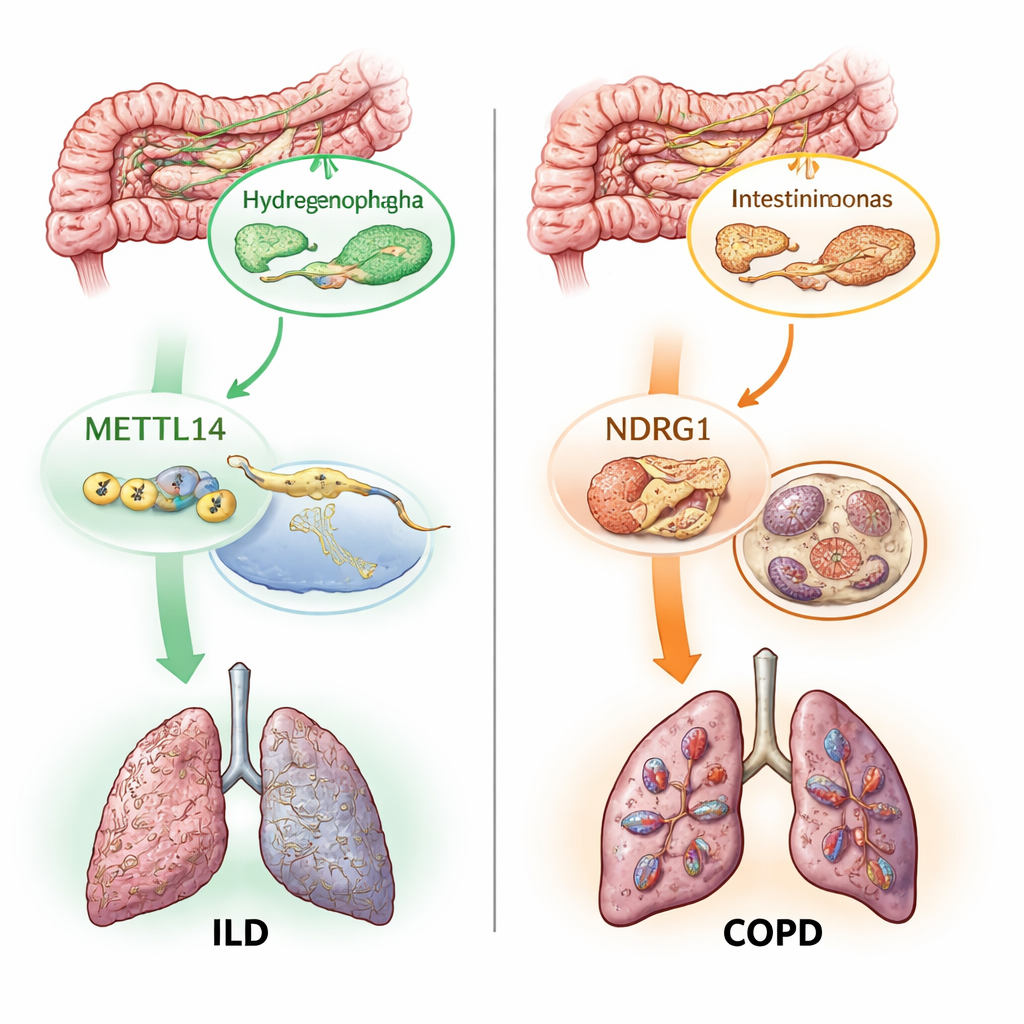
Zwei molekulare Schalter: RNA‑Marken und eisenabhängiger Zelltod
Über die Kartierung relevanter Mikroben hinaus fragten die Autorinnen und Autoren, wie diese mikroskopischen Partner Lungengewebe beeinflussen könnten. Sie konzentrierten sich auf zwei molekulare Prozesse, die bereits im Zusammenhang mit Lungenschäden vermutet werden. Die erste, die m6A‑Modifikation, ist ein kleines chemisches Etikett auf RNA, das reguliert, wie Gene an- und abgeschaltet werden. Die zweite, Ferroptose, ist eine Form eisenabhängigen Zelltods, die durch unkontrollierte Oxidation von Fetten in Zellmembranen ausgelöst wird. Mithilfe genetischer Stellvertreter für 19 m6A‑bezogene Gene und Hunderte ferroptosebezogener Gene testeten sie, ob Veränderungen in diesen Wegen kausal mit Lungenerkrankungen verknüpft sind. Sie fanden, dass ein m6A‑Writer‑Gen, METTL14, mit einem geringeren Risiko für ILD assoziiert war, während mehrere Ferroptose‑Gene, darunter NDRG1, mit einem höheren Risiko für COPD, ILD und Asthma verknüpft waren.
Die Verbindung herstellen: Von Mikroben über Zellen zur Krankheit
Der neuartigste Teil der Arbeit bestand darin, nachzuzeichnen, wie diese Bausteine in Kausalketten zusammenpassen. Statistische Mediationsanalysen deuteten darauf hin, dass ein Teil des schützenden Effekts von METTL14 auf ILD über Veränderungen vermittelt wird, die es in einem bestimmten Darmkeim namens Hydrogenophaga erzeugt. In einem anderen Pfad schien ein spezifisches Darmbakterium, Intestinimonas massiliensis, das COPD‑Risiko teilweise dadurch zu beeinflussen, dass es NDRG1 und das Ferroptose‑Programm aktiviert. Das Team überprüfte anschließend Daten aus menschlichem Lungengewebe und bestätigte, dass sowohl METTL14 als auch NDRG1 in kranken gegenüber gesunden Proben unterschiedlich exprimiert sind. Schließlich klärten Einzelzell‑genetische Karten von Immunzellen auf, dass NDRG1s schädlicher Effekt auf COPD auf eine bestimmte Untergruppe von Immunzellen — eine Art Monozyten — zurückzuführen ist, was nahelegt, dass künftige Medikamente gegen dieses Gen zelltypspezifisch wirken müssten.
Was das für künftige Therapien bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft: Lungen‑Gesundheit hängt nicht nur davon ab, was wir einatmen, sondern auch von den Mikroben, die in und auf uns leben, und den molekularen Schaltern, die sie in unseren Zellen umlegen. Diese Studie kann nicht jeden Schritt experimentell beweisen und ist vor allem auf Personen europäischer Abstammung beschränkt, liefert aber starke genetische Hinweise darauf, dass Darmmikroben, RNA‑Marken wie m6A und eisenabhängiger Zelltod eine verknüpfte Kausalkette bilden, die zu chronischer Lungenschädigung führt. Langfristig könnte diese Forschung neue Strategien inspirieren, die mikrobiombasierte Therapien mit Wirkstoffen gegen METTL14, NDRG1 oder Ferroptose kombinieren — mit dem Ziel, nicht nur Symptome zu lindern, sondern die biologischen Schaltkreise zu unterbrechen, die das Fortschreiten chronischer Atemwegserkrankungen antreiben.
Zitation: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Schlüsselwörter: Darmmikrobiom, chronische Lungenerkrankung, Asthma und COPD, RNA-Epigenetik, Zelltodwege