Clear Sky Science · de
Integrative Analysen des Transkriptoms metastasierter Tumoren enthüllen klinisch unterscheidbare zelluläre Zustände und Ökosysteme
Warum die Nachbarschaft rund um Tumoren wichtig ist
Die meisten Menschen wissen, dass Krebs in entfernte Organe streuen kann — und dass dieses Metastasieren die Mehrheit der Krebstodesfälle verursacht. Weniger bekannt ist jedoch, dass jeder metastasierte Tumor eher einer geschäftigen Stadt als einem einfachen Klumpen von Krebszellen gleicht. Er enthält viele Arten normaler und maligner Zellen, die miteinander interagieren, konkurrieren und kooperieren — auf Weisen, die die Krankheit entweder bremsen oder ihr Wachstum fördern können. Diese Studie kartiert diese verborgenen „Nachbarschaften“ in Tausenden metastasierter Tumoren und liefert Hinweise darauf, warum manche Patientinnen und Patienten länger leben und besser auf Behandlungen ansprechen als andere.
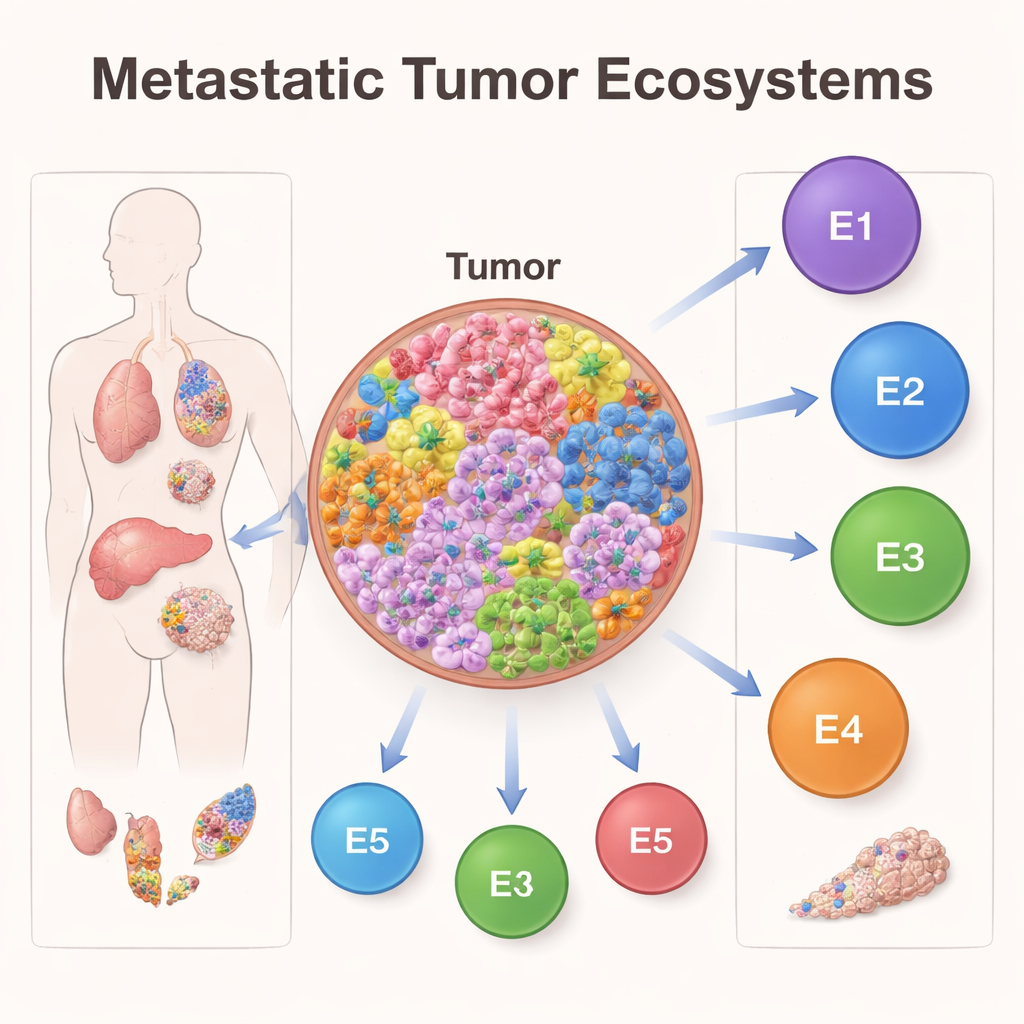
Blick in Tausende metastasierter Tumoren
Die Forschenden analysierten Genaktivitätsdaten von 2.822 Patientinnen und Patienten mit metastasiertem Krebs über 25 Tumorarten hinweg, darunter Prostata-, Haut- und Brustkrebs. Statt einzelne Zellen unter dem Mikroskop zu untersuchen, nutzten sie fortgeschrittene rechnerische Methoden, um aus Bulk-Gewebe-Daten zu „entmischen“ und abzuschätzen, welche Zelltypen vorhanden waren und wie aktiv ihre Gene waren. Mit einem maschinellen Lernverfahren namens EcoTyper gruppierten sie Zellen in wiederkehrende Muster der Genaktivität, die sie zelluläre Zustände nennen, und betrachteten dann, wie diese Zustände sich zu breiteren Ökosystemen innerhalb der Tumoren zusammenlagern.
Viele Zelltypen, viele Persönlichkeiten
Innerhalb der metastasierten Tumoren konzentrierte sich das Team auf 12 Hauptzellarten, etwa maligne epitheliale Zellen, Immunzellen (darunter T‑Zellen, B‑Zellen und natürliche Killerzellen), Gefäßzellen und Fibroblasten, die das Gewebegerüst formen. Über diese 12 Typen hinweg identifizierten sie 45 unterschiedliche zelluläre Zustände — im Grunde „Persönlichkeitsmodi“, die Zellen annehmen können. Beispielsweise waren einige T‑Zell‑Zustände auf Angriff ausgerichtet, während andere erschöpft wirkten und weniger fähig waren, Krebs zu bekämpfen. Bestimmte Fibroblasten‑Zustände standen mit einer Umbildung des Gewebes in Verbindung, die die Tumorausbreitung begünstigen kann. Diese Zustände traten nicht zufällig auf: Ihre Häufigkeiten variierten je nach ursprünglichem Krebstyp und dem Organ, in dem metastasiert wurde, was den starken Einfluss sowohl des Tumorursprungs als auch der lokalen Umgebung zeigt.
Fünf Tumorökosysteme, die mit dem Überleben verknüpft sind
Als die Forschenden betrachteten, welche zellulären Zustände typischerweise zusammen auftreten, entdeckten sie fünf große Ökosysteme oder „Ökotypen“ innerhalb metastasierter Tumoren. Jeder Ökotyp war eine charakteristische Mischung von Zelltypen und Zuständen. Manche waren reich an verschiedenen Immun‑ und Stromazellen, andere wurden stärker von malignen Zellen dominiert. Diese Ökotypen sind nicht nur akademische Kategorien — sie korrelierten stark mit der Überlebenszeit der Patientinnen und Patienten. Ein Ökotyp, bezeichnet als E5, war mit vergleichsweise guten Ergebnissen verbunden, während andere, insbesondere E2 und E3, mit schlechterer Überlebensrate verknüpft waren. Dieselben Ökotyp‑Muster traten über verschiedene Krebsarten und Organe hinweg auf, was darauf hindeutet, dass sie allgemeine Regeln der Organisation metastasierter Tumoren erfassen.
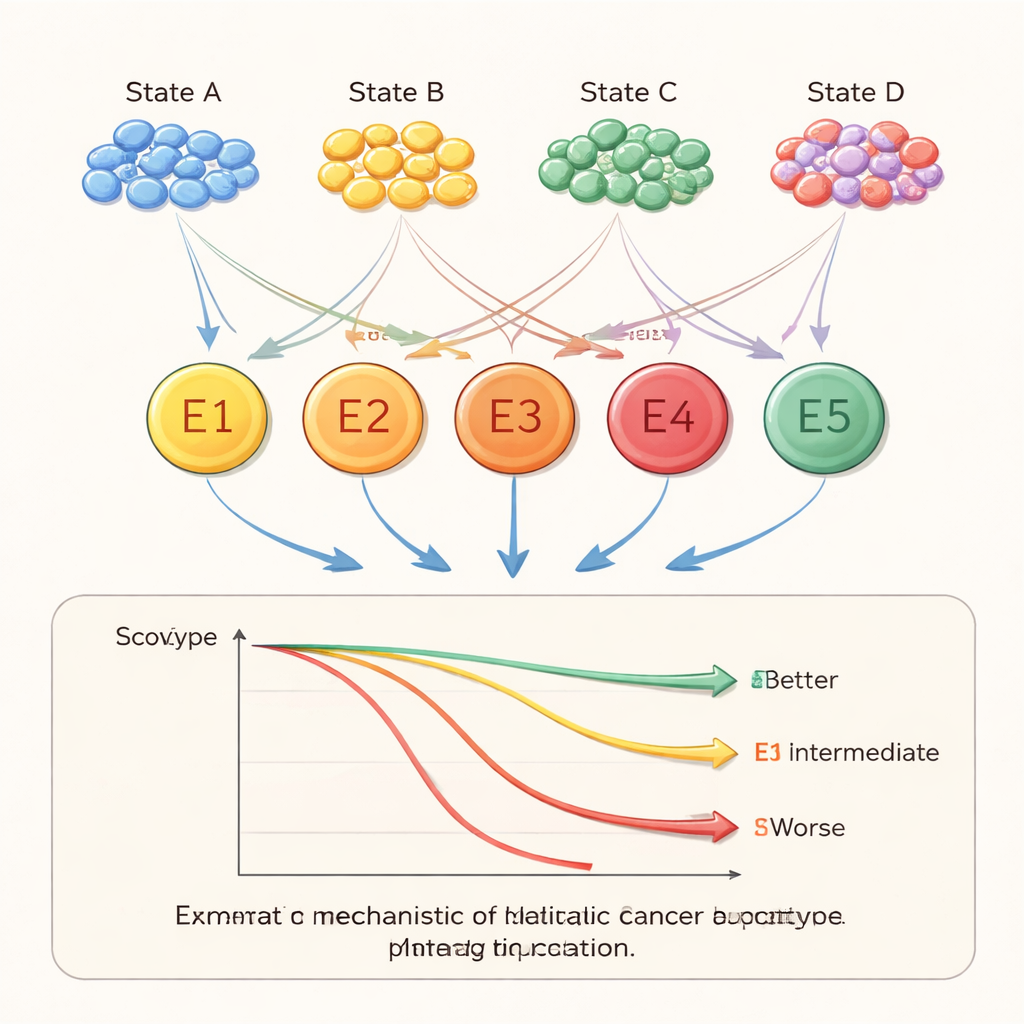
Immunaktivität, Therapieansprechen und Kontrollschalter
Um zu verstehen, was diese Ökosysteme tun, untersuchte das Team, welche biologischen Signalwege in ihren Genen aktiv waren. Viele zelluläre Zustände zeigten Anreicherungen in Immunfunktionen oder klassischen Krebswege, etwa Reaktionen auf niedrigen Sauerstoffgehalt oder Signale, die Zellteilung und Invasion antreiben. Ein Ökotyp (E1) zeigte starke Immun‑ und Entzündungsaktivität sowie hohe Anteile an Immun‑ und Stromazellen, während ein anderer (E2) in Wachstums‑ und Zellzykluswege angereichert war, die mit aggressiver Erkrankung verbunden sind. Die Forschenden untersuchten auch Marker im Zusammenhang mit modernen Immuntherapien. Einige Ökotypen wiesen Merkmale auf, die nahelegen, dass Tumoren der Immunabwehr entgehen und schlecht auf Checkpoint‑Blocker reagieren könnten, während andere eher profitieren könnten. Schließlich identifizierten sie durch das Durchsuchen nach Transkriptionsfaktoren — den Mastersteuerungen, die Genprogramme kontrollieren — mehrere Kandidaten, darunter SPIB, SRF und NR1D1, die offenbar helfen, diese Ökosysteme zu formen und selbst mit der Prognose der Patientinnen und Patienten verknüpft waren.
Was das für Patientinnen und Patienten bedeutet
Für Nicht‑Fachleute ist die Kernbotschaft: Metastasierte Tumoren sind nicht alle gleich, auch wenn die Diagnose dieselbe ist. Sie bestehen aus wiederkehrenden Kombinationen von Zell‑„Persönlichkeiten“ und Ökosystemen, die die Krankheit entweder bremsen oder beschleunigen können, und diese Muster hinterlassen nachweisbare Spuren in Genaktivitätsdaten. Indem sie 45 zelluläre Zustände und fünf Haupt‑Tumorökosysteme in Tausenden von Patientinnen und Patienten kartierten, liefert diese Arbeit einen hochauflösenden Atlas der metastasierten Tumormikroumgebung. Künftig könnten solche Karten Ärzten helfen vorherzusagen, welche Patientinnen und Patienten ein höheres Risiko haben, wer am ehesten von bestimmten Behandlungen — insbesondere Immuntherapien — profitiert und welche zellulären Schalter die vielversprechendsten Ziele für neue Medikamente sein könnten.
Zitation: Zhang, C., Li, S., Yu, Y. et al. Integrative analyses of metastatic cancer transcriptome reveal clinically distinct cellular States and ecosystems. Sci Rep 16, 7343 (2026). https://doi.org/10.1038/s41598-026-36512-3
Schlüsselwörter: metastasierter Krebs, tumormikroumgebung, zelluläre Zustände, immunes Ökosystem, präzisionsonkologie