Clear Sky Science · de
Integrierter BSI-Bakterienidentifikator-on-Chip mit approximativer k‑Mer-Übereinstimmung
Warum schnellere Keimerkennung wichtig ist
Bei Patientinnen und Patienten, die lebensrettende Stammzelltransplantationen erhalten, können Infektionen im Blutkreislauf die Erholung innerhalb weniger Stunden in einen medizinischen Notfall verwandeln. Ärztinnen und Ärzte wissen, dass jede Minute zählt, doch die heutigen Labormethoden zur Ermittlung der ursächlichen Bakterien sind oft langsam oder erfordern leistungsstarke Rechner. Diese Studie stellt einen winzigen, energieeffizienten Computerchip vor – PC‑CAM –, der DNA aus Patientenproben schnell durchsuchen und gefährliche Bakterien in Echtzeit markieren kann, potenziell direkt am Krankenbett.
Das Infektionsrisiko nach einer darmrettenden Behandlung
Manche Transplantationspatienten entwickeln eine schwere Komplikation, bei der die gespendeten Immunzellen den Darm des Patienten angreifen. Eine vielversprechende Behandlung ist die fäkale Mikrobiota-Transplantation, bei der gesunde Darmmikroben eines Spenders in den Patienten übertragen werden. Während dies den Darm retten kann, bringt es mitunter ein zusätzliches Risiko: schädliche Darmbakterien können in den Blutkreislauf gelangen und lebensbedrohliche Infektionen auslösen. Um diese Infektionen effektiv zu behandeln, müssen Ärzte schnell herausfinden, welche Bakterienarten vorhanden sind, doch herkömmliche Tests können Stunden bis Tage dauern und unbekannte Stämme übersehen.
Vom langsamen Aufbau ganzer Genome zu schnellen DNA-Fragmenten
Moderne DNA-Sequenzer können genetisches Material nahezu in Echtzeit direkt aus Blut- oder Stuhlproben lesen. Der Flaschenhals ist nicht mehr das Auslesen der DNA, sondern ihre Interpretation. Konventionelle Methoden versuchen zunächst, ganze Genome aus Millionen kurzer DNA-Stücke zusammenzusetzen und diese dann mit einer Referenzbibliothek abzugleichen – ein rechenintensiver Prozess. Die Autoren ersetzen dies durch eine einfachere Strategie: Sie zerlegen die DNA in kurze, fest lange Stücke, sogenannte k‑Mer, und suchen diese Stücke direkt in einer Datenbank bekannter bakterieller Sequenzen. Statt einer perfekten Buchstaben-für-Buchstaben-Übereinstimmung toleriert ihr System eine bestimmte Anzahl von Unterschieden, wodurch es mit den unvermeidlichen Fehlern bei der Sequenzierung und natürlichen Mutationen umgehen kann. 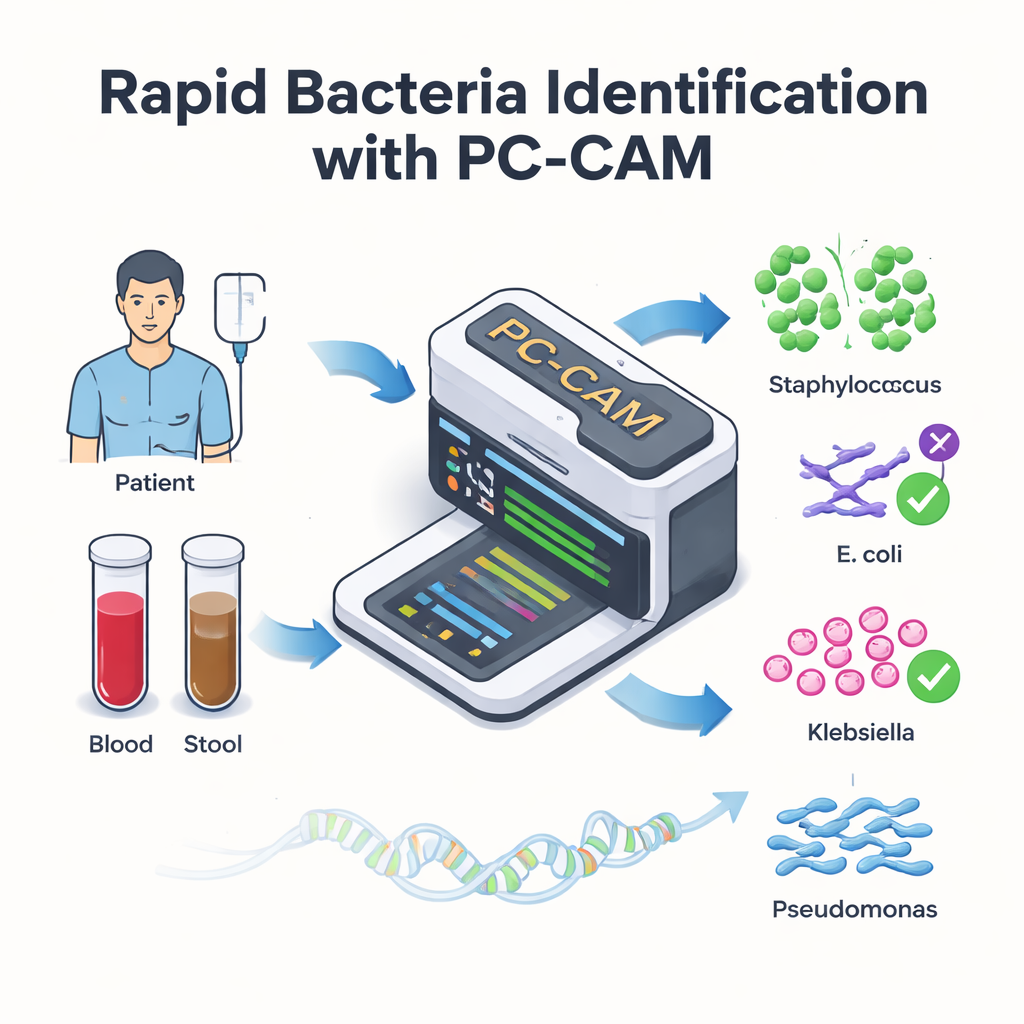
Ein intelligenter Speicherchip für DNA-Suchen
Kernstück von PC‑CAM ist eine spezialisierte Speicherart namens Content-Addressable Memory, die eingehende Daten gleichzeitig gegen den gesamten gespeicherten Inhalt vergleichen kann. Die Forschenden entwickelten eine „approximate search“-Variante dieses Speichers (ACAM), die so eingestellt werden kann, dass sie Nah‑Treffer statt exakter Übereinstimmungen akzeptiert. Jedes kurze DNA‑Fragment wird kodiert und als Zeile in diesem Speicher abgelegt. Wenn ein neues Fragment aus einer Patientenprobe eintrifft, aktiviert der Chip eine Suchleitung durch alle Zeilen gleichzeitig und misst, wie schnell winzige elektrische Signale entladen werden. Durch Anpassung zweier Steuerungen kann das System eine Schwelle einstellen, wie viele Fehlstellen es toleriert, und damit festlegen, wie nachsichtig die Übereinstimmung sein soll. Dieser Vergleich auf Hardware‑Ebene erlaubt es dem Chip, Muster deutlich schneller und mit weniger Energieaufwand als ein Universalrechner zu durchsuchen.
Wie gut der Chip echte Bakterien findet
Das Team testete PC‑CAM an realen Datensätzen von Patientinnen und Patienten, die eine fäkale Mikrobiota‑Transplantation erhalten hatten, und verglich die im Blut und Stuhl nachgewiesenen Bakterien mit den Ergebnissen einer vollständigen, softwarebasierten Genomanalyse. Selbst wenn der Chip nur eine kleine, sorgfältig ausgewählte Teilmenge von DNA‑Fragmenten jedes bakteriellen Genoms speicherte, stimmten seine Ergebnisse weitgehend mit der rechenintensiveren Methode überein und identifizierten bei mehreren Patienten die wesentlichen Krankheitserreger korrekt. In erweiterten Experimenten mit simulierten DNA‑Reads aus verschiedenen Bakterien und unterschiedlichen Fehlerquoten stieg die Sensitivität des Chips (seine Fähigkeit, wahre Übereinstimmungen zu erfassen), je mehr Unterschiede er tolerierte, während die Spezifität (die Fähigkeit, Fehlalarme zu vermeiden) bei sehr hoher Toleranz abnahm. Die Autoren zeigen, dass einfache Nachverarbeitungsschritte – etwa das Erfordernis mehrerer übereinstimmender Fragmente oder das Verwerfen schwacher Treffer – diese falsch-positiven Befunde reduzieren können. 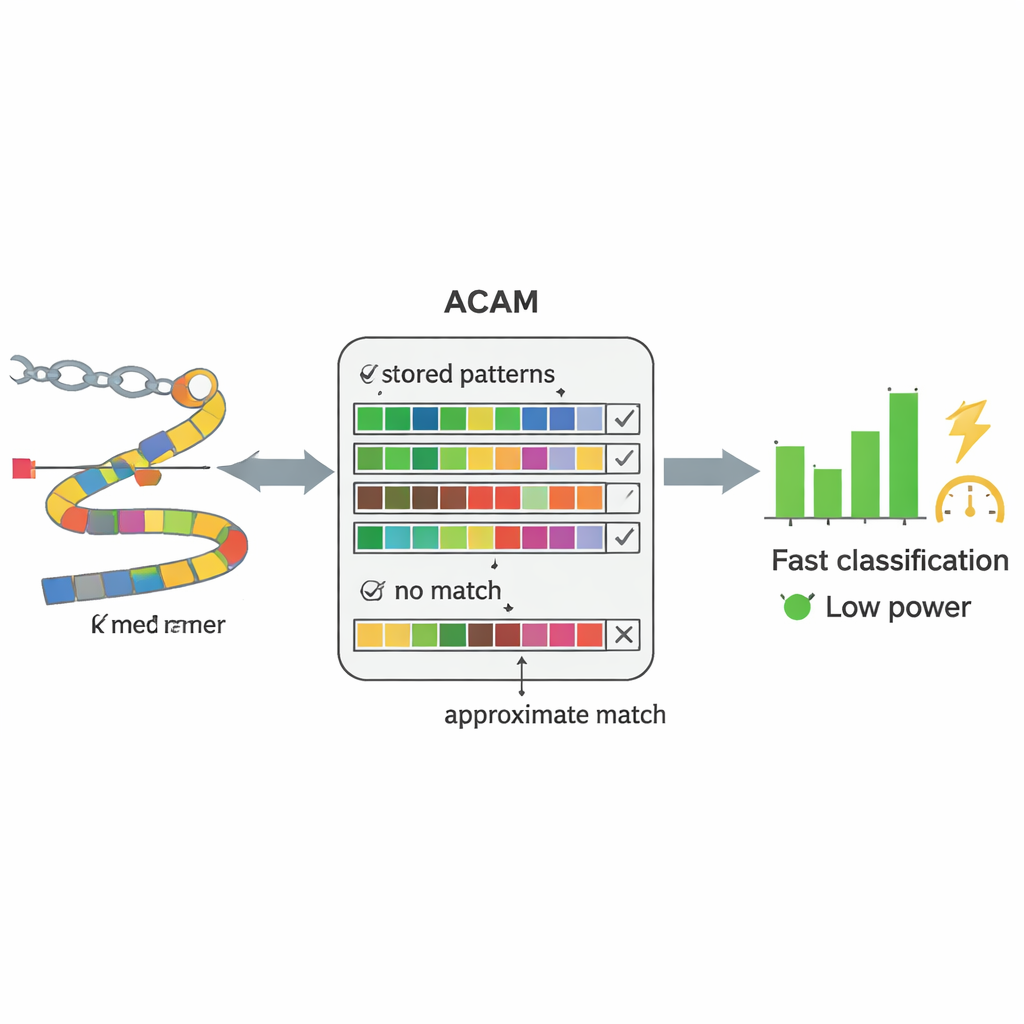
Kleine Hardware mit hoher Geschwindigkeit und geringem Stromverbrauch
PC‑CAM integriert den ACAM‑Speicher mit einem kleinen RISC‑V‑Prozessor auf einem Chip von nur wenigen Quadratmillimetern, gefertigt in einer Standard‑65‑Nanometer‑Technologie. Messungen an realer Hardware zeigen, dass er etwa 960.000 kurze DNA‑Reads pro Sekunde klassifizieren kann und dabei rund 1,27 Milliwatt Leistung verbraucht – weniger als viele digitale Armbanduhren. Im Vergleich mit einem führenden Softwarewerkzeug, das auf einem High‑End‑Desktop‑Prozessor lief, war der Chip für diese Klassifizierungsaufgabe etwa 1.900‑mal schneller. Zwar ist seine Genauigkeit durch das Speichern einer verdünnten Version jedes Genoms moderat reduziert, doch die Autoren argumentieren, dass dieser Kompromiss akzeptabel ist, wenn Geschwindigkeit und Energieverbrauch die wichtigsten Einschränkungen sind, etwa in der Notfallversorgung oder in tragbaren Geräten.
Was das für Patientinnen, Patienten und darüber hinaus bedeutet
Vereinfacht gesagt zeigt die Studie, dass ein winziger, stromsparender Chip als spezialisierte Suchmaschine für bakterielle DNA fungieren kann und gefährliche Keime in Blut- oder Stuhlproben nahezu sofort erkennt. Er ersetzt nicht die umfassende genetische Analyse in einem großen Labor, kann aber schnell vor Ort Hinweise liefern, welche Bakterien vorhanden sind, und so Ärztinnen und Ärzten helfen, früher und gezielter Antibiotika auszuwählen. Der gleiche Ansatz ließe sich auf die Überwachung von Antibiotikaresistenzen, die Kontrolle von Lebensmitteln und Trinkwasser auf Kontaminationen oder die Beobachtung von Pflanzenkrankheiten ausdehnen – alles mit kompakter Hardware, die anspruchsvolle DNA‑Analysen aus dem Rechenzentrum näher an die Stellen bringt, an denen Entscheidungen getroffen werden müssen.
Zitation: Garzón, E., Galindo, V., Harary, Y. et al. Integrated BSI bacteria identifier-on-chip using approximate k-mer matching. Sci Rep 16, 5722 (2026). https://doi.org/10.1038/s41598-026-36497-z
Schlüsselwörter: Blutstrominfektion, schnelle Krankheitserreger-Erkennung, DNA-Sequenzierung, Lab-on-a-Chip, Mikrobiom